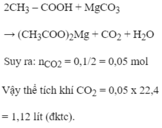CH3COOH + MgCO3 -> ? + ?

Những câu hỏi liên quan
Cho 12.6g MgCO3 vào 200g dd CH3COOH
a) Tính V ?
b) Tính nồng độ phần trăm của dd CH3COOH cần dùng
\(n_{MgCO_3}=\dfrac{12.6}{84}=0.15\left(mol\right)\)
\(Mg+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Mg+CO_2+H_2O\)
\(0.15..........0.3............................................0.15\)
\(V_{CO_2}=0.15\cdot22.4=3.36\left(l\right)\)
\(m_{CH_3COOH}=0.3\cdot60=18\left(g\right)\)
\(C\%_{CH_3COOH}=\dfrac{18}{200}\cdot100\%=9\%\)
Đúng 1
Bình luận (0)
Pthh MgCO3+2CH3COOH--->(CH3COO)2Mg+CO2+H2O
Ta có nMgCO3=0,15 mol
Theo pthh thì nCH3COOH=0,3 mol
=>mCH3COOH=17,7 g
=>C%CH3COOH=8,85%
Đúng 0
Bình luận (0)
Tính thể tích khí C O 2 thoát ra (đktc) khi đem 100ml dung dịch C H 3 C O O H 1M tác dụng với M g C O 3 dư.
Bài 5 : Cho 10,4g hỗn hợp gồm : MgO, MgCO3 tác dụng vừa đủ với 200ml dd acid CH3COOH thì thu đc 2,479 lít khí CO2 (đkc)
a) Tính thành phần % về khối lượng mỗi chất trong hỗn hợp ban đầu
b) Tính nồng độ mol dd CH3COOH cần dùng
a, \(n_{CO_2}=\dfrac{2,479}{24,79}=0,1\left(mol\right)\)
PT: \(MgO+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Mg+H_2O\)
\(MgCO_3+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Mg+CO_2+H_2O\)
Theo PT: \(n_{MgCO_3}=n_{CO_2}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{MgCO_3}=\dfrac{0,1.84}{10,4}.100\%\approx80,77\%\\\%m_{MgO}\approx19,23\%\end{matrix}\right.\)
b, \(n_{MgO}=\dfrac{10,4-0,1.84}{40}=0,05\left(mol\right)\)
Theo PT: \(n_{CH_3COOH}=2n_{MgO}+2n_{MgCO_3}=0,3\left(mol\right)\)
\(\Rightarrow C_{M_{CH_3COOH}}=\dfrac{0,3}{0,2}=1,5\left(M\right)\)
Đúng 2
Bình luận (0)
Câu 10: Hòa tan 31,8 gam hỗn hợp X gồm MgCO3 và CaCO3 bằng dung dịch CH3COOH vừa đủ thu được dung dịch A và 7,84 lít khí CO2 ( đktc). a) Tính % khối lượng các chất trong X.b) Tính thể tích dung dịch CH3COOH 2M đã dùng.c) Cô cạn dung dịch A được bao nhiêu gam muối khan.Giúp mình với pls mai mình thi r :
Đọc tiếp
Câu 10: Hòa tan 31,8 gam hỗn hợp X gồm MgCO3 và CaCO3 bằng dung dịch CH3COOH vừa đủ thu được dung dịch A và 7,84 lít khí CO2 ( đktc).
a) Tính % khối lượng các chất trong X.
b) Tính thể tích dung dịch CH3COOH 2M đã dùng.
c) Cô cạn dung dịch A được bao nhiêu gam muối khan.
Giúp mình với pls mai mình thi r :<
Hơi muộn nhé, lần sau bạn đăng sớm hơn chứ hầu hết giờ nay mọi người đi ngủ rồi, chúc bạn thi tốt nhé ^^
a) Gọi \(\left\{{}\begin{matrix}n_{MgCO_3}=a\left(mol\right)\\n_{CaCO_3}=b\left(mol\right)\end{matrix}\right.\)
\(n_{CO_2}=\dfrac{7,84}{22,4}=0,35\left(mol\right)\)
PTHH:
MgCO3 + 2CH3COOH ---> (CH3COO)2Mg + CO2 + H2O
a---------->2a-------------------->a----------------->a
CaCO3 + 2CH3COOH ---> (CH3COO)2Ca + CO2 + H2O
b---------->2b------------------>b------------------>b
=> \(\left\{{}\begin{matrix}84a+100b=31,8\\a+b=0,35\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\left(mol\right)\\b=0,15\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}m_{MgCO_3}=0,2.84=16,8\left(g\right)\\m_{CaCO_3}=0,15.100=15\left(g\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}\%m_{MgCO_3}=\dfrac{16,8}{31,8}.100\%=52,8\%\\\%m_{CaCO_3}=100\%-52,8\%=47,2\%\end{matrix}\right.\)
b) \(V_{dd}=\dfrac{2.0,2+2.0,15}{2}=0,35\left(l\right)\)
c) \(m_{muối}=0,2.142+0,15.158=52,1\left(g\right)\)
Đúng 2
Bình luận (0)
Câu 8. Cho 42 (g) MgCO3 vào dung dịch CH3COOH 2M. a. Tính thể tích chất khí thoát ra (đktc) b. Tính thể tích dung dịch axit tham gia phản ứng c. Trung hòa dung dịch axit trên bằng 300 (ml) dung dịch NaOH. Tính nồng độ mol dung dịch thu được
Câu 8 :
\(n_{MgCO3}=\dfrac{42}{84}=0,5\left(mol\right)\)
Pt : \(2CH_3COOH+MgCO_3\rightarrow\left(CH_3COO\right)_2Mg+CO_2+H_2O\)
1 0,5 0,5
a) \(V_{CO2\left(dktc\right)}=0,5.22,4=11,2\left(l\right)\)
b) \(V_{CH3COOH}=\dfrac{1}{2}=0,5\left(l\right)\)
c) Pt : \(CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\)
1 1
300ml = 0,3l
\(C_{MCH3COONa}=\dfrac{1}{0,3}=\dfrac{10}{3}\left(M\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
cho m gam hỗn hợp X gồm Mg và MgCO3 tác dụng hết với dung dịch CH3COOH sau phản ứng thu được hỗn hợp khí A. Dẫn toàn bộ khí A vào dung dịch Ca(OH)2 dư thì thu được 5g kết tủa và còn lại 4,48l khí không màu
a. viet PTHH
b. xác định m
Gọi \(\left\{{}\begin{matrix}n_{Mg}:x\left(mol\right)\\n_{MgCO3}:y\left(mol\right)\end{matrix}\right.\)
\(2CH_3COOH+Mg\rightarrow\left(CH_3COO\right)_2Mg+H_2\)
\(MgCO_3+2CH_3COOH\rightarrow\left(CH_3COO\right)_2Mg+CO_2+H_2O\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
Ta có:
\(n_{CaCO3}=n_{CO2}=y=\frac{5}{100}=0,05\left(mol\right)\)
\(n_H=x=\frac{4,48}{22,4}=0,2\left(mol\right)\)
\(\Rightarrow m=0,2.24+0,05.120=10,8\left(g\right)\)
Đúng 0
Bình luận (0)
Câu 1. Cho các công thức hoá học: O3 ; NO2 ; Cu ; MgCO3 ; S ; KOH ; H2S. Các công thức hoá học biểu diễn hợp chất là:A. NO2 ; H2S ; S ; MgCO3 B. H2S ; Cu ; MgCO3 ; O3C. MgCO3; H2S ; NO2 ; S D. KOH ; H2S ; MgCO3 ; NO2 Câu 3. Công thức của nhôm oxit (tạo bởi Al (III) và O) và kali oxit (tạo bởi K (I) và O) lần lượt là:A. Al2O3 và KO B. Al2O3 và K2O C. Al2O và KO D. AlO...
Đọc tiếp
Câu 1. Cho các công thức hoá học: O3 ; NO2 ; Cu ; MgCO3 ; S ; KOH ; H2S. Các công thức hoá học biểu diễn hợp chất là:
A. NO2 ; H2S ; S ; MgCO3 B. H2S ; Cu ; MgCO3 ; O3
C. MgCO3; H2S ; NO2 ; S D. KOH ; H2S ; MgCO3 ; NO2
Câu 3. Công thức của nhôm oxit (tạo bởi Al (III) và O) và kali oxit (tạo bởi K (I) và O) lần lượt là:
A. Al2O3 và KO B. Al2O3 và K2O C. Al2O và KO D. AlO3 và K2O
Câu 8. 2 mol nguyên tử Al có chứa số nguyên tử Al là:
A. 1,8.1022 B. 12.1023 C. 6.1023 D. 6.1022
Câu 9. Cho phản ứng nhiệt phân sau: KClO3 ⟶ KCl + O2. Khi đem nhiệt phân hoàn toàn 0,6 mol KClO3 thì số mol KCl và O2 thu được lần lượt là:
A. 0,6 mol và 0,9 mol. B. 0,6 mol và 0,6 mol.
C. 0,5 mol và 0,4 mol. D. 0,3 mol và 0,9 mol.
Câu 10. Trong phản ứng: Kẽm + Axit clohiđric → Kẽm clorua + khí Hiđro. Axit clohiđric là
A. chất sản phẩm. B. chất phản ứng. C. xúc tác. D. môi trường.
Câu 15. Số nguyên tử có trong 1 mol phân tử CO2 là:
A. 6. 1023 nguyên tử B. 9. 1023 nguyên tử
C. 12. 1023 nguyên tử D. 18. 1023 nguyên tử
Câu 21. Số phân tử oxi chứa trong 1,5 mol phân tử oxi là:
A. 1,8.1022 B. 6.1023 C. 9.1023 D. 18.1023
Câu 23. Khối lượng của N phân tử NaBr là:
A. 93 gam B. 103 gam C. 102 đvC D. 100 gam
TỰ LUẬN
Câu 2. Cho sơ đồ phản ứng: 𝐻2+𝑂2 → 𝐻2𝑂. Tính khối lượng khí oxi cần dùng để phản ứng hết với 3,36 lít khí hiđro (đktc) ?
Câu 4. Hãy tính:
b. Khối lượng của hỗn hợp khí A gồm 11,2 lít khí N2 và 3,36 lít khí CO ở điều kiện tiêu chuẩn.
d. Tính khối lượng của Fe trong 92,8 g Fe3O4 ?
Câu 1. Hãy tính số mol của:
a. 5,35 gam Fe(OH)3. b. 0,56 lít khí NH3 (đktc). c. 11g khí CO2.
Câu 2. Hãy tính khối lượng của:
a. 0,03 mol khí CH4. b. 0,5 mol CuSO4. c. 2,24 lít khí CO (đktc)
Câu 3. Hãy tính thể tích (đktc) của:
a. 0,2 mol khí C2H4. b. 3 mol khí CO2.
b. 1,6 gam khí O2. d. 6,8 gam khí H2S.
Câu 1: D
Câu 3: B
Câu 8: B
Câu 9: A
Câu 10: B
Câu 15: D
Câu 21: C
Câu 23: B
Câu 2:
a) \(m_{CH_4}=n.M=0,03.16=0,48\left(g\right)\)
b) \(m_{C\text{uS}O_4}=n.M=0,5.160=80\left(g\right)\)
c) \(n_{CO}=\dfrac{V_{\left(\text{đ}ktc\right)}}{22,4}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
`=>` \(m_{CO}=n.M=0,1.28=2,8\left(g\right)\)
Câu 3:
a) \(V_{C_2H_4\left(\text{đ}ktc\right)}=n.22,4=0,2.22,4=4,48\left(l\right)\)
b) \(V_{CO_2\left(\text{đ}ktc\right)}=n.M=3.22,4=67,2\left(l\right)\)
c) \(n_{O_2}=\dfrac{m}{M}=\dfrac{1,6}{32}=0,05\left(mol\right)\)
`=>` \(V_{O_2\left(\text{đ}ktc\right)}=n.22,4=0,05.22,4=1,12\left(l\right)\)
d) \(n_{H_2S}=\dfrac{m}{M}=\dfrac{6,8}{34}=0,2\left(mol\right)\)
`=>` \(V_{H_2S\left(\text{đ}ktc\right)}=n.22,4=0,2.22,4=4,48\left(l\right)\)
Đúng 1
Bình luận (0)
AI GIÚP LUÔN VỚI ĐC HOK Ạ
ĐANG CẦN GẤP LẮM Ạ
Đúng 0
Bình luận (0)
BT4. Cho 8,4 g MgCO3 vào HCl thu được MgCl2, H2O và 1,12 l CO2 ở đktc
a) Chứng minh MgCO3 còn dư và tính khối lượng MgCO3 dư
b)Tính khối lượng HCl đã tham gia phản ứng
nMgCO3 = 8.4/84 = 0.1 mol
nCO2 = 0.05 mol
MgCO3 + 2HCl => MgCl2 + CO2 + H2O
0.05______0.1___________0.05
nMgCO3= 0.05 < 0.1 => MgCO3 dư
mMgCO3 dư = 0.05*84 = 4.2 g
mHCl = 0.1*36.5 = 3.65 g
Đúng 2
Bình luận (0)
Cho các chất sau đây tác dụng với nhau: CH3COOH + Na2CO3
→
CH3COOH + C6H5ONa
→
CH3COOH + Ca(OH)2
→
CO2+ H2O + CH3COONa
→
CH3COOH + CaCO3
→
CH3COOH + Cu(OH)2
→
CH3COOH + KHCO3
→
Số phản ứng xảy ra đồng thời chứng minh được lực axit của axit axetic mạnh hơn axit cacbonic là A. 2. B. 3. C. 4. D. 5.
Đọc tiếp
Cho các chất sau đây tác dụng với nhau:
CH3COOH + Na2CO3 →
CH3COOH + C6H5ONa →
CH3COOH + Ca(OH)2 →
CO2+ H2O + CH3COONa →
CH3COOH + CaCO3 →
CH3COOH + Cu(OH)2 →
CH3COOH + KHCO3 →
Số phản ứng xảy ra đồng thời chứng minh được lực axit của axit axetic mạnh hơn axit cacbonic là
A. 2.
B. 3.
C. 4.
D. 5.
Đáp án B.
3.
CH3COOH + Na2CO3 →
CH3COOH + CaCO3 →
CH3COOH + KHCO3 →
Đúng 0
Bình luận (0)