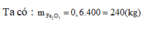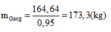Tính khối lượng sắt có trong 100 tấn quặng hematit chứa 60% Fe2O3

Những câu hỏi liên quan
Bài 2. Hãy tính:
a) Khối lượng sắt có trong 10 tấn quặng hematit chứa 60% Fe2O3 (còn lại là tạp chất không chứa sắt).
b) Tổng số nguyên tử của các nguyên tố có trong 36 gam H2O
a) mFe2O3= 60%.10=6(tấn)
=> mFe= (112/160).6= 4,2(tấn)
b) nH2O=36/18=2(mol)
=> Số mol nguyên tử trong 2 mol H2O là: 2.2+ 2.1=6(mol)
Tổng số nguyên tử của các nguyên tố trong 36 gam H2O là:
6.6.1023=3,6.1024 (nguyên tử)
Chúc em học tốt!
Đúng 2
Bình luận (1)
1.Tính khối lượng Cu CÓ TRONG 48g CuSO4?
2.Tính lượng sắt có trong 60 tấn quặng sắt chứa 80% Fe2O3
1, \(n_{CuSO_4}=\dfrac{48}{160}=0,3 (mol)\)
\(n_{Cu}=n{CuSO_4}=0,3 mol\)
\(=> m_{Cu}=0,3 \) x 64 = 19, 2 (gam)
2, CHỊU
Đúng 1
Bình luận (0)
\(n=\dfrac{m}{M}=\dfrac{48}{160}=0,3\left(mol\right)\)
\(=>m=0,3.64=19,2\left(g\right)\)
Đúng 1
Bình luận (0)
Cần bao nhiêu tấn quặng hematit chứa 85% Fe2O3 để có một lượng sắt bằng lượng sắt có trong 2,4 tấn muối chứa trong 80% muối sắt (II) sunphat
Tính khối lượng quặng hematit chứa 60% Fe2O3 để sane xuất đc 1 tấn gang chứa 95% Fe.Biết hiệu suất quá trình phản ứng la 80
giúp với
Từ 400kg quặng hematit đỏ chứa 60% Fe2O3 về khối lượng) có thể luyện được m kg gang có hàm lượng sắt bằng 95%. Biết lượng sắt bị hao hụt trong sản xuất là 2%. Giá trị của m là: A. 116,2 B. 180,5 C. 155,1 D. 173,3
Đọc tiếp
Từ 400kg quặng hematit đỏ chứa 60% Fe2O3 về khối lượng) có thể luyện được m kg gang có hàm lượng sắt bằng 95%. Biết lượng sắt bị hao hụt trong sản xuất là 2%. Giá trị của m là:
A. 116,2
B. 180,5
C. 155,1
D. 173,3
Để sản xuất một lượng gang như nhau người ta đã dùng m1 tấn quặng hematit chứa 60% Fe2O3 và m2 tấn quặng manhetit chứa 69,6% Fe3O4. Tính tỉ lệ m1 : m2 ?
Mọi người ơi giúp em lẹ đi ạ!
Em đang cần gấp!
Đúng 0
Bình luận (0)
Chọn lượng chất : 1 mol Fe
=> nFe2O3 = 0,5 (mol) ; nFe3O4 = 1/3 (mol)
=> mFe2o3 = 80 (g) ; mFe3o4 = 232/3 (g)
=> m1 = 80.100/60 = 400/3 (g) ;
m2 = (232/3).100/69,6 = 1000/9 (g)
=> m1 : m2 = 6/5
Đúng 1
Bình luận (0)
%mFe/Fe2O3= 70%
=> %mFe/hematit= 70% x 60%= 42%m1
mFe/Fe3O4= 168/232
=> %mFe/manhetit= 168/232 x 69,6%= 50,4%m2
Vì: 42%m1= 50,4%m2
<=> m1/m2= 50,4%/42%=6/5
Đúng 0
Bình luận (0)
Hematit là quặng phổ biến nhất của sắt trong tự nhiên, được dùng để sản xuất gang. Từ 1 tấn quặng hematit (chứa 70% oxit sắt về khối lượng, còn lại là tạp chất trơ) có thể sản xuất được lượng gang thành phẩm (chứa 5% C về khối lượng) tối đa là A. 506,9 kg B. 515,8 kg C. 533,6 kg D. 490 kg
Đọc tiếp
Hematit là quặng phổ biến nhất của sắt trong tự nhiên, được dùng để sản xuất gang. Từ 1 tấn quặng hematit (chứa 70% oxit sắt về khối lượng, còn lại là tạp chất trơ) có thể sản xuất được lượng gang thành phẩm (chứa 5% C về khối lượng) tối đa là
A. 506,9 kg
B. 515,8 kg
C. 533,6 kg
D. 490 kg
Đáp án B
Ta có: m(Fe2O3) = 7.103 (kg) → n(Fe2O3) = 4,375 mol → n(Fe trong gang) = 4,375. 2 = 8,75
→ m(Fe trong gang) = 490 → m(gang) = 490. 100 : 95 = 515,8 (kg)
Đúng 0
Bình luận (0)
Hematit là quặng phổ biến nhất của sắt trong tự nhiên, được dùng để sản xuất gang. Từ 1 tấn quặng hematit (chứa 70% oxit sắt về khối lượng, còn lại là tạp chất trơ) có thể sản xuất được lượng gang thành phẩm (chứa 5% C về khối lượng) tối đa là A. 506,9 kg B. 515,8 kg C. 533,6 kg D. 490 kg
Đọc tiếp
Hematit là quặng phổ biến nhất của sắt trong tự nhiên, được dùng để sản xuất gang. Từ 1 tấn quặng hematit (chứa 70% oxit sắt về khối lượng, còn lại là tạp chất trơ) có thể sản xuất được lượng gang thành phẩm (chứa 5% C về khối lượng) tối đa là
A. 506,9 kg
B. 515,8 kg
C. 533,6 kg
D. 490 kg
Đáp án B
Ta có: m(Fe2O3) = 7.103 (kg) → n(Fe2O3) = 4,375 mol → n(Fe trong gang) = 4,375. 2 = 8,75
→ m(Fe
trong gang) = 490 → m(gang) = 490. 100 : 95 = 515,8 (kg) Câu 86: Đáp án D
Gọi n(Fe) = a và n(C) = b → 56a + 12b = 99,2
BT e: 3a + 4b =2n(SO2) → n(SO2) = 1,5a + 2b
→ n(hh khí) = 1,5a + 2b + b = 1,5a + 3b = 2,925
→ a = 1,75 và b = 0,1 → % = 0,1. 12. 100% : 99,2 = 1,21%
Đúng 0
Bình luận (0)
Hematit là quặng phổ biến nhất của sắt trong tự nhiên, được dùng để sản xuất gang. Từ 1 tấn quặng hematit (chứa 70% oxit sắt về khối lượng, còn lại là tạp chất trơ) có thể sản xuất được lượng gang thành phẩm (chứa 5% C về khối lượng) tối đa là A. 506,9 kg B. 515,8 kg C. 533,6 kg D. 490 kg
Đọc tiếp
Hematit là quặng phổ biến nhất của sắt trong tự nhiên, được dùng để sản xuất gang. Từ 1 tấn quặng hematit (chứa 70% oxit sắt về khối lượng, còn lại là tạp chất trơ) có thể sản xuất được lượng gang thành phẩm (chứa 5% C về khối lượng) tối đa là
A. 506,9 kg
B. 515,8 kg
C. 533,6 kg
D. 490 kg
Đáp án A
Gọi n(Fe) = a và n(Cu) = b → 56x + 64y = 15,2
BT e: 3x + 2y = 3n(NO) = 0,6
→ x = 0,1 và y = 0,15 → m(Cu) = 9,6 → % = 63,16%
Đúng 0
Bình luận (0)