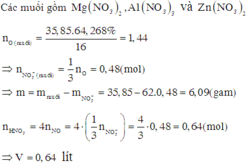cho 16,25g kim loại Zn tác dụng vừa đủ với 400ml đ HNO3 aM thu được 0,896 l khí N2 duy nhất . Tính a và khối lượng muốn tạo thành trong dd

Những câu hỏi liên quan
Cho 1,68 gam bột Mg tác dụng vừa đủ với 500ml dung dịch HNO3 aM thu được dung dịch Y và 0,448 lít khí NO duy nhất. Tính a và khối lượng muối tạo thành trong Y
Cho 7,75 gam hỗn hợp 2 kim loại Al và Cu tác dụng vừa đủ với 140 ml dd HNO3 đặc, nóng thu được 7,84 lít
(đktc)khí màu nâu (sp khử duy nhất).
a.Tính % khối lượng mỗi kim loại trong hỗn hợp ban đầu.
b.Tính CM của dd HNO3 cần dùng
\(\text{Đ}\text{ặt}:n_{Al}=a\left(mol\right);n_{Cu}=b\left(mol\right)\left(a,b>0\right)\\ Al+6HNO_3\rightarrow Al\left(NO_3\right)_3+3NO_2+3H_2O\\ Cu+4HNO_3\rightarrow Cu\left(NO_3\right)_2+2NO_2+2H_2O\\ \Rightarrow\left\{{}\begin{matrix}27a+64b=7,75\\3.22,4a+2.22,4b=7,84\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,05\\b=0,1\end{matrix}\right.\\ a,\Rightarrow\%m_{Al}=\dfrac{0,05.27}{7,75}.100\approx17,419\%\\ \Rightarrow\%m_{Cu}\approx82,581\%\\ b,n_{HNO_3}=6a+4b=0,7\left(mol\right)\\ C_{M\text{dd}HNO_3}=\dfrac{0,7}{0,14}=5\left(M\right)\)
Đúng 1
Bình luận (0)
Cho 2,46g hỗn hợp Al, Cu tác dụng vừa đủ với dung dịch HNO3 5% thu được 0,896 lit NO (đktc) (sản phẩm khử duy nhất) và dung dịch X
a) Tính khối lượng mỗi kim loại trong hỗn hợp đầu
b) Tính C% các muối trong dung dịch X.
a, \(\left\{{}\begin{matrix}27n_{Al}+64n_{Cu}=2,46\\3n_{Al}+2n_{Cu}=3n_{NO}=0,12\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Al}=0,02\left(mol\right)\\n_{Cu}=0,03\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}m_{Al}=0,54\left(g\right)\\n_{Cu}=1,92\left(g\right)\end{matrix}\right.\)
Đúng 1
Bình luận (0)
b, \(n_{HNO_3}=4n_{NO}=0,16\left(mol\right)\)
\(\Rightarrow m_{HNO_3}=10,08\left(g\right)\)
\(\Rightarrow m_{ddHNO_3}=201,6\left(g\right)\)
\(\Rightarrow m_{\text{dd sau pư}}=2,46+201,6-0,04.30=202,86\left(g\right)\)
\(\Rightarrow C\%\left(Al\left(NO_3\right)_3\right)=\dfrac{0,02.213}{202,86}.100\%=2,1\%\)
\(\Rightarrow C\%\left(Cu\left(NO_3\right)_2\right)=\dfrac{0,03.188}{202,86}.100\%=2,78\%\)
Đúng 1
Bình luận (0)
Cho 2,11 gam hỗn hợp Zn và Al tác dụng hết với dung dịch HNO3 đặc, nóng thu được 2,912 lít khí duy nhất NO2 (đktc). Tính thành phần phần trăm khối lượng mỗi kim loại trong hỗn hợp đầu.
$n_{NO_2} = 0,13(mol)$
$n_{Zn} = a(mol) ; n_{Al} = b(mol)$
Ta có :
$m_{hh} = 65a + 27b = 2,11(gam)$
Bảo toàn electron : $2a + 3b = 0,13$
Suy ra a = 0,02 ; b = 0,03
$\%m_{Zn} = \dfrac{0,02.65}{2,11}.100\% = 61,61\%$
$\%m_{Al} = 100\% -61,61\% = 38,39\%$
Đúng 1
Bình luận (0)
cho kim loại zinc ( zn ) tác dụng vừa đủ với dd h2so4 thu 19,832 lít h2 (đkc)
a tính khối lượng zn phản ứng
b khối lượng h2so4 cần dùng
c khối lượng muối tạo thành
( zn = 65 , cl= 35,5 , s=32 , h = 1 )
a)\(n_{H_2}=\dfrac{19,832}{24,79}=0,8\left(mol\right)\)
\(PTHH:Zn+H_2SO_4\xrightarrow[]{}ZnSO_4+H_2\)
tỉ lệ :1 1 1 1
số mol :0,8 0,8 0,8 0,8
\(m_{Zn}=0,8.65=52\left(g\right)\)
b)\(m_{H_2SO_4}=0.8.98=78,4\left(g\right)\)
c)\(m_{ZnSO_4}=0,8.161=128\left(g\right)\)
Đúng 2
Bình luận (0)
Cho m gam hỗn hợp các kim loại Mg, Al, Zn tác dụng vừa đủ với V lít dung dịch HNO3 1M, thu được sản phẩm khử là khí NO duy nhất và 35,85 gam muối trong đó oxi chiếm 64,268% khối lượng muối. Giá trị của m và V lần lượt là: A. 6,09 và 0,48 B. 5,61 và 0,48 C. 6,09 và 0,64 D. 25,93 và 0,64
Đọc tiếp
Cho m gam hỗn hợp các kim loại Mg, Al, Zn tác dụng vừa đủ với V lít dung dịch HNO3 1M, thu được sản phẩm khử là khí NO duy nhất và 35,85 gam muối trong đó oxi chiếm 64,268% khối lượng muối. Giá trị của m và V lần lượt là:
A. 6,09 và 0,48
B. 5,61 và 0,48
C. 6,09 và 0,64
D. 25,93 và 0,64
cho 3,51g hỗn hợp E gồm al và ag tác dụng hoàn toàn và vừa đủ với V ml dd hno3 loãng, thu được 448 ml lít(đktc) khí NO là sản phẩm khử duy nhất
a) Viết PTHH xảy ra
b) tính %khối lượng mỗi kim loại trong E và tính giá trị v
\(3Ag+4HNO_3\rightarrow3AgNO_3+NO+2H_2O\)
\(Al+4HNO_3\rightarrow Al\left(NO_3\right)_3+NO+2H_2O\)
\(NO\) là sản phẩm khử duy nhất.
\(\Rightarrow n_{NO}=\dfrac{0,448}{22,4}=0,02mol\)
Ta có: \(\left\{{}\begin{matrix}27n_{Al}+108n_{Ag}=3,51g\\BTe:3n_{Al}+n_{Ag}=3n_{NO}=0,06\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Al}=0,01mol\\n_{Ag}=0,03mol\end{matrix}\right.\)
\(\%m_{Al}=\dfrac{0,01\cdot27}{3,51}\cdot100\%=7,7\%\)
\(\%m_{Ag}=100\%-7,7\%=92,3\%\)
Đúng 1
Bình luận (1)
a, \(Al+4HNO_3\rightarrow Al\left(NO_3\right)_3+NO+2H_2O\)
\(3Ag+4HNO_3\rightarrow3AgNO_3+NO+2H_2O\)
Đúng 0
Bình luận (0)
b, \(\left\{{}\begin{matrix}\underrightarrow{BTE}3n_{Al}+n_{Ag}=\dfrac{0,448.3}{22,4}=0,06\\\underrightarrow{BTKL}27n_{Al}+108n_{Ag}=3,51\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}n_{Al}=0,01\\n_{Ag}=0,03\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%Al=\dfrac{0,01.27}{3,51}.100\%=7,69\%\\\%Ag=\dfrac{0,03.108}{3,51}.100\%=92,31\%\end{matrix}\right.\)
Đúng 0
Bình luận (0)
Cho 11,9 gam hh Al,Zn tác dụng vừa đủ với 200ml dd HCl 4M thu đuọc dd X và V lít khí (đkc) a) Tính % khối lượng mỗi kim loại b) Tính V=? Tính CM các muối trong dd X
Gọi \(\left\{{}\begin{matrix}n_{Al}=x\left(mol\right)\\n_{Zn}=y\left(mol\right)\end{matrix}\right.\)
\(n_{HCl}=0,2\cdot4=0,8mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(x\) \(\rightarrow\) \(3x\) \(x\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(y\) \(\rightarrow\) \(2y\) \(y\)
\(\Rightarrow\left\{{}\begin{matrix}27x+65y=11,9\\3x+2y=0,8\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}x=0,2\\y=0,1\end{matrix}\right.\)
a)\(\%m_{Al}=\dfrac{0,2\cdot27}{11,9}\cdot100\%=45,38\%\)
\(\%m_{Zn}=100\%-45,38\%=54,62\%\)
b)\(\Sigma n_{H_2}=\dfrac{3}{2}x+y=\dfrac{3}{2}\cdot0,2+0,1=0,4mol\)
\(V_{H_2}=0,4\cdot22.4=8,96l\)
Đúng 2
Bình luận (0)
giúp em với cho 10,95 gam hỗn hợp gồm Al và Cu tác dụng vừa đủ V ml dung dịch HNO3 2M thu được 3,36 lít khí duy nhất không màu hóa nâu trong không khí (đktc) và dung dịch A a)tính % khối lượng từng kim loại trong hỗn hợp b)tính thể tích của dung dịch HNO3 đã dùng