5,4 nhôm phản ứng với dung dịch HCL dư thu được dung dịch A và V lít khí H2 (đktc)
A. Viết PTHH xảy ra
B. Tính V
C. Cho A phản ứng đủ với 200ml dung dịch NAOH thì thu được kết tủa. Tính khối lượng kết tủa và nồng độ OH mol NAOH
Cho 1,56 gam hỗn hợp gồm Al và A l 2 O 3 phản ứng hết với dung dịch HCl (dư), thu được V lít khí H 2 (đktc) và dung dịch X. Nhỏ từ từ dung dịch N H 3 đến dư vào dung dịch X thu được kết tủa, lọc hết lượng kết tủa, nung đến khối lượng không đổi thu được 2,04 gam chất rắn. Viết các PTHH xảy ra và tính giá trị của V
Cho 5,4 gam Nhôm phản ứng với dung dịch HCl dư thu được Nhôm Clorua
a,Viết PTHH xảy ra?
b,Tính khối lượng HCl đã phản ứng
c,tính thể tích khí Hidro thu đc ở đktc
\(n_{Al}=\dfrac{5.4}{27}=0.2\left(mol\right)\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(0.2........0.6.........................0.3\)
\(m_{HCl}=0.6\cdot36.5=21.9\left(g\right)\)
\(V_{H_2}=0.3\cdot22.4=6.72\left(l\right)\)
a) $2Al + 6HCl \to 2AlCl_3 + 3H_2$
b) n Al = 5,4/27 = 0,2(mol)
n HCl = 3n Al = 0,6(mol)
=> m HCl = 0,6.36,5 = 21,9 gam
c) n H2 = 3/2 n Al = 0,3(mol)
=> V H2 = 0,3.22,4 = 6,72 lít
Bài 8. a) Cho 200ml dung dịch HCl 2M tác dụng với lượng dư KMnO4 thu được dung dịch A, V1 lít khí Cl2 (đktc). b) Cho 200ml dung dịch HCl 2M tác dụng với lượng dư MnO2 thu được dung dịch B, V2 lít khí Cl2 (đktc). - Viết PTHH của phản ứng xảy ra. - Tính thể tích khí Cl2 thu được (V1, V2). Mọi người giúp mình với ạ mình thật sự rất cần
- PT: a, \(2KMnO_4+16HCl\rightarrow2KCl+2MnCl_2+5Cl_2+8H_2O\) (1)
\(MnO_2+4HCl_đ\underrightarrow{t^o}MnCl_2+Cl_2+2H_2O\) (2)
- Ta có: \(n_{HCl\left(1\right)}=n_{HCl\left(2\right)}=0,2.2=0,4\left(mol\right)\)
Theo PT (1): \(n_{Cl_2}=\dfrac{5}{16}n_{HCl\left(1\right)}=0,125\left(mol\right)\Rightarrow V_1=0,125.22,4=2,8\left(l\right)\)
(2): \(n_{Cl_2\left(2\right)}=\dfrac{1}{4}n_{HCl\left(2\right)}=0,1\left(mol\right)\Rightarrow V_2=0,1.22,4=2,24\left(l\right)\)
Cho 5g hỗn hợp X gồm Mg và Cu tác dụng với dung dịch HCl 14,6% (phản ứng vừa đủ), thu được dung dịch Y và 3,36 lít khí H2 (ở đktc)
a) Viết PTHH của phản ứng xảy ra
b) Tính % theo khối lượng của mỗi kim loại trong hhX?
c) Tính Khối lượng dung dịch HCl đã dùng
d) Tính nồng độ % của dung dịch Y
a. PTHH : Mg + 2HCl ➝ MgCl2 + H2 (1)
b. theo bài : nH2 = 3,36 : 22,4 = 0,15 (mol)
theo (1) nMg = nH2 = 0,15 (mol)
➞ mMg = 0,15 ✖ 24 = 3,6 (g)
➞ %mMg = (3,6 : 5)✖100 = 72%
➞ %mCu = 100% - 72% = 28%
c. theo (1) nHCl = 2nH2 = 2✖0,15 = 0,3 (mol)
mHCl = 0,3✖36,5 = 10,95(g)
➜mddHCl = (10,95✖100):14,6 = 75(g)
d. dung dịch Y : MgCl2
mdd(spư)= 3,6+75-0,3 = 78,3(g)
theo (1) nMgCl2 = nH2 = 0,15(mol)
mMgCl2 = 0,15✖95 = 14,25(g)
C%MgCl2 = (14,25 : 78,3)✖100 = 18,199%
Cho 5,4 g nhôm(Al)tác dụng với 18,25 g dung dịch axit clohiđric (HCL) thu được AlCl3 và khí H2 thoát ra. a)hãy viết phương trình phản ứng xảy ra b) tính thể tích khí H2 thu được ở (đktc) c)tính khối lượng AlCl3 thu được
\(n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\)
PTHH:
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
0,2 0,2 0,3
\(V_{H_2}=n.22,4=6,72\left(l\right)\)
\(m_{AlCl_3}=n.M=0,2.133,5=26,7\left(g\right)\)
a) \(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
b) \(n_{Al}=\dfrac{m}{M}=\dfrac{5,4}{27}=0,2\left(mol\right)\) ; \(n_{HCl}=\dfrac{m}{M}=\dfrac{18,25}{36,5}=0,5\left(mol\right)\)
\(2Al\) \(+\) \(6HCl\) → \(2AlCl_3\) \(+\) \(3H_2\)
Tỉ lệ: \(\dfrac{0,2}{2}>\dfrac{0,5}{6}\) ⇒ Al dư, tính theo HCl
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
\(0,5\) → \(\dfrac{1}{6}\) → \(0,25\) ( mol )
\(V_{H_2}=n.22,4=0,25.22,4=5,6\left(l\right)\)
c) \(m_{AlCl_3}=n.M=\dfrac{1}{6}.\left(27+35,5.3\right)=22,25\left(g\right)\)
Cho 150gam CaCO3 tác dụng vừa đủ với dung dịch HCl,sau phản ứng thu được 500ml dung dịch X và V lít khí CO2(đktc) a)Viết PTHH xảy ra và tính V b)Tính nồng độ mol của chất có trong dung dịch X
\(n_{CaCO_3}=\dfrac{150}{100}=1.5\left(mol\right)\)
\(CaCO_3+2HCl\rightarrow CaCl_2+CO_2+H_2O\)
\(n_{CaCl_2}=n_{CO_2}=n_{CaCO_3}=1.5\left(mol\right)\)
\(V_{CO_2}=1.5\cdot22.4=33.6\left(l\right)\)
\(C_{M_{CaCl_2}}=\dfrac{1.5}{0.5}=3\left(M\right)\)
nHCl = 0,2.2.5 =0,5 mol
Fe + 2HCl → FeCl2 + H2
x 2x x x (mol)
2Al + 6HCl → 2AlCl3 + 3H2
y 3y y 3/2y (mol)
Phản ứng vừa đủ nên ta có
Bảo toàn nguyên tố H ==> nH2 thu được = 0,25 mol ==> VH2 = 0,25.22,4 =5,6 lít
Gọi số mol Fe, Al lần lượt là x, y ta có hệ pt:\(\left\{{}\begin{matrix}56x+27y=8,3\\2x+3y=0,5\end{matrix}\right.\)
==> x = 0,1 và y = 0,1 mol
dd A gồm \(\left\{{}\begin{matrix}FeCl2\\AlCl3\end{matrix}\right.\) + 0,6 mol NaOH , NaOH dư nên kết tủa Al(OH)3 sinh ra bị hòa tan hết . Kết tủa Z thu được chỉ có Fe(OH)2 0,1 mol
Fe(OH)2 nung trong không khí ==> Fe2O3 0,05 mol
mChat rắn = mFe2O3= 0,05. 160= 8 gam
Tiến hành phản ứng nhiệt nhôm m gam hỗn hợp A gồm Al và một oxit sắt thu được hỗn hợp chất rắn B. Cho B tác dụng với dung dịch NaOH dư thu được dung dịch C, phần không tan D và 0,672 lít khí H2 (đktc). Cho từ từ dung dịch HCl vào dung dịch C đến khi thu được lượng kết tủa lớn nhất rồi lọc và nung kết tủa đến khối lượng không đổi được 5,1 gam chất rắn. Phần không tan D cho tác dụng hết với dung dịch H2SO4 đặc nóng. Sau phản ứng chỉ thu được dung dịch E chứa một muối sắt duy nhất và 2,688 lít khí SO2 duy nhất (đktc). (Biết các phản ứng xảy ra hoàn toàn; dung dịch E không hòa tan được bột Cu). Thành phần % khối lượng của oxit sắt trong hỗn hợp A là
A. 76,19%.
B. 70,33%.
C. 23,81%.
D. 29,67%.
Đáp án A
· Có n Al ( B ) = 2 3 . n H 2 = 2 3 . 0 , 672 22 , 4 = 0 , 02 mol
· Chất rắn thu được sau khi nung là Al2O3:
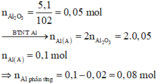
· Quy đổi A tương đương với hỗn hợp gồm 0,1 mol Al, a mol Fe, b mol O
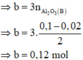
· Phần không tan D gồm Fe và oxit sắt + H2SO4 ® Dung dịch E + 0,12 mol SO2
Dung dịch E chứa một muối sắt duy nhất và không hòa tan được bột Cu
Þ Muối sắt là FeSO4.
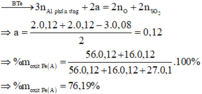
Tiến hành phản ứng nhiệt nhôm m gam hỗn hợp A gồm Al và một oxit sắt thu được hỗn hợp chất rắn B. Cho B tác dụng với dung dịch NaOH dư thu được dung dịch C, phần không tan D và 0,672 lít khí H2 (đktc). Cho từ từ dung dịch HCl vào dung dịch C đến khi thu được lượng kết tủa lớn nhất rồi lọc và nung kết tủa đến khối lượng không đổi được 5,1 gam chất rắn. Phần không tan D cho tác dụng với dung dịch H2SO4 đặc nóng. Sau phản ứng chỉ thu được dung dịch E chứa một muối sắt duy nhất và 2,688 lít khí SO2 duy nhất (đktc). (Biết các phản ứng xảy ra hoàn toàn). Trong hỗn hợp A, thành phần % khối lượng của Al gần nhất với giá trị nào sau đây?
A. 24%
B. 20%
C. 14%
D. 10%
Sau phản ứng có Al dư do phản ứng với NaOH tạo H2
=> nAl dư = 2/3 .nH2 = 0,02 mol
Sau phản ứng có Al và Al2O3 + NaOH => NaAlO2
Bảo toàn Al ta có :
2nAl2O3 sau nung= nAl dư + 2nAl2O3 => nAl2O3 = 0,04 mol
=>nAl ban đầu = 0,1 mol
Do các phản ứng hàn toàn , mà khi nhiệt nhôm Al dư => oxit sắt hết
=>D chỉ có Fe
=>Bảo toàn e : 3nFe = 2nSO2 => nFe = 0,08 mol
Bảo toàn khối lượng : mA = mB = mFe + mAl + mAl2O3 = 9,1g
=>%mAl(A) = 29,67% gần nhất với giá trị 24%
=>A