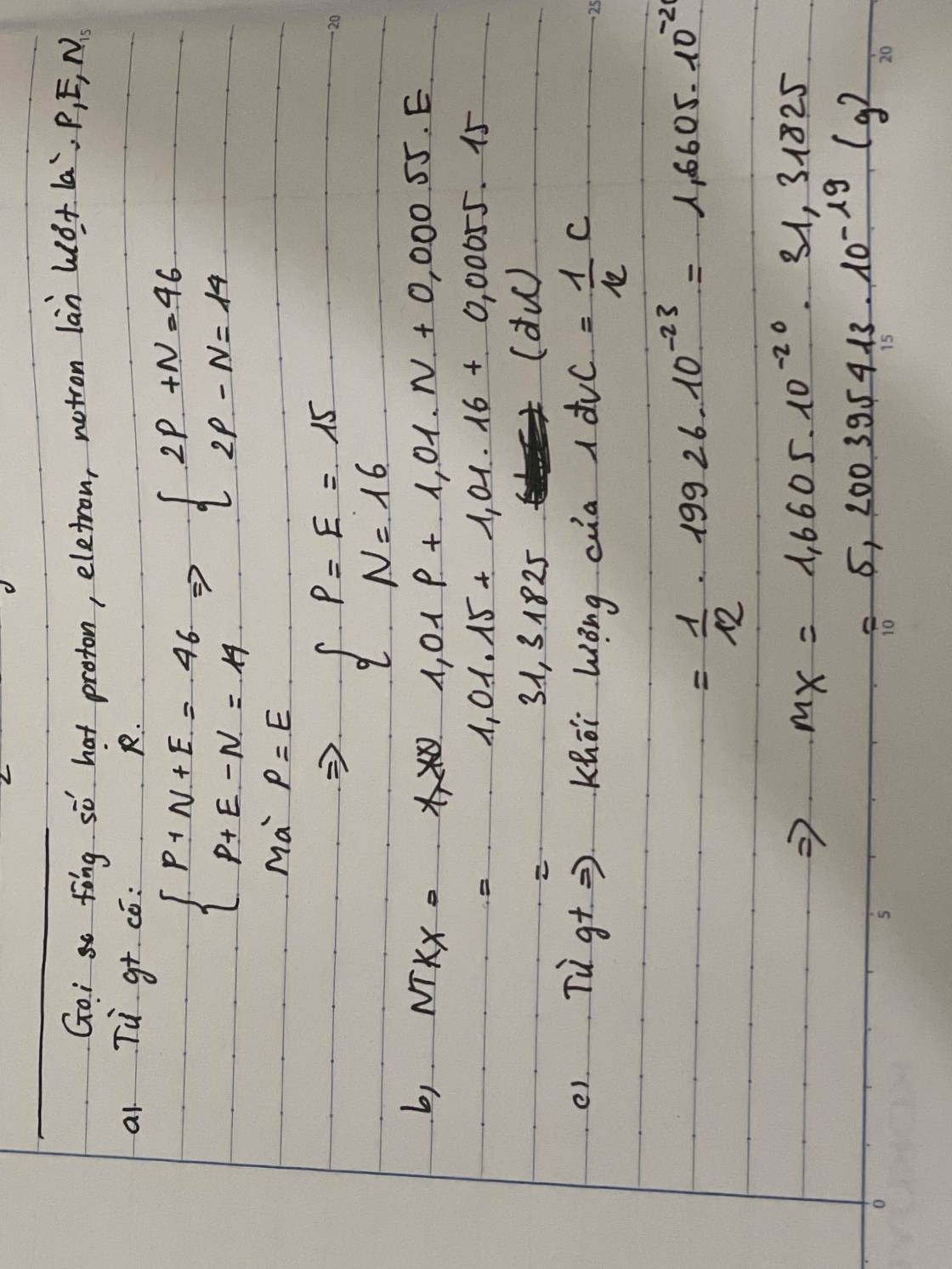nguyên tử Y có số hạt mang điện tích âm bằng 1/4 số hạt mang điện của X và có số notron bằng 0,4 lần số notron của X. Tính số khối của Y là

Những câu hỏi liên quan
nguyên tử Y có tổng số hạt là 36 số hạt không mang điện thì bằng một nửa hiệu số giữa tổng số hạt và số hạt mang điện tích âm hãy xác địch số khối số hiệu nguyên tử số đơn vị diện tích hạt nhân, điện tích hạt nhân số notron của từng nguyên tố
Ta có hệ :\(\left\{{}\begin{matrix}2Z+N=36\\N=\dfrac{36-Z}{2}\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}Z=12\left(Mg\right)\\N=12\end{matrix}\right.\)
=> A=Z+N=12+12=24
Số đơn vị điện tích hạt nhân Z = số proton = số electron=12
Điện tích hạt nhân :Z+ = 12+
Đúng 1
Bình luận (1)
\(\left\{{}\begin{matrix}N+P+E=36\\N=\dfrac{1}{2}.\left(P+E\right)\\P=E\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}2P+N=36\\N=P\\P=E\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}N=12\\P=12\\E=12\end{matrix}\right.\\\Leftrightarrow\left\{{}\begin{matrix}A=P+N=12+12=24\left(đ.v.C\right)\\Z^+=12\end{matrix}\right.\)
Đúng 0
Bình luận (0)
1/ Phân tử A có công thức XYZ (X, Y, Z là ba nguyên tố khác nhau). Tổng số ba loại hạt proton, notron, electron trong một phân tử A là 141. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 35; hiệu nguyên tử khối giữa Y và Z gấp 64 lần nguyên tử khối của X; tổng số nguyên tử khối của Y và Z gấp 96 lần nguyên tử khối của X; trong nguyên tử Z có số hạt không mang điện bằng một nửa số hạt mang điện. Tìm công thức của chất A Xem nội dung đầy đủ tại:
Đọc tiếp
1/ Phân tử A có công thức XYZ (X, Y, Z là ba nguyên tố khác nhau). Tổng số ba loại hạt proton, notron, electron trong một phân tử A là 141. Trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 35; hiệu nguyên tử khối giữa Y và Z gấp 64 lần nguyên tử khối của X; tổng số nguyên tử khối của Y và Z gấp 96 lần nguyên tử khối của X; trong nguyên tử Z có số hạt không mang điện bằng một nửa số hạt mang điện. Tìm công thức của chất A Xem nội dung đầy đủ tại:
Tìm số proton,notron, electron và số khối của các nguyên tử sau : a) X có tổng số hạt là 18, số p= số n b)Y có số khối là 27 và số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt c)Z có số khối là 35, số proton kém số notron 1 hạt
Tìm số proton,notron, electron và số khối của các nguyên tử sau :
a) X có tổng số hạt là 18, số p= số n
\(\left\{{}\begin{matrix}2Z+N=18\\Z=N\end{matrix}\right.\)
=> Z=P=E=6
N=6
b)Y có số khối là 27 và số hạt mang điện nhiều hơn số hạt không mang điện là 12 hạt
\(\left\{{}\begin{matrix}Z+N=A=27\\2Z-N=12\end{matrix}\right.\)
=> Z=P=E= 13
N=14
c)Z có số khối là 35, số proton kém số notron 1 hạt
\(\left\{{}\begin{matrix}Z+N=A=35\\N-Z=1\end{matrix}\right.\)
=> Z=P=E= 17
N=18
Đúng 3
Bình luận (0)
a) S=P+E+N
P=E=N
=>P=E=N=18/3=6
=> A= P+N=6+6=12
=> Nguyên tử X có 6p,6e,6n. Số khối 12.
b) Nguyên tử Y:
A=P+N=27
Mặt khác:2P-N=12
=> Ta tìm được: P=E=13; N=14
=> Nguyên tử Y có 13p,13e,14n và số khối là 27.
c) Nguyên tử Z:
A=P+N=35
N=P+1
Ta tìm được: P=E=17; N=18
=> Nguyên tử Z có 17p,17e,18n và số khối là 35
Đúng 2
Bình luận (0)
Một nguyên tử X có tổng số hạt electron , proton , notron là 46 . Số hạt mang điện nhiều hơn số hạt ko mang điện 14 hạt .a) Tính số hạt proton, electron, notron.b) Tính nguyên tử khối của X, biết khối lượng proton khối lượng notron 1,01đvC.c) Tính khối lượng bằng gam của X, biết khôi lượng của nguyên tử C là 1,9926.10^{-23} gam.
Đọc tiếp
Một nguyên tử X có tổng số hạt electron , proton , notron là 46 . Số hạt mang điện nhiều hơn số hạt ko mang điện 14 hạt .
a) Tính số hạt proton, electron, notron.
b) Tính nguyên tử khối của X, biết khối lượng proton = khối lượng notron = 1,01đvC.
c) Tính khối lượng bằng gam của X, biết khôi lượng của nguyên tử C là 1,9926.10\(^{-23}\) gam.
Hợp chất A có công thức là XY2 ; trong đó tổng số hạt proton, notron, electron là 66; .Hạt mang điện của X,Y hơn kém nhau 20 hạt. Trong hạt nhân của nguyên tử X và Y đều có số hạt mang điện bằng số hạt không mang điện. Tìm công thức hóa học của A.
Gọi m,n,p,q lần lượt số p và số n của X,Y (m,n,p,q:nguyên, dương)
=> 2m+n+4p+2q= 66 (1)
Mặt khác, số hạt mang điện X,Y hơn kém nhau 20 hạt:
=> 2m - 2p = 20 (2)
Tiếp theo, hạt nhân X,Y có số hạt không mang điện bằng số hạt mang điện:
=> m=n (3); p=q(4)
Từ (1), (2), (3), (4) ta lập hệ pt 4 ẩn giải ra được:
=> m=14; n=14; p=4;q=4
=> ZX=14 => X là Silic
=> ZY= 4 => Y là Beri
=> A: SiBe2 (thường viết là Be2Si nhiều hơn)
Đúng 1
Bình luận (0)
Nguyên tử của nguyên tố X có tổng số hạt là 188 hạt . Biết rằng số hạt mang điện tích âm ít hơn số hạt không mang điện là 23 hạt . Xác định số hạt proton, notron, electron của nguyên tử nguyên tố X
N+P+E=188=>N+2Z=188
N-E=23=>N-Z=23
N=78,Z=P=N=55
Đúng 1
Bình luận (0)
ta có : e + p + n = 188
mà : p = e ; n = e + 23
thay vào ta đc : e + e + e + 23 = 188
=> 3e + 23 = 188
=> 3e = 165
=> e = 55
=> p = e = 55
=> n = e + 23 = 55 + 23 = 78
Đúng 1
Bình luận (0)
Nguyên tử nguyên tố x có tổng số hạt proton notron electron là 34 hạt trong đó số hạt mang điện nhiều hơn số hạt không mang điện là 10 hạt
a, xác định nguyên tố x
b, tính khối lượng bằng gam của một nguyên tử x biết khối lượng của một nguyên tử C là 1,9926×10^_23 gam và nguyên tử khối của Cacbon bằng 12 dvc
Xem chi tiết
a, Gọi số proton, electron và notron của X lần lượt là p;e;n
Theo gt ta có:
\(\left\{{}\begin{matrix}2p+n=34\\2p-n=10\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}p=11\\n=12\end{matrix}\right.\)
Vậy X là Na
b, Ta có: $m_{Na}=23.1,9926.10^{-23}:12=3,819.10^{-23}$
Đúng 1
Bình luận (0)
Nguyên tử X có số hạt p, n, e là 34 → p + n + e = 34 → 2p + n = 34 (1)
Trong đó, số hạt mang điện nhiều hơn số hạt không mang điện là 10 → p + e – n = 10 → 2p – n = 10 (2)
Từ (1) và (2) → p = 11, n = 12
Số khối A = p + n = 11 + 12 = 23
Đúng 0
Bình luận (0)
Nguyên tử X có tổng hạt proton, notron và electron là 52. Trong đó số hạt mang điện âm ít hơn số hạt ko mang điện là 1.
a. Tính số hạt proton, notron và electron của nguyên tử X?
b. Cho biết X là nguyên tố nào ?
Mn gửi cả lời giải giúp mình với .... Thanks tr
a,Trong nguyên tử, số proton mang điện tích dương = số electron mang điện tích âm, hạt notron ko mang điện tích
Gọi x là số hạt elentron , y là số hạt notron, ta có
\(_{\begin{cases}2x+y=52\\y-x=1\end{cases}\Leftrightarrow}^{ }_{ }\begin{cases}x=17\\y=18\end{cases}}\)
số e = số p = 17
số n= 18
b, số e=17 => nguyên tố Clo ( bảng tuần hoàn )
Đúng 0
Bình luận (0)
Phân tử XY3 có tổng số proton, notron, electron bằng 196 trong đó số hạt mang điện nhiều hơn số hạt không mạng điện 60, số hạt mạng điện của X ít hơn số hạt mang điện của Y là 76. Xác định X, Y và XY3.