Mn giúp mình với :
1/Một lọ đựng 50ml bạc nitrat được cho vào một miếng đồng. Sau phản ứng đem miếng đồng đi cân thấy khối lượng tăng thêm 3,12 gam. Hãy xác định nồng độ mol dung dịch bạc nitrat
2/Hòa tan 13,2g hỗn hợp X gồm hai kim loại có cùng hóa trị vào 200ml dung dịch HCl 3M. Cô cạn dung dịch sau phản ứng thu được 22,06g hỗn hợp muối khan.
a/ Hỏi hai kim loại có tan hết không ? b/ Tính thể tích hidro sinh ra.
3/Hỗn hợp X gồm 2 kim loại Mg và Zn. Y là dung dịch H2SO4 có nồng độ x mol/l. Trường hợp 1: cho 24,3g (X) vào 2 lít (Y) sinh ra 8,96 lít khí H2. Trường hợp 2: cho 24,3g (X) vào 3 lít (Y) sinh ra 11,2 lít khí H 2. Hãy chứng minh trong trường hợp 1 thì hỗn hợp kim loại chưa tan hết, trong trường hợp 2 axit còn dư. Tính nồng độ x mol/l của dung dịch (Y) và % khối lượng mỗi kim loại trong X (cho biết khí H2 sinh ra ở đktc)
4/Thí nghiệm 1: cho a gam Fe hòa tan trong dung dịch HCl, sau khi cô cạn dung dịch thu được 3,1 gam chất rắn. Thí nghiệm 2: cho a gam Fe và b gam Mg vào dung dịch HCl (cùng với lượng như trên) sau khi cô cạn dung dịch thì thu được 3,34g chất rắn và 448ml H2. Tính a, b và khối lượng của các muối.
5/Một hỗn hợp 4,15g chứa Fe và Al tác dụng với 200ml dung dịch CuSO4 0,525M. Khuấy kỹ để phản ứng xảy ra hoàn toàn. Thu được kết tủa gồm hai kim loại có khối lượng 7,48g. Tìm số mol các kim loại trong hỗn hợp ban đầu và trong kết tủa.

Những câu hỏi liên quan
Bài 5. Một lọ đựng 50ml bạc nitrat được cho vào một miếng đồng. Sau phản ứng đem miếng đồng đi cân thấy khối lượng tăng thêm 3,04 gam. Hãy xác định nồng độ mol dung dịch bạc nitrat.
Bài 5 :
Pt : \(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag|\)
1 2 1 2
x 0,04 2x
Gọi x là số mol của Cu
Vì khối lượng đồng tăng so với ban đầu nên ta có phương trình :
\(m_{Ag}-m_{Cu}=3,04\left(g\right)\)
216x - 64x = 3,04
152x = 3,04
⇒ x = \(\dfrac{3,04}{152}=0,02\left(mol\right)\)
\(n_{AgNO3}=\dfrac{0,02.2}{1}=0,04\left(mol\right)\)
50ml = 0,05l
\(C_{M_{ddAgNO3}}=\dfrac{0,04}{0,05}=0,8\left(M\right)\)
Chúc bạn học tốt
Đúng 2
Bình luận (0)
Cu + 2AgNO3 → Cu(NO3)2 + 2Ag↓
1.…… 2 mol………………………2 mol
64g………………………………….216g
Áp dụng phương pháp tăng giảm khối lượng
- Số mol AgNO3 tham gia phản ứng:
nAgNO3 = 3,04/(216-64).2=0,04 mol
- Nồng độ mol dung dịch bạc nitrat: 0,04/0,05 = 0,8M
Đúng 3
Bình luận (3)
Ngâm một lá đồng trong 20ml dung dịch bạc nitrat cho đến khi đồng không thể tan thêm được nữa. Lấy lá đồng ra, rửa nhẹ, làm khô và cân thì khối lượng lá đồng tăng thêm 1,52g. Hãy xác định nồng độ mol của dung dịch bạc nitrat đã dùng (giả thiết toàn bộ bạc giải phóng ra bám hết vào lá đồng). A. 0,75 M B. 0,5 M C. 1 M D. 0,25 M
Đọc tiếp
Ngâm một lá đồng trong 20ml dung dịch bạc nitrat cho đến khi đồng không thể tan thêm được nữa. Lấy lá đồng ra, rửa nhẹ, làm khô và cân thì khối lượng lá đồng tăng thêm 1,52g. Hãy xác định nồng độ mol của dung dịch bạc nitrat đã dùng (giả thiết toàn bộ bạc giải phóng ra bám hết vào lá đồng).
A. 0,75 M
B. 0,5 M
C. 1 M
D. 0,25 M
Cu → 2Ag
1 2 → mtang = 2.108-64 = 152g
x 2x → mtang = =1,52g
⇒ x = 1,52/152 = 0,01 mol
⇒ n A g N O 3 = n A g = 2x = 0,02 mol
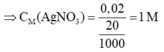
⇒ Chọn C.
Đúng 0
Bình luận (0)
Bài 1: ngâm một lá đồng 500ml dd AgNO3 đến khi phản ứng hoàn toàn. lấy lá đồng ra làm khô, cân thì thấy khối lượng lá đồng tăng thêm 15,2g. Hãy xác định nồng độ mol của dd bạc nitrat...Bài 2: cho 78g một kim loại A tác dụng với khí clo dư tạo thành 149g muối . Hãy xác định kim loại A có hóa trị 1. Bài 3: viết các pthh a, điều chế Zn từ ZnSO4 b, điều chế MgSO4 từ mỗi chất sau : Mg, MgCl2, MgO, MgCO3các chất cần thiết coi như đủ
Đọc tiếp
Bài 1: ngâm một lá đồng 500ml dd AgNO3 đến khi phản ứng hoàn toàn. lấy lá đồng ra làm khô, cân thì thấy khối lượng lá đồng tăng thêm 15,2g. Hãy xác định nồng độ mol của dd bạc nitrat...
Bài 2: cho 78g một kim loại A tác dụng với khí clo dư tạo thành 149g muối . Hãy xác định kim loại A có hóa trị 1.
Bài 3: viết các pthh
a, điều chế Zn từ ZnSO4
b, điều chế MgSO4 từ mỗi chất sau : Mg, MgCl2, MgO, MgCO3
các chất cần thiết coi như đủ
Bài 1:
\(PTHH:Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\\ \Rightarrow n_{Ag}=2n_{Cu}\\ m_{tăng}=m_{Ag}-m_{Cu}=15,2\left(g\right)\\ \Rightarrow108n_{Ag}-64n_{Cu}=15,2\\ \Rightarrow216n_{Cu}-64n_{Cu}=15,2\\ \Rightarrow n_{Cu}=0,1\left(mol\right)\\ \Rightarrow n_{AgNO_3}=0,2\left(mol\right)\\ \Rightarrow C_{M_{AgNO_3}}=\dfrac{0,2}{0,5}=0,4M\)
Bài 2:
\(n_A=\dfrac{78}{M_A}\left(mol\right);n_{ACl}=\dfrac{149}{M_A+35,5}\left(mol\right)\\ PTHH:2A+Cl_2\rightarrow2ACl\\ \Rightarrow n_A=n_{ACl}\Rightarrow\dfrac{78}{M_A}=\dfrac{149}{M_A+35,5}\\ \Rightarrow78M_A+2769=149M_A\\ \Rightarrow71M_A=2769\\ \Rightarrow M_A=39\\ \Rightarrow A\text{ là kali }\left(K\right)\)
Bài 3:
\(a,2Al+3ZnSO_4\rightarrow Al_2\left(SO_4\right)_3+3Zn\\ b,Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ MgO+H_2SO_4\rightarrow MgSO_4+H_2O\\ MgCO_3+H_2SO_4\rightarrow MgSO_4+H_2O+CO_2\uparrow\)
Đúng 2
Bình luận (1)
Ngâm một lá đồng trong 20 ml dung dịch bạc nitrat cho tới khi đồng không thể tan thêm được nửa. Lấy lá đồng ra, rửa nhẹ, làm khô và cân thì thấy khối lượng lá đồng tăng thêm 1,52 gam. Hãy xác định nồng độ mol của dung dịch bạc nitrat đã dùng (giả thiết toàn bộ lượng bạc giải phóng bám hết vào lá đồng)
Đọc tiếp
Ngâm một lá đồng trong 20 ml dung dịch bạc nitrat cho tới khi đồng không thể tan thêm được nửa. Lấy lá đồng ra, rửa nhẹ, làm khô và cân thì thấy khối lượng lá đồng tăng thêm 1,52 gam. Hãy xác định nồng độ mol của dung dịch bạc nitrat đã dùng (giả thiết toàn bộ lượng bạc giải phóng bám hết vào lá đồng)
Một hợp chất khí, phân tử có 85,7% C về khối lượng, còn lại là H. Phân tử khối của hợp chất là 28. Tìm số nguyên tử của mỗi nguyên tố trong 1 phân tử hợp chất.
Cho một lá đồng có khối lượng là 6 gam vào dung dịch bạc nitrat. Phản ứng xong, đem lá kim loại ra rửa nhẹ, làm khô cân được 13,6 gam. Tính khối lượng đồng đã phản ứng
Khối lượng kim loại tăng : 13,6 - 6 = 7,6 (gam)
Gọi n Cu = x mol
n Ag = 2x mol
Có: 2x x 108 - 64x = 7,6
=> x = 0,05 → m Cu = 0,05 x 64 = 3,2g
Đúng 1
Bình luận (0)
Ngâm một lá đồng trong 20 ml dung dịch bạc nitrat cho tới khi đồng không thể tan thêm được nữa. Lấy lá đồng ra, rửa nhẹ, làm khô và cân thì thấy khối lượng lá đồng tăng thêm 1,52 g. Hãy xác định nổng độ mol của dung dịch bạc nitrat đã dùng (giả thiết toàn bộ lượng bạc giải phóng bám hết vào lá đồng).
PTHH: Cu + 2AgNO3 → Cu(NO3)2 + 2Ag ↓
Theo PTHH: 1 mol Cu tác dụng với 2 mol AgNO3 thì khối lượng tăng 152g.
x mol Cu tác dụng với y mol AgNO3 tăng 1,52g.
=> x = 0,02 mol AgNO3.
Nồng độ dung dịch AgNO3: CMAgNO3 = n/V = 0,02/0,02 = 1(M).
Đúng 1
Bình luận (2)
Giải cách này nhé:
Cu+2AgNO3\(\rightarrow\)Cu(NO3)2+2Ag
- Gọi số mol Cu phản ứng là x\(\rightarrow\)số mol Ag tạo thành là 2x
- Độ tăng khối lượng lá Cu=khối lượng Ag sinh ra bám vào Cu- khối lượng Cu bị mất đi do phản ứng. Tức là:
108.2x-64x=1,52\(\rightarrow\)152x=1,52\(\rightarrow\)x=0,01mol
Số mol AgNO3=2x=0,02mol
\(C_{M_{AgNO_3}}=\dfrac{n}{v}=\dfrac{0,02}{0,02}=1M\)
Đúng 4
Bình luận (0)
Nhúng 1 thanh kim loại đồng nặng 2g vào 196g dung dịch Bạc nitrat một lúc sau lấy thanh kim lọa ra rửa sạch đặt lên cân thấy thanh kim loại nặng 3.52 g . Tính khối lượng đồng phản unges với Khối lượng bạc sinh ra. Tính nồng độ % của dung dịch muối thu được
Đặt \(n_{Cu}=a\left(mol\right)\)
\(PTHH:Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\)
\(\left(mol\right)\) \(a\) \(2a\) \(a\) \(2a\)
Theo đề bài ta có:
\(\Delta m\uparrow=108.2a-64a=3,52-2\Leftrightarrow a=0,01\left(mol\right)\)
\(m_{Cu}=0,01.64=0,64\left(g\right)\)
\(m_{Ag}=108.0,02=2,16\left(g\right)\)
\(C\%_{ddCu\left(NO_3\right)_2}=\dfrac{188.0,01}{2+196-3,52}.100\%=0,967\left(\%\right)\)
Đúng 1
Bình luận (0)
Cho 4,32g hỗn hợp hai kim loại sắt và đồng tác dụng vừa đủ với 50ml dung dịch AgNO3 dư. Sau phản ứng thu được 15,12g bạc a/ Viết PTHH b/ Tính khối lượng của mỗi kim loại trong hỗn hợp ban đầu c/ Tính nồng độ mol dung dịch bạc nitrat đã dùng
a)
$Fe + 2AgNO_3 \to Fe(NO_3)_2 + 2Ag$
$Cu + 2AgNO_3 \to Cu(NO_3)_2 + 2Ag$
b) Gọi $n_{Fe} =a (mol) ; n_{Cu} = b(mol) \Rightarrow 56a + 64b = 4,32(1)$
Theo PTHH :
$n_{Ag} = 2a + 2b = \dfrac{15,12}{108} = 0,14(2)$
Từ (1)(2) suy ra : a = 0,02 ; b = 0,05
$m_{Fe} = 0,02.56 = 1,12(gam)$
$m_{Cu} = 0,05.64 =3,2(gam)$
c) $n_{AgNO_3} = n_{Ag} = 0,14(mol)$
$C_{M_{AgNO_3}} = \dfrac{0,14}{0,05} = 2,8M$
Đúng 1
Bình luận (0)
Cho một lá đồng có khối lượng là 6 gam vào dung dịch bạc nitrat. Phản ứng xong, đem lá kim loại ra rửa nhẹ, làm khô cân được 13,6 gam. Viết phương trình hoá học.























