Tính pH của dung dịch sau:
a, 1 lít dung dịch hỗn hợp NaOH 0,005M; KOH 0,005M và Ba(OH)2 0,005M

Những câu hỏi liên quan
2/ Tính pH của các dung dịch sau: a) Dung dịch NaOH 0,01M b) Dung dịch Ba(OH)2 0,005M
a.
\(pH=14+log\left[OH^-\right]=14+log\left(0.01\right)=12\)
b.
\(pH=14+log\left[OH^-\right]=14+log\left(0.005\cdot2\right)=12\)
Đúng 2
Bình luận (0)
Trộn 250ml dung dịch hỗn hợp gồm H2SO4 0,005M và HCl 0,01M với 200ml dung dịch hỗn hợp gồm NaOH 0,001M và Ba(OH)2 0,0005M thu được dung dịch X. Dung dịch X có pH là:
A. 12,3
B. 1,18
C. 11,87
D. 2,13
Đáp án D
nH2SO4 = 0,005 .0,25 =0,00125(mol)
nHCl = 0,01. 0,25= 0,0025 (mol)
∑n= 0,00125 + 0,0025= 0,00375 (mol)
∑n= 0,001.0,2 + 0,0005.2.0,2=0,0004
H+ + OH- → H2O
Ban đầu: 0,00375 0,0004
Phản ứng: 0,0004 0,0004
Sau phản ứng: 0,00335 0
Vsau = 0,2 + 0,25= 0,45(lít)
Mà 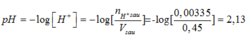
Đúng 0
Bình luận (0)
1. Trộn 100ml dung dịch hỗn hợp gồm H2SO4 0,05M và HCl 0,1M với V lít dung dịch hỗn hợp gồm NaOH 0,2M và Ba(OH)2 0,1M
a) viết pthh
b) tính giá trị của V
2. Hỗn hợp A gồm MgO và CuO. Hòa tan 11g hh A = dung dịch H2SO4 20% vừa đủ được dung dịch B chứa MgSO4, CuSO4 với nồng độ phần trăm của MgSO4 là 10,91%. Tính nồng độ % CuSO4 trong dung dịch B.
Tính PH của dung dịch chứa hỗn hợp axit hoặc bazơ mạnh a.Tính PH của dung dịch chứa hỗn hợp HCL 0,003M và H2SO4 0,002M b.Tính PH của dung dịch chứa hỗn hợp NaOH 0,0001 và Ba(OH)2 0,0001M
a, Ta có: \(\left[H^+\right]=\left[HCl\right]+2\left[H_2SO_4\right]=0,003+2.0,002=0,007\left(M\right)\)
\(\Rightarrow pH=-log\left(0,007\right)\approx2,155\)
b, Ta có: \(\left[OH^-\right]=\left[NaOH\right]+2\left[Ba\left(OH\right)_2\right]=0,0001+2.0,0001=0,0003\left(M\right)\)
\(\Rightarrow pH=14-\left[-log\left(0,0003\right)\right]\approx10,477\)
Đúng 2
Bình luận (0)
Có V lít dung dịch NaOH 0,5M. Trường hợp nào sau đây làm pH của dung dịch NaOH tăng? A. Thêm V lít nước cất B. Thêm V lít dung dịch HCl 0,4M C. Thêm V lít dung dịch KOH 0,4M D. Thêm V lít dung dịch Ba(OH)2 0,3M
Đọc tiếp
Có V lít dung dịch NaOH 0,5M. Trường hợp nào sau đây làm pH của dung dịch NaOH tăng?
A. Thêm V lít nước cất
B. Thêm V lít dung dịch HCl 0,4M
C. Thêm V lít dung dịch KOH 0,4M
D. Thêm V lít dung dịch Ba(OH)2 0,3M
Đáp án D
CM OH-=( V.0,5+ 2.0,3.V)/ 2V= 0,55 M nên pH tăng
Đúng 0
Bình luận (0)
Dung dịch A chứa hỗn hợp KOH 0,02M và Ba(OH)2 0,005M; dung dịch B chứa hỗn hợp HCl 0,05M và H2SO4 0,05M.
a.Tính thể tích dung dịch B cần để trung hòa 1 lít dung dịch A?
b.Tính nồng độ mol của các muối trong dung dịch thu được sau phản ứng, cho rằng thể tích dung dịch không thay đổi.
Rót từ từ 10ml dung dịch H2SO4 0,01M vào 20ml dung dịch 0,005M. Tính pH của dung dịch a) viết phương trình hóa học của phản ứng đã xảy ra trong thí nghiệm trê b) tính nồng độ mol của các chất sau phản ứng c) Tính pH của dung dịch d) Nhúng quỳ tím vào lọ hóa chất sau phản ứng có hiện tượng gì xảy ra
Hỗn hợp dung dịch X gồm NaOH 0.1M và KOH 0.1M. Trộn 100 ml dung dịch X với 100 ml dung dịch
H2SO4 0.2M thu được dung dịch A.
a. Tính nồng độ các ion trong dung dịch A.
b. Tính pH của dung dịch A.
Hỗn hợp dung dịch X gồm NaOH 0.1M và KOH 0.1M. Trộn 100 ml dung dịch X với 100 ml dung dịch
H2SO4 0.2M thu được dung dịch A.
a. Tính nồng độ các ion trong dung dịch A.
b. Tính pH của dung dịch A.
a, \(\left[Na^+\right]=0,1\)
\(\left[K^+\right]=0,1\)
\(\left[OH^-\right]=0,2\)
\(\left[SO_4^{2-}\right]=0,2\)
\(\left[H^+\right]=0,4\)
b, \(n_{H^+}=0,1.0,4=0,04\left(mol\right)\)
\(n_{OH^-}=0,1.0,2=0,02\left(mol\right)\)
\(H^++OH^-\rightarrow H_2O\)
\(\Rightarrow n_{H^+dư}=0,02\left(mol\right)\)
\(\Rightarrow\left[H^+\right]=\dfrac{0,02}{200}=10^{-4}\)
\(\Rightarrow pH=4\)
Đúng 0
Bình luận (0)
















