Cho 12 g một oxit của kim loại hóa trị không đổi tác dụng với dung dịch 18.25g HCl . Sau phản ứng lượng HCl còn dư tác dụng vừa hết với 9.4 g Kalioxit .Công thức của oxit ban đầu'
Cho 6,2 gam oxit của kim loại hóa trị I tác dụng với nước dư thu được dung dịch A có tính kiềm. Chia A thành 2 phần bằng nhau:
Phần 1 tác dụng với 95ml dung dịch HCl 1M thấy dung dịch sau phản ứng làm xanh quỳ tím.
Phần 2 tác dụng với 55ml dung dịch HCl 2M thấy dung dịch sau phản ứng làm đỏ quỳ tím.
Công thức oxit kim loại đã dùng là:
A.Li2O.
B. Na2O.
C.K2O.
D.Rb2O.
Gọi n M 2 O = a thì nMOH = 2a, mỗi phần có nMOH = a
Khi nHCl = 0,095 thì dung dịch sau phản ứng làm quỳ tím hóa xanh nên MOH dư => a > 0,095
Khi nHCl = 0,11 thì dung dịch sau phản ứng làm quỳ tím hóa đỏ nên HCl dư => a < 0,11
Có 0,095 < a < 0,11
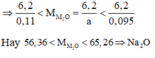
Đáp án B
cho 5,1g oxit kim loại hóa trị (III) tác dụng vừa đủ với 100ml dung dịch HCl 3M
tìm khối lượng dung dịch H2SO4 25% cần phản ứng hết với lượng oxit trên
Ta có: \(n_{HCl}=\dfrac{100}{1000}.3=0,3\left(mol\right)\)
\(PTHH:\)
\(A_2O_3+6HCl--->2ACl_3+3H_2O\left(1\right)\)
Theo PT(1): \(n_{A_2O_3}=\dfrac{1}{6}.n_{HCl}=\dfrac{1}{6}.0,3=0,05\left(mol\right)\)
\(\Rightarrow M_{A_2O_3}=\dfrac{5,1}{0,05}=102\left(\dfrac{g}{mol}\right)\)
Mà: \(M_{A_2O_3}=2A+16.3=102\left(\dfrac{g}{mol}\right)\)
\(\Leftrightarrow A=27\left(\dfrac{g}{mol}\right)\)
Vậy A là nhôm (Al)
\(PTHH:Al_2O_3+3H_2SO_4--->Al_2\left(SO_4\right)_3+3H_2O\left(2\right)\)
Theo PT(2): \(n_{H_2SO_4}=3.n_{Al_2O_3}=3.0,05=0,15\left(mol\right)\)
Mà: \(C_{\%_{H_2SO_4}}=\dfrac{0,15.98}{m_{dd_{H_2SO_4}}}.100\%=25\%\)
\(\Leftrightarrow m_{dd_{H_2SO_4}}=58,8\left(g\right)\)
Gọi công thức của oxit là A2O3
Ta có A2O3 + 6HCl → 2ACl3 + 3H2O
Từ pthh ta có nA2O3 = 1/6 nHCl = 1/6 . 0,3 = 0,05 mol
=> MA2O3 = mA2O3 : nA2O3 = 5,1 : 0,05 = 102
MA2O3 = 2 . MA + 3 . 16 = 2MA + 48 = 102
=> MA = 27 => A là nhôm
=>Al2O3+3H2SO4->Al2(SO4)3+3H2O
0,05-----0,15 mol
=>m dd H2SO4=58,8g
Gọi công thức của oxit là A2O3
Ta có A2O3 + 6HCl → 2ACl3 + 3H2O
Từ pthh ta có nA2O3 = 1/6 nHCl = 1/6 . 0,3 = 0,05 mol
=> MA2O3 = mA2O3 : nA2O3 = 5,1 : 0,05 = 102
MA2O3 = 2 . MA + 3 . 16 = 2MA + 48 = 102
=> MA = 27 => A là nhôm
=>Al2O3+3H2SO4->Al2(SO4)3+3H2O
0,05-----0,15 mol
=>m dd H2SO4=58,8g
cho 10,4 gam oxit của một nguyên tố kim loại không rõ hóa trị tác dụng với dung dịch HCl dư sau phản ứng tạo thành 15,9 gam muối. xác định nguyên tố kim loại
Gọi CTHH của oxit là $R_2O_n$
$R_2O_n + 2nHCl \to 2RCl_n + nH_2O$
Theo PTHH :
$n_{RCl_n} = 2n_{R_2O_n} \Rightarrow \dfrac{15,9}{R + 35,5n} = 2.\dfrac{10,4}{2R + 16n}$
$\Rightarrow R = 44n$
1) Cho 26,82g Al và Al2O3 tác dụng với dung dịch HCl 2M (D = 1,12 g/ml) vừa đủ. Sau phản ứng thu được 6,72 lít H2 (đkc)
a)Tìm % khối lượng mỗi chất
b) Tính nồng độ C% của dung dịch sau phản ứng
2)Hỗn hợp 31,2g một kim loại hóa trị II và oxit của nó hòa an vừa đủ trong 250ml dung dịch HCl 4M. Người ta thu được 6,72 lít khí
a) Xác định tên kim loại
b)Tính % khối lượng hỗn hợp đầu
Giúp em với em đang cần gấp
Bài 1:
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\\ n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ Al_2O_3+6HCl\rightarrow2AlCl_3+3H_2\\ n_{Al}=\dfrac{2}{3}.0,3=0,2\left(mol\right)\\ \Rightarrow m_{Al}=0,2.27=5,4\left(g\right)\\ \%m_{Al}=\dfrac{5,4}{26,82}.100\approx20,134\%\\\Rightarrow \%m_{Al_2O_3}\approx79,866\%\\ b,n_{Al_2O_3}=\dfrac{26,82-5,4}{102}=0,21\left(mol\right)\\ n_{HCl}=6.0,21+2.0,3=1,86\left(mol\right)\\ V_{ddHCl}=\dfrac{1,86}{2}=0,93\left(l\right)=930\left(ml\right)\\ m_{ddHCl}=930.1,12=1041,6\left(g\right)\\ n_{AlCl_3}=2.0,21+0,2=0,62\left(mol\right)\\ C\%_{ddAlCl_3}=\dfrac{0,62.133,5}{1041,6-0,3.2}.100\approx7,951\%\)
2)
a) Gọi KL và oxit của nó là M và MO
nHCl = 4.0,25 = 1 (mol)
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: M + 2HCl --> MCl2 + H2
0,3<-0,6<--------------0,3
MO + 2HCl --> MCl2 + H2O
0,2<---0,4
=> 0,3.MM + 0,2.(MM + 16) = 31,2
=> MM = 56 (g/mol)
=> Kim loại là Sắt (Fe)
b)
\(\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,3.56}{31,2}.100\%=53,85\%\\\%m_{FeO}=\dfrac{0,2.72}{31,2}.100\%=46,15\%\end{matrix}\right.\)
Bài 2:
Đặt A là kim loại cần tìm
\(a,A+2HCl\rightarrow ACl_2+H_2\left(1\right)\\ AO+2HCl\rightarrow ACl_2+H_2O\left(2\right)\\ n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ n_{HCl\left(ban.đầu\right)}=0,25.4=1\left(mol\right)\\ n_{HCl\left(1\right)}=2.n_{H_2}=0,6\left(mol\right)\\ n_{HCl\left(2\right)}=1-0,6=0,4\left(mol\right)\\ n_{AO}=\dfrac{0,4}{2}=0,2\left(mol\right)\\ n_A=n_{H_2}=0,3\left(mol\right)\\ Vì:m_{hhđầu}=31,2\\ \Leftrightarrow m_A+m_{AO}=31,2\\ \Leftrightarrow0,3.M_A+0,2.\left(M_A+16\right)=31,2\\ \Leftrightarrow M_A=56\left(\dfrac{g}{mol}\right)\\ \Rightarrow A:Sắt\left(Fe=56\right)\\ b,\%m_{Fe}=\dfrac{0,3.56}{31,2}.100\approx53,846\%\\ \Rightarrow\%m_{FeO}\approx46,154\%\)
Cho a(g) hỗn hợp của 2 kim loại Al và Zn tác dụng với lượng Oxi dư thu được 32(g) hỗn hợp 2 oxit .
Cũng lấy lượng hỗn hợp kim loại như trên cho tác dụng vs dung dịch HCl dư , sau phản ứng thu được 56l khí H2 .(đktc)
a) Viết phương trình phản ứng
b) Tính khôi lượng hỗn hợp ban đầu
Khử 3,48 g một oxit của kim loại M cần dùng 1,344 lít H2(đktc). Toàn bộ lượng kim loại M sinh ra cho tác dụng với dung dịch HCl dư thu được 1,008 lít H2 (đktc). Công thức oxit là :
A. Fe3O4.
B. Fe2O3.
C. FeO.
D. ZnO.
khử hoàn toàn m(g) Fe2O3 ở nhiệt độ cao bằng CÓ.Cho lượng Fe thu được sau phản ứng tác dụng hoàn toàn với HCl . Sau phản ứng thu được dung dịch FeCl2 và H2. Nếu dùng lượng H2 vừa đủ để khử Oxi của 1 kim loại có hóa trị 2 thì thấy khối lượng oxit của kim loại bị khử cũng là m gam. Tìm CTHH của Oxit kim loại
Bài 12. Hòa tan 32g oxit của một kim loại hóa trị III cần dùng 300ml dung dịch H2SO4
2M
a) Xác định công thức của oxit kim loại?
b) Tính khối lượng muối tạo thành sau phản ứng?
Bài 13. Cho 9g hỗn hợp gồm Al và Ag tác dụng hết với với dd acid H2SO4 10%, thu được
7,437 lít khí (25độC, 1bar).
a. Tính khối lượng và thành phần % về khối lượng của mỗi kim loại có trong hỗn
hợp.
b. Tính khối lượng dd acid H2SO4 đã dùng
Bài 14. Cho 0,83g hỗn hợp gồm nhôm và sắt tác dụng với dung dịch H2SO4 loãng, dư.
Sau phản ứng thu được 0,61975 lít khí ở 25C, 1bar
a) Viết các phương trình hóa học?
b) Tính thành phần % theo khối lượng của mỗi kim loại trong hỗn hợp đầu?
Bài 15. Cho 20 g hỗn hợp bột Mg và Fe tác dụng với dung dịch HCl dư thấy có 12,395 lít
khí H2 bay ra (2độC, 1bar). Khối lượng muối clorua tạo ra trong dung dịch là bao
nhiêu gam?
Bài 12
a. Gọi kim loại cần tìm là R có \(PTK=x\)
\(n_{R_2O_3}=\dfrac{32}{2x+48}\left(mol\right);n_{H_2SO_4}=2\cdot0,3=0,6\left(mol\right)\\ PTHH:R_2O_3+3H_2SO_4\rightarrow R_2\left(SO_4\right)_3+3H_2O\\ \Rightarrow n_{R_2O_3}=\dfrac{1}{3}n_{H_2SO_4}=0,2\left(mol\right)\\ \Rightarrow\dfrac{32}{2x+48}=0,2\\ \Rightarrow2x+48=160\\ \Rightarrow x=56\left(đvC\right)\)
Vậy kim loại cần tìm là Fe (sắt) có CT oxit là \(Fe_2O_3\)
b. \(PTHH:Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
\(\Rightarrow n_{Fe_2\left(SO_4\right)_3}=n_{Fe_2O_3}=0,2\left(mol\right)\\ \Rightarrow m_{Fe_2\left(SO_4\right)_3}=0,2\cdot400=80\left(g\right)\)
Bài 13:
a. Vì Ag không phản ứng với \(H_2SO_4\) nên 7,437 lít khí là sản phẩm của Al với \(H_2SO_4\)
\(PTHH:2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ n_{H_2}=\dfrac{7,437}{24,79}=0,3\left(mol\right)\\ \Rightarrow n_{Al}=0,2\left(mol\right)\\ \Rightarrow m_{Al}=0,2\cdot27=5,4\left(g\right)\\ \Rightarrow\%m_{Al}=\dfrac{5,4}{9}\cdot100\%=60\%\\ \Rightarrow\%m_{Ag}=100\%-60\%=40\%\)
b. \(n_{H_2SO_4}=n_{H_2}=0,3\left(mol\right)\)
\(\Rightarrow m_{CT_{H_2SO_4}}=0,3\cdot98=29,4\left(g\right)\\ \Rightarrow m_{dd_{H_2SO_4}}=\dfrac{29,4\cdot100\%}{10\%}=294\left(g\right)\)
Cho 6,2g Oxit kim loại M hóa trị I tác dụng với H2O dư được dung dịch A có tính kiềm.Chia A thành 2 phần bằng nhau:
Phần I:Cho tác dụng với 95ml dung dịch HCl 1M,thấy dng dịch sau phản ứng làm xanh quỳ tím
Phần II:Cho tác dụng với 55ml dung dịch HCl 2M,thấy dung dịch sau phản ứng làm đỏ quỳ tím
Xác định công thức oxit của M.Gọi tên
nêu cả cách giải vs
gọi Oxit kim loại M là A2O
cho M tác dụng với H2O dư được dung dịch A có tính kiềm
PTHH: \(A2O+H2O->2AOH\)(1)
theo phần 1 khi cho dung dịch thu được trong pư(1) tác dụng vs dd HCl (95ml) thấy dung dịch sau pư làm quỳ tím xanh
=>AOH+HCL\(->ACL+H2O\)
ta có \(C\left(HCL\right)=\dfrac{nHCL}{VHCL}=>nHCL=VHCl.C\left(HCL\right)=\dfrac{95}{1000}.1=0,095mol\)
do dung dịch sau pư LÀM quỳ tím háo xanh=>AOH dư
=>nA2O>nHCL=>nA2O>0,095(2)
theo phần 2 vì khi cho dung dịch thu đc sau pư (1) Cho tác dụng với 55ml dung dịch HCl 2M,thấy dung dịch sau phản ứng làm đỏ quỳ tím
=>pthh: AOH+HCL->ACL+H2O
tương tự trên =>\(nHCL=2.\dfrac{55}{1000}=0,11mol\)
vì sau pư thấy dd làm đỏ q tím=>HCL còn dư=>nA2O<nHCL=0,11(3)
từ(2)(3)=>0,095<nA2O<0,01=>\(\dfrac{6,2}{0,095}>\dfrac{6,2}{nA2O}>\dfrac{6,2}{0,11}\)
=>65,2>MA2O>56,3=>MA2O=62(g/mol)=>A là Na=>ct : NA2O
natri oxit