Đốt cháy hoàn toàn 0.9g hợp chất hữu cơ A, thu được khí 1,32 g CO2 và 0.54 g H2O.
a)Xác định CTPT của a biết khối lượng mol của A là 180
b) tính khối lượng bạc sinh ra khi oxi hóa 18g A
Giúp em với
1. Hợp chất hữu cơ (A) gồm 3 nguyên tố. Khi đốt cháy A trong khí oxi chỉ thu được CO2 và H2O. Biết khối lượng mol của A bằng 60 g/mol và nguyên tố oxi chiếm 53,33% theo khối lượng.
Tìm CTPT của A.
Giả sử có 1 mol A => mA = 1.60 = 60(g)
=> \(m_O=\dfrac{53,33.60}{100}=32\left(g\right)=>n_O=\dfrac{32}{16}=2\left(mol\right)\)
=> CTPT: CxHyO2
=> 12x + y + 32 = 60
=> 12x + y = 28
=> Chọn x = 2; y = 4
=> CTPT: C2H4O2
đốt cháy hoàn toàn 6 gam hợp chất hữu cơ A thu được 8,8 gam khí CO2 và 3,6 gam H2O a) hợp chất chứa những nguyên tố hóa học nào ?
b)Xác định CTPT của A biết khối lượng mol của A là 60 gam
c) Viết CTCT chi tiết và thu gọn của A biết phân tử A có nhóm-COOH
d) Viết PTHH của A với dung dịch NaOH
GIÚP MÌNH VỚI Ạ MÌNH CẢM ƠN
\(n_{CO_2}=\dfrac{8,8}{44}=0,2\left(mol\right)\) -> \(n_C=0,2\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\) -> \(n_H=0,4\)
\(m_C+m_H=0,2.12+0,4=2,8\left(g\right)\)
-> Trong A có \(m_O=6-2,8=3,2\left(g\right)\)
\(n_O=\dfrac{3,2}{16}=0,2\left(mol\right)\)
Gọi CTPT của A là \(C_xH_yO_z\)
\(x:y:z=n_C:n_H:n_O=0,2:0,4:0,2=1:2:1\)
\(\Leftrightarrow\left(CH_2O\right)_n=60.\Rightarrow n=2\)
a. CTPT của A là \(C_2H_4O_2\)
b. CTCT thu gọn:
\(CH_3COOH\)
mình không gõ được CTCT chi tiết (bạn lên mạng xem nhé)
c. \(CH_3COOH+NaOH\rightarrow CH_3COONa+H_2O\)
Đốt cháy hoàn toàn 0,9 gam một hợp chất hữu cơ A có thành phần gồm các nguyên tố C, H, O người ta thu được 1,32 gam CO2 và 0,54 gam H2O. Khối lượng phân tử của A bằng 180 đv.C. Hãy xác định CTPT của A.
\(n_{CO_2}=\dfrac{1,32}{44}=0,03mol\Rightarrow n_C=0,03\Rightarrow m_C=0,36g\)
\(n_{H_2O}=\dfrac{0,54}{18}=0,03mol\Rightarrow n_H=0,06mol\Rightarrow m_H=0,06g\)
Nhận thấy \(m_C+m_H=0,42< m_A=0,9g\Rightarrow\)có chứa oxi.
\(\Rightarrow m_O=0,9-0,42=0,48g\)
Gọi CTHH là \(C_xH_yO_z\)
\(x:y:z=\dfrac{m_C}{12}:\dfrac{m_H}{1}:\dfrac{m_O}{16}=\dfrac{0,36}{12}:\dfrac{0,06}{1}:\dfrac{0,48}{16}=0,03:0,06:0,03\)
\(\Rightarrow x:y:z=1:2:1\Rightarrow CH_2O\)
Gọi CTPT là \(\left(CH_2O\right)_n\)
\(\Rightarrow M=180=30n\Rightarrow n=6\)
Vậy CTPT cần tìm là \(C_6H_{12}O_6\)
Đốt cháy hoàn toàn m gam hợp chất hữu cơ A cần dùng 11,2 gam khí oxi, thu được 8,8 gam C O 2 và 5,4 gam H 2 O . Ở đktc 2,24 lít khí A có khối lượng 3 gam. Xác định CTPT của A?
A. C 2 H 6
B. C 2 H 4
C. C 3 H 8
D. C 3 H 6
n O 2 = 11,2/32 = 0,35 mol
n C O 2 = 8,8/44 = 0,2 mol ⇒ n C = 0,2 mol
n H 2 O = 5,4/18 = 0,3 mol
⇒ n H = 2.0,3 = 0,6 mol
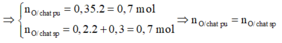
Vậy hợp chất hữu cơ A chỉ có C và H.
Gọi CTTQ của A là C x H y , khi đó ta có:
Vậy CTĐGN của A là C H 3 n
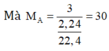
⇒ n = 30/15 = 2
Vậy A là C 2 H 6 .
⇒ Chọn A.
giúp em giải Đốt cháy hoàn toàn 7 gam một hợp chất hữu cơ A thu được 11,2 lít Co2 (dktc) và 9 gam H2O. a) tính khối lượng của các nguyên tố trong A . b) xác định CTĐGN, CTPT của A biết d A/He =7
\(n_{CO_2}=n_{H_2O}=0,5\left(mol\right)\\ m_C+m_H=0,5.12+0,5.2=7\left(g\right)\\ \Rightarrow A.c\text{ó}:C,H\\ n_H=2n_C\Rightarrow Anken:C_nH_{2n}\\ M\text{à}:M_A=4.7=28\left(\dfrac{g}{mol}\right)=14n\\ \Rightarrow n=2\Rightarrow CTPT:C_2H_4\left(CH_2=CH_2\right)\)
đốt cháy hoàn toàn 6g hợp chất hữu cơ A thu đc 4,48l CO2(đktc) và 3,6g h2o a: tính CTPT của A biết MA= 60g/mol b: dẫn toàn bộ lượng CO2 qua dd Ca(OH)2 tính khối lượng khí thu đc
a.Bảo toàn C: \(n_C=n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\)
Bảo toàn H: \(n_H=2.n_{H_2O}=2.\dfrac{3,6}{18}=0,4mol\)
\(n_O=\dfrac{6-\left(0,2.12+0,4.1\right)}{16}=0,2mol\)
=> A gồm C,H và O
\(CTPT:C_xH_yO_z\)
\(x:y:z=0,2:0,4:0,2=2:4:2\)
\(CTĐG:\left(C_2H_4O_2\right)n=60\)
\(\Leftrightarrow n=1\)
Vậy CTPT A: \(C_2H_4O_2\) hay \(CH_3COOH\)
b.\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,2 0,2 ( mol )
\(m_{CaCO_3}=0,2.100=20g\)
Đốt cháy 4.5g chất hữu cơ A thu được 6.6g khí CO2 và 2.7 g H2O .Xác định công thức phân tử hợp chất hữu cơ A . Biêt khối lượng mol của hợp chất là 60g/mol.
Ta có: n C=n CO2=0,15 mol; n H=2.n H2O=0,3 mol
mC+mH=2,1 g < m HCHC
-->HCHC chứa Oxi
mO=2,4g -->n O=0,15 mol
Đặt CTDGN là CxHyOz
x:y:z=0,15:0,3:0,15=1:2:1
-->CTĐGN là CH2O
Đốt cháy hoàn toàn 0,9 g một chất hữu cơ có thành phần c h o ta được 1,32 gam CO2 và 0,54 gam H2O khối lượng phân tử chất đó là 180 xác định công thức phân tử của chất hữu cơ trên Giúp em vs ạ
\(n_{CO_2}=\dfrac{1,32}{44}=0,03\left(mol\right)\)
\(n_{H_2O}=\dfrac{0,54}{18}=0,03\left(mol\right)\)
Bảo toàn C: nC = 0,03 (mol)
Bảo toàn H: nH = 0,06 (mol)
=> \(n_O=\dfrac{0,9-0,03.12-0,06.1}{16}=0,03\left(mol\right)\)
Xét nC : nH : nO = 0,03 : 0,06 : 0,03 = 1 : 2 : 1
=> CTPT: (CH2O)n
Mà PTK = 180 đvC
=> n = 6
=> CTPT: C6H12O6
Đốt cháy hoàn toàn 4,5 gam 1 hợp chất hữu cơ A thu được 6,6 gam CO2 và 2,7 gam H2O. Biết khối lượng mol của phân tử hợp chất hữu cơ là 60g/mol. Xác định CTHH của hợp chất hữu cơ
\(TrongA:n_C=n_{CO_2}=0,15\left(mol\right)\\ n_H=2n_{H_2O}=0,3\left(mol\right)\\ \Rightarrow n_O=\dfrac{4,5-12.0,15-0,3.1}{16}=0,15\left(mol\right)\\ \Rightarrow CTPT:C_xH_yO_z\\ Tacó:x:y:z=0,15:0,3:0,15=1:2:1\\ \Rightarrow CTĐGN:\left(CH_2O\right)_n\\ Tacó:\left(12+2+16\right).n=60\\ \Rightarrow n=2\\ Vậy:CTHHcủaA:C_2H_4O_2\)