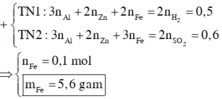cho 14.8g hỗn hợp X gồm Fe VÀ Cu tác dụng vừa đủ với dd150ml ddH2SO4 aM (loãng) thu được 3.36 lít khí h2 (đktc). Mặt khác, cũng hỗn hợp X trên đem hòa tang hết trong axit H2SO4 đặc nóng thu được V lit khí SO2(dktc). a.tinh%về khối lượng khí so2
b. tính a
c. tính v

Những câu hỏi liên quan
Hỗn hợp X gồm Al, Zn và Fe. Cho m gam hỗn hợp X tác dụng với H2SO4 loãng, dư thu được 5,6 lít H2 (đktc). Mặt khác, khi hòa tan hoàn toàn X trong dung dịch H2SO4 đặc, nóng dư thu được 6,72 lít SO2 (đktc). Tính khối lượng Fe có trong m gam hỗn hợp X A. 5,6 gam B. 8,4 gam C. 6,72 gam D. 2,8 gam
Đọc tiếp
Hỗn hợp X gồm Al, Zn và Fe. Cho m gam hỗn hợp X tác dụng với H2SO4 loãng, dư thu được 5,6 lít H2 (đktc). Mặt khác, khi hòa tan hoàn toàn X trong dung dịch H2SO4 đặc, nóng dư thu được 6,72 lít SO2 (đktc). Tính khối lượng Fe có trong m gam hỗn hợp X
A. 5,6 gam
B. 8,4 gam
C. 6,72 gam
D. 2,8 gam
Đáp án : A
nH2 = 0,25 mol; nSO2 = 0,3 mol
2H+ + 2e → H2 S+6 + 2e → S+4
0,5 <-- 0,25 0,6 <-- 0,3
nFe = 0,6 – 0,5 = 0,1 mol
=> mFe = 5,6g
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Al, Zn và Fe. Cho m gam hỗn hợp X tác dụng với H2SO4 loãng dư, thu được 5,6 lít H2 (đktc). Mặt khác, khi hòa tan hoàn toàn X trong dung dịch H2SO4 đặc nóng (dư), thu được 6,72 lít SO2 (đktc). Khối lượng Fe có trong m gam hỗn hợp X là A. 5,6 gam. B. 8,4 gam. C. 6,72 gam. D. 2,8 gam.
Đọc tiếp
Hỗn hợp X gồm Al, Zn và Fe. Cho m gam hỗn hợp X tác dụng với H2SO4 loãng dư, thu được 5,6 lít H2 (đktc). Mặt khác, khi hòa tan hoàn toàn X trong dung dịch H2SO4 đặc nóng (dư), thu được 6,72 lít SO2 (đktc). Khối lượng Fe có trong m gam hỗn hợp X là
A. 5,6 gam.
B. 8,4 gam.
C. 6,72 gam.
D. 2,8 gam.
Cho 21,6 gam hỗn hợp X gồm Fe và MgSO3 tác dụng vừa đủ với dung dịch H2SO4 loãng, sau phản ứng thu được 6,72 l hỗn hợp khí (đktc)a) Xác định khối lượng các chất trong Xb) Cho toàn bộ lượng X trên tác dụng với H2SO4 đặc, nóng dư thu được V lít khí SO2 (sản phẩm khử duy nhất ở đktc). Tính Vc) Tính số mol KOH tối thiểu để hấp thụ hết V lít SO2 trênd) Cho 0,03 mol Ba(OH)2 tác dụng hoàn toàn với 0,1 V lít SO2 trên. Tính khối lượng kết tủa thu được
Đọc tiếp
Cho 21,6 gam hỗn hợp X gồm Fe và MgSO3 tác dụng vừa đủ với dung dịch H2SO4 loãng, sau phản ứng thu được 6,72 l hỗn hợp khí (đktc)
a) Xác định khối lượng các chất trong X
b) Cho toàn bộ lượng X trên tác dụng với H2SO4 đặc, nóng dư thu được V lít khí SO2 (sản phẩm khử duy nhất ở đktc). Tính V
c) Tính số mol KOH tối thiểu để hấp thụ hết V lít SO2 trên
d) Cho 0,03 mol Ba(OH)2 tác dụng hoàn toàn với 0,1 V lít SO2 trên. Tính khối lượng kết tủa thu được
Cho m gam hỗn hợp X gồm Fe và Cu tác dụng với 800g dung dịch H2SO4 loãng (lấy dư 10% so với lượng tham gia phản ứng) thì thu được 4,48 lit H2 (đktc) và dung dịch Y. Mặc khác, nếu cho m gam X trên tác dụng với H2SO4 đặc, nóng, dư thì thu được 8,96 lít khí SO2 (đktc)a) Viết các PTHH xảy rab) Tính khối lượng mỗi chất trong hỗn hợp Xc) Tính nồng độ phần trăm của dung dịch H2SO4 loãng ban đầu.----------------------------------các bạn giúp tớ với!!
Đọc tiếp
Cho m gam hỗn hợp X gồm Fe và Cu tác dụng với 800g dung dịch H2SO4 loãng (lấy dư 10% so với lượng tham gia phản ứng) thì thu được 4,48 lit H2 (đktc) và dung dịch Y. Mặc khác, nếu cho m gam X trên tác dụng với H2SO4 đặc, nóng, dư thì thu được 8,96 lít khí SO2 (đktc)
a) Viết các PTHH xảy ra
b) Tính khối lượng mỗi chất trong hỗn hợp X
c) Tính nồng độ phần trăm của dung dịch H2SO4 loãng ban đầu.
----------------------------------
các bạn giúp tớ với!!
Cho 11,2 gam hỗn hợp X gồm Cu và kim loại M tác dụng với dung dịch H2SO4 loãng dư, thu được 3,136 lít khí H2. Cũng lượng hỗn hợp X như vậy cho tác dụng hết với dung dịch H2SO4 đặc nóng dư, thu được 5,88 lít (đktc) khí SO2 (sản phẩm khử duy nhất ). Xác định kim loại M
TH1: Hóa trị `M` đổi `->M:\ Fe`
`Fe^0->Fe^{+2}+2e`
`2H^{-1}+2e->H_2^0`
Bảo toàn electron: `n_{Fe}=n_{H_2}=0,14(mol)`
`->n_{Cu}={11,2-0,14.56}/{64}=0,0525(mol)`
`Cu^0->Cu^{+2}+2e`
`Fe^0->Fe^{+3}+3e`
`S^{+6}+2e->S^{+4}`
Bảo toàn electron: `2n_{Cu}+3n_{Fe}=2n_{SO_2}=0,525`
`->2.0,0525+3.0,14=0,525`
Nhận.
`->M` là Iron `(Fe).`
TH2: Hóa trị `M` không đổi.
`M` hóa trị `n`
Đặt `n_{Cu}=x(mol);n_M=y(mol)`
`M^0->M^{+n}+n.e`
`2H^{-1}+2e->H_2^0`
Bảo toàn electron: `ny=2n_{H_2}=0,28`
`->y={0,28}/n(mol)`
`M^0->M^{+n}+n.e`
`Cu^0->Cu^{+2}+2e`
`S^{+6}+2e->S^{+4}`
Bảo toàn electron: `2x+ny=2n_{SO_2}=0,525`
`->x={0,525-0,28}/2=0,1225(mol)`
`->m_M=11,2-0,1225.64=3,36(g)`
`->M_M={3,36}/{{0,28}/n}=12n`
`->n=2;M_M=24`
`->M` là magnesium `(Mg).`
Vậy `M` là `Mg` hoặc `Fe.`
Đúng 2
Bình luận (0)
Hỗn hợp X gồm Zn, Fe, Cu. Cho 18,5 gam hỗn hợp X tác dụng với dung dịch HCl dư thu được 4,48 lit H2 (đktc). Mặt khác cho 0,15 mol hỗn hợp X phản ứng vừa đủ với 3,92 lít khí Cl2 (đktc). Số mol Fe có trong 18,5 gam hỗn hợp X là A. 0,12 mol B. 0,15 mol C. 0,1 mol D. 0,08 mol
Đọc tiếp
Hỗn hợp X gồm Zn, Fe, Cu. Cho 18,5 gam hỗn hợp X tác dụng với dung dịch HCl dư thu được 4,48 lit H2 (đktc). Mặt khác cho 0,15 mol hỗn hợp X phản ứng vừa đủ với 3,92 lít khí Cl2 (đktc). Số mol Fe có trong 18,5 gam hỗn hợp X là
A. 0,12 mol
B. 0,15 mol
C. 0,1 mol
D. 0,08 mol
Đáp án C
Đặt số mol mỗi kim loại trong 18,5 gam hỗn hợp lần lượt là a, b, c.
Ta có: mhh X =65a + 56b + 64c; n H 2 = a + b = 3 , 92 22 , 4 = 0 , 175 mol
Có số phân tử Cl2 phản ứng trung bình với hỗn hợp X:
n Cl 2 n X = 0 , 175 0 , 15 = 7 6 = ( a + 1 , 5 b + c ) ( a + b + c )
Từ đó ta có a - 2b + c = 0.
Tóm lại ta sẽ có a = b = c = 0,1 mol.
Vậy trong 18,5g hỗn họp X sẽ có 0,1 mol Fe
Chú ý:
Dung dịch axit như dung dịch HCl, HBr, HI hoặc dung dịch H2SO4 có khả năng phản ứng với các kim loại đứng trước H trong dãy điện hóa, tức là trong bài này phản ứng với Zn và Fe tạo ra ZnCl2 và FeCl2.
- Clo có khả năng phản ứng với hầu hết các kim loại (trừ Au, Pt) thậm chí còn có khả năng phản ứng với Ag ở điều kiên thích hợp và đưa kim loại lên số oxi hóa cao nhất vì vậy sản phẩm là ZnCl2,CuCl2,FeCl3
Đúng 0
Bình luận (0)
Cho 12 gam hỗn hợp X gồm 2 kim loại Fe và Cu tác dụng với H2SO4 ( đặc nóng) vừa đủ thu được 5,6 lit khí không màu, mùi hắc (đktc, sản phẩm khử duy nhất).
a. Tính khối lượng của Fe có trong hỗn hợp ban đầu.
b. Nếu cho một nửa hỗn hợp X trên tác dụng với H2SO4 loãng thì khí thu được là khí gì? Tính thể tích khí thu được ở đktc
a)
Gọi số mol Fe, Cu là a, b (mol)
=> 56a + 64b = 12 (1)
\(n_{SO_2}=\dfrac{5,6}{22,4}=0,25\left(mol\right)\)
PTHH: 2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
a------------------------------->1,5a
Cu + 2H2SO4 --> CuSO4 + SO2 + 2H2O
b---------------------------->b
=> 1,5a + b = 0,25 (2)
(1)(2) => a = 0,1 (mol); b = 0,1 (mol)
=> mFe = 0,1.56 = 5,6 (g)
b)
1 nửa hỗn hợp X trên chứa \(\left\{{}\begin{matrix}Fe:0,05\left(mol\right)\\Cu:0,05\left(mol\right)\end{matrix}\right.\)
PTHH: Fe + H2SO4 --> FeSO4 + H2
0,05---------------------->0,05
=> Thu được khí H2
VH2 = 0,05.22,4 = 1,12 (l)
Đúng 2
Bình luận (2)
Cho 20,4 gam hỗn hợp gồm Zn, Fe, Al tác dụng với dd chứa HCl và H2SO4 loãng dư thu được 10,08 lít khí H2. Mặt khác 0,2 mol hỗn hợp X tác dụng vừa đủ với 6,16 lít khí Cl2 (đktc). Xác định khối lượng mỗi kim loại trong 20,4 gam X
Trong \(20,4g\) hỗn hợp có: \(\left\{{}\begin{matrix}n_{Zn}=a\left(mol\right)\\n_{Fe}=b\left(mol\right)\\n_{Al}=c\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow65a+56b+27c=20,4\left(1\right)\)
\(n_{H_2}=\dfrac{10,08}{22,4}=0,45mol\)
\(BTe:2n_{Zn}+2n_{Fe}+3n_{Al}=2n_{H_2}\)
\(\Rightarrow2a+2b+3c=2\cdot0,45\left(2\right)\)
Trong \(0,2mol\) hhX có \(\left\{{}\begin{matrix}Zn:ka\left(mol\right)\\Fe:kb\left(mol\right)\\Al:kc\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow ka+kb+kc=0,2\)
\(n_{Cl_2}=\dfrac{6,16}{22,4}=0,275mol\)
\(BTe:2n_{Zn}+3n_{Fe}+3n_{Al}=2n_{Cl_2}\)
\(\Rightarrow2ka+3kb+3kc=2\cdot0,275\)
Xét thương:
\(\dfrac{ka+kb+kc}{2ka+3kb+3kc}=\dfrac{0,2}{2\cdot0,275}\Rightarrow\dfrac{a+b+c}{2a+3b+3c}=\dfrac{4}{11}\)
\(\Rightarrow3a-b-c=0\left(3\right)\)
Từ (1), (2), (3)\(\Rightarrow\left\{{}\begin{matrix}a=0,1mol\\b=0,2mol\\c=0,1mol\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}m_{Zn}=6,5g\\m_{Fe}=11,2g\\m_{Al}=2,7g\end{matrix}\right.\)
Đúng 2
Bình luận (1)
Cho 2,4 gam hỗn hợp X gồm Fe và Cu tác dụng với dung dịch axit sunfuric loãng , dư thu được V ml khí hidro ( đktc ) . Nếu cho m gam hỗn hợp X đó tác dụng với dung dịch axit sunfuric đặc nóng dư thì thu được 1,12 lít khí sunfurơ ( đktc ) . a . Tính V. b . Tính thành phần phần trăm về khối lượng các chất trong hỗn hợp X. c . Dẫn toàn bộ lượng khí sunfurơ thu được vào 50ml dung dịch NaOH 1,2M . Tính nồng độ mol / l của chất tan trong dung dịch sau phản ứng . Coi thể tích dung dịch không đổi .
Đọc tiếp
Cho 2,4 gam hỗn hợp X gồm Fe và Cu tác dụng với dung dịch axit sunfuric loãng , dư thu được V ml khí hidro ( đktc ) . Nếu cho m gam hỗn hợp X đó tác dụng với dung dịch axit sunfuric đặc nóng dư thì thu được 1,12 lít khí sunfurơ ( đktc ) . a . Tính V. b . Tính thành phần phần trăm về khối lượng các chất trong hỗn hợp X. c . Dẫn toàn bộ lượng khí sunfurơ thu được vào 50ml dung dịch NaOH 1,2M . Tính nồng độ mol / l của chất tan trong dung dịch sau phản ứng . Coi thể tích dung dịch không đổi .