Đốt cháy hiđrocacbon A, người ta thu được CO2 và H2O theo tỉ lệ mCO2:mH2O=44:9. Biết A không làm mất màu dung dịch brom.
Hỏi A là hiđrocacbon nào trong số các hiđrocacbon sau ?
CH ≡ CH ; CH3 - CH3 ; CH2 = CH - C = CH ; CH2 = CH2 ; Benzen
Đốt cháy hiđrocacbon A, người ta thu được CO 2 và H 2 O theo tỉ lệ m CO 2 : m H 2 O = 44 : 9. Biết A không làm mất màu dung dịch brom.
Hỏi A là hiđrocacbon nào trong số các hiđrocacbon sau ?
CH ≡CH ; CH 3 - CH 3 ; CH 2 = CH - C = CH ; CH 2 = CH 2 ;
Gọi công thức phân tử của A là: C x H y
C x H y → x CO 2 + y/2 H 2 O
Theo đề bài ta có: 44x : 9y = 44 : 9
⇒ x : y = 1 : 1 ⇒ C 6 H 6
A, B, C là ba hiđrocacbon khi đốt cháy đều thu được số mol khí CO 2 bằng hai lần số mol hiđrocacbon đem đốt. Biết :
A không làm mất màu dung dịch brom.
Một mol B tác dụng được tối đa với 1 mol brom.
Một mol C tác dụng được tối đa với 2 mol brom.
Hãy xác định công thức phân tử và công thức cấu tạo của A, B, C.
Gọi công thức của ba hiđrocacbon đó là : C x H y , C a H b , C n H m
Khi đốt ta có :
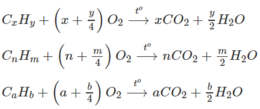
Vì số mol CO 2 tạo ra bằng 2 lần số mol hiđrocacbon đem đốt. Vậy theo phương trình hoá học của phản ứng cháy
→ X = a = n = 2.
Mặt khác : A không làm mất màu nước brom → không có liên kết đôi hoặc ba. Vậy A là CH 3 - CH 3
1 mol B chỉ tác dụng tối đa với 1 mol brom → có 1 liên kết đôi.
Vậy B là CH 2 = CH 2
1 mol C tác dụng tối đa với 2 mol brom → có liên kết ba.
Vậy C là CH ≡CH.
Đốt cháy hoàn toàn hỗn hợp X gồm axetilen, etilen và hiđrocacbon A thu được CO2 và H2O theo tỉ lệ mol 1 : 1. Dẫn X đi qua bình đựng dung dịch brom dư thấy khối lượng bình tăng 0,82 gam, đốt cháy hoàn toàn khí thoát ra khỏi bình brom thu được 1,32 gam CO2 và 0,72 gam H2O. Phần trăm thể tích của A trong X là
A. 50%.
B. 75%.
C. 25%.
D. 33,33%.
Đốt cháy hoàn toàn 2,24l hiđrocacbon thể khí thu được 6,72l CO2 và 5,4 g H2O . Các thể tích khí đo ở đktc . Xác định Công thức phân tử H-C ; viết CTCT của H-C biết rằng hợp chất có thể làm mất màu dung dịch Brom
\(n_{HC}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\\ n_{H_2O}=\dfrac{5,4}{18}=0,3\left(mol\right)\\ Vì:n_{CO_2}=n_{H_2O}\\ \Rightarrow Hidrocacbon:Anken\left(Do.td.được.với.Brom\right)\\ Đặt.CTTQ:C_aH_{2a}\left(a\ge2\right)\\ Ta.có:a=\dfrac{n_{CO_2}}{n_{hidrocacbon}}=\dfrac{0,3}{0,1}=3\\ \Rightarrow CTPT:C_3H_6\\ CTCT:CH_2=CH-CH_3\)
Tham khảo:
Đặt công thức phân tử của A là
CxHyOz CxHy + (x + y/4)O2 → xCO2 + y/2H2O
0,1 0,3 0,3
Ta có:
0,1 : 1 = 0,3 : x → x = 3
0,1 : 1 = (0,3.2) : y → y = 6
Vậy A là C3H6 nhé
Hỗn hợp X gồm axetilen, etilen và hiđrocacbon A cháy hoàn toàn thu được CO2 và H2O theo tỉ lệ mol 1:1. Dẫn X đi qua bình đựng dung dịch brom dư thấy khối lượng bình tăng lên 0,82 gam, khí thoát ra khỏi bình đem đốt cháy hoàn toàn thu được 1,32 gam CO2 và 0,72 gam H2O. Phần trăm thể tích của A trong hỗn hợp X là
A. 25%
B. 66,66%
C. 33,33%
D. 75%
Đáp án A
Hỗn hợp chứa axetilen, etilen và chất A khi đốt thu được CO2 và H2O tỉ lệ 1:1 thì chất A chắc chắn phải là ankan (do axetilen đốt thu được nCO2 > nH2O, etilen đốt thu được nCO2=nH2O, cần phải có 1 chất đốt thu được nCO2< nH2O để đảm bảo tỉ lệ)
Hơn nữa, nC2H2=nA
Khí thoát ra khỏi bình là ankan:
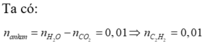
Khối lượng bình tăng lên là khối lượng của axetilen và etilen.

Trong các nhận xét dưới đây, nhận xét nào sai ?
A. Khi đốt cháy hoàn toàn một hiđrocacbon thì sản phẩm thu được chỉ là C O 2 và H 2 O .
B. Nếu sản phẩm của phản ứng đốt cháy hoàn toàn một chất chỉ là C O 2 và H 2 O thì chất đem đốt là hiđrocacbon.
C. Khi đốt cháy hoàn toàn một ankan, thì trong sản phẩm thu được, số mol H 2 O lớn hơn số mol C O 2 .
D. Nếu trong sản phẩm đốt cháy một hiđrocacbon, số mol H 2 O lớn hơn số mol C O 2 thì hiđrocacbon đem đốt phải là ankan.
Đáp án: B (vì chất mang đốt có thể chứa cả oxi).
từ 1 loại tinh dầu người ta tách ra được hợp chất hữu cơ A. Đốt cháy hoàn toàn 2,64g A cần vừa đủ 4,704 lít khí O2(đktc) chỉ thu được CO2 và H2O với tỉ lệ khối lượng là \(\dfrac{mCO2}{mH2O}\) = \(\dfrac{11}{2}\). Biết MA < 150. Xác định công thức phân tử của A
Đốt cháy 1,6(g) chất CxHy cần 6,4 (g) khí oxi thu được khí CO2 và hơi nước theo tỉ lệ mCO2 : mH2O=11:9. Tính mCO2 và mH2O.
gọi mCO2= 11x
=> mH2O=9x
=> mH2O+mCO2=20x
BTKL: mCxHy + mO2= mH2O+mCO2
=> 1,6+6,4=20x
=> x=0,4g
=> mCO2= 11x=4,4g
=> mH2O= 3,6g
Gọi khối lượng của CO2 và H2O lần lượt là 11a và 9a
Áp dụng định luật bảo toàn khối lượng
mM + mO2 = mCO2 + mH2O
=> 1,6 + 6,4 = 11a + 9a
=> 8 = 20a => a = 0,4
=> mCO2 = 4,4g và mH2O = 3,6g
Cho các kết luận sau:
(1) Đốt cháy hiđrocacbon thu được n H 2 O > n C O 2 thì hiđrocacbon đó là ankan.
(2) Đốt cháy hiđrocacbon thu được n H 2 O = n C O 2 thì hiđrocacbon đó có độ bất bão hòa bằng 1.
(3) Đốt cháy ankin thì được n H 2 O < n C O 2 và nankin = = n C O 2 - n H 2 O .
(4) Tất cả các ankin đều có thể tham gia phản ứng thế bởi AgNO3/NH3.
(5) Anilin là chất lỏng, không màu, ít tan trong nước. Để lâu trong không khí, anilin có nhuốm màu đen vì bị oxi hoá.
(6) Cao su là vật liệu polime có tính đàn hồi.
(7) Toluen và stiren đều làm mất màu dung dịch thuốc tím ở điều kiện thường.
Trong các kết luận trên, số kết luận đúng là:
A. 3
B. 4
C. 6
D. 5
Câu 8: Biết 0,2 mol hiđrocacbon A làm mất màu 100ml dung dịch brom 2M. A là hiđrocacbon nào sau đây: *
A. C2H2
B. C2H6
C. C2H4
D. CH4
n Br2 = 0,1.2 = 0,2(mol) = n A
Suy ra A chứa 1 liên kết pi
Chọn đáp án C
\(n_{Br_2}=0.1\cdot2=0.2\left(mol\right)\)
\(n_A=n_{Br_2}=0.2\left(mol\right)\)
\(\Rightarrow A:anken\)
\(\Rightarrow C\)
Ta có: nBr2 = 0,1.2 = 0,2 (mol) = nA
⇒ A là anken.
Đáp án: C
Bạn tham khảo nhé!