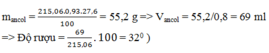Trộn 2l dung dịch rượu etylic có nồng độ 1M vào 3l dung dịch rượu etylic có nồng độ 2M .tính nồng độ của rượu etylic sau khi pha trộn

Những câu hỏi liên quan
Cho em hỏi với ạ....
Trộn 2 lít rượu etylic có nồng độ 1M vào 3 lít dung dịch rượu có nồng độ 2M. Tính nồng độ mol của dung dịch rượu etylic sau khi pha trộn.
Giúp em nhé mọi người, đang cần gấp để ôn thi học kỳ, cám ơn trước ạ..!!
nC2H5OH (1)= 2*1= 2 mol
nC2H5OH (2)= 3*2= 6 mol
VC2H5OH (1,2)= 2 + 3= 5l
nC2H5OH (1,2)= 2+6= 8 mol
CM C2H5OH= 8/5= 1.6M
Đúng 0
Bình luận (1)
Đem hòa tan rượu etylic vào nước được 215,06 ml dung dịch rượu có nồng độ 27,6%, khối lượng riêng của dung dịch rượu là 0,93 g/ml, khối lượng riêng của rượu etylic nguyên chất là 0,8 g/ml. Dung dịch trên có độ rượu là: A. 27,60 B. 220 C. 320 D. Đáp án khác.
Đọc tiếp
Đem hòa tan rượu etylic vào nước được 215,06 ml dung dịch rượu có nồng độ 27,6%, khối lượng riêng của dung dịch rượu là 0,93 g/ml, khối lượng riêng của rượu etylic nguyên chất là 0,8 g/ml. Dung dịch trên có độ rượu là:
A. 27,60
B. 220
C. 320
D. Đáp án khác.
Trộn 10ml rượu etylic 8 độ với 20ml rượu etylic 12 độ tạo ra dung dịch có độ rượu là
A. 20 °
B. 10 °
C. 3,93 °
D. 10,67 °
Đáp án D
Thể tích rượu etylic = 10 x 0,08 + 20 x 0,12 = 3,2 ml.
Thể tích dung dịch = 10 + 20 = 30.
Độ rượu 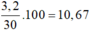
Đúng 0
Bình luận (0)
Cho m gam dung dịch rượu etylic nồng độ 29,87% tác dụng hết với Na (dư) thu được 11,76 lít khí H2 (đktc). Biết khối lượng riêng của rượu etylic là 0,8 g/ml. Độ rượu của dung dịch trên là
m C2H5OH = m.29,87% = 0,2987m(gam)
=> n C2H5OH = 0,2987m/46 (mol)
m H2O = m - 0,2987m = 0,7013m(gam)
=> n H2O = 0,7013m/18(mol)
$2C_2H_5OH + 2Na \to 2C_2H_5ONa + H_2$
$2Na + 2H_2O \to 2NaOH + H_2$
n H2 = 1/2 n C2H5OH + 1/2 H2O = 11,76/22,4 = 0,525(mol)
=> 1/2 . 0,2987m/46 + 1/2 . 0,7013m/18 = 0,525
=> m = 23,1(gam)
Suy ra :
m C2H5OH = 0,2987.23,1 = 6,9(gam)
V C2H5OH = 6,9/0,8 = 8,625(ml)
m H2O = 0,7013.23,1 = 16,2(gam)
V H2O = 16,2/1 = 16,2(ml)
Vậy :
Đr = V C2H5OH / V(dd) .100 = 8,625/(8,625 + 16,2) .100 = 34,74o
Đúng 2
Bình luận (1)
Giúp mk câu này vs ạHòa tan 92 gam rượu etylic (C2H5OH) vào nước để được 250ml dd. Tính nồng độ mol, C%, độ rượu và tỉ khối của dd. Giả thiết k có sự hao hụt về thể tích các chất khi pha trộn và khối lượng riêng của rượu nguyên chất là 0,8g/cm3.
Đọc tiếp
Giúp mk câu này vs ạ![]()
Hòa tan 92 gam rượu etylic (C2H5OH) vào nước để được 250ml dd. Tính nồng độ mol, C%, độ rượu và tỉ khối của dd. Giả thiết k có sự hao hụt về thể tích các chất khi pha trộn và khối lượng riêng của rượu nguyên chất là 0,8g/cm3.
\(n_{C_2H_5OH}=\dfrac{92}{46}=2\left(mol\right)\)
\(CM_{C_2H_5OH}=\dfrac{2}{0,25}=8M\)
\(C\%_{doruou}=\dfrac{92}{250.0,8}.100=46^o\)
Đúng 1
Bình luận (0)
Hòa tan m gam rượu etylic ( D = 0,8 g/ml) vào 108 ml nước ( D= 1 g/ml) tạo thành dung dịch A. Cho dung dịch A tác dụng với kim loại Na dư, thu được 85,12 lít khí H2 (đktc). Tính giá trị m và nồng độ mol của rượu etylic
nH2 = 85,12 : 22,4 = 3,8 (mol) ; nH2O = VH2O.D = 108 (g) => nH2O = 108/18 = 6 (mol)
PTHH:
2Na + 2C2H5OH → 2C2H5ONa + H2↑
x → 0,5x (mol)
2Na + 2H2O → 2NaOH + H2↑
6 → 3 (mol)
Ta có: nH2 = 0,5x + 3 = 3,8
=> x = 1,6 (mol) = nC2H5OH
mC2H5OH = 1,6.46 = 73,6 (g)
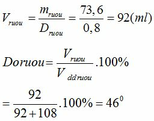
Đúng 0
Bình luận (0)
Giấm ăn được điều chế bằng cách lên men dung dịch rượu etylic ở nồng độ thấp. Hãy tính khối lượng giấm ăn 5% thu được khi lên men 50 lít rượu etylic 4°. Biết hiệu suất của quá trình lên men là 80%
V C 2 H 5 OH = 50.4/100 = 2l
→ m C 2 H 5 OH = 2.1000.0,8 = 1600g
Phương trình hóa học :
C 2 H 5 OH + O 2 → CH 3 COOH + H 2 O
46 gam 60 gam
1600 gam x
x = 1600x60/46
Vì hiệu suất đạt 80% → m CH 3 COOH = 1600.60.80/(46.100) = 1669,6g
→ m giấm = 1669,6/5 x 100 = 33392 (gam) = 33,392 kg
Đúng 0
Bình luận (0)
Để pha loãng rượu etylic, ngta trộn 80ml rượu etylic với 50ml nước. Em hãy:
a) Xác định chất tan và dung môi trong trường hợp này
b) Cho biết thể tích dung dịch sau khi pha loãng
a) Chất tan là rượu etylic
Dung môi lầ nước
b) Thể tích dung dich sau khi pha loãng = Vrượu + Vnước = 50 + 80 = 130 ml
Đúng 1
Bình luận (2)
Giấm ăn được điều chế bằng cách lên men dung dịch rượu etylic ở nồng độ thấp.Tính khối ượng giấm ăn5% thu được khi lên men 25 lít rượu etylic 4độ . biết hiệu suất quá trình lên men là 92% và khối lượng riêng của etylic là 0,8g/mol
\(C_2H_5OH+O_2\rightarrow\left(men.giấm\right)CH_3COOH+H_2O\\ V_{C_2H_5OH}=25.4\%=1\left(l\right)=1000\left(ml\right)\\ m_{C_2H_5OH}=1000.0,8=800\left(g\right)\\ m_{CH_3COOH\left(LT\right)}=\dfrac{800.60}{46}=\dfrac{48000}{46}\left(g\right)\\ m_{CH_3COOH\left(TT\right)}=\dfrac{48000}{46}:92\%=1134,2155\left(gam\right)\\ m_{ddCH_3COOH}=1135,2155:5\%=22684,31\left(g\right)\)
Đúng 1
Bình luận (0)