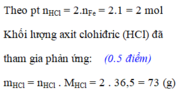Tính khối lượng của muối thu được khi cho 5,6 g sắt vào dung dịch Axit Clohiđric ( HCl ) dư thì thu được muối sắt2 Clorua và khí Hiđrô

Những câu hỏi liên quan
Hòa tan 5,6 (g) sắt (Fe) vào dung dịch chứa 7,3 gam axit clohiđric (HCl) thu được 12,7 (g) muối sắt (II) clorua (FeCl2 ) và khí hiđro. Hãy tính khối lượng của khí hiđro tạo ra sau phản ứng.
BTKL: \(m_{Fe}+m_{HCl}=m_{muối}+m_{H_2}\)
\(\Rightarrow m_{H_2}=5,6+7,3-12,7=0,2\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 11,2g sắt vào dung dịch Axit Clohiđric vừa đủ , thu được muối sắt clorua ( FeCl2) vào khí hiđrô ( đktc )a) Viết phương trình hóa họcb)tính thể tích khí H2 ( đkct ) thu đượccc tính khối lượng Axit Cohiđric ban đầu ( theo 2 cách )Giúp tui đi mai tu...
Xem chi tiết
\(n_{Fe}=\dfrac{11.2}{56}=0.2\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(0.2......0.4...........0.2.........0.2\)
\(V_{H_2}=0.2\cdot22.4=4.48\left(l\right)\)
\(m_{HCl}=0.4\cdot36.5=14.6\left(g\right)\)
\(BTKL:\)
\(m_{HCl}=m_{FeCl_2}+m_{H_2}-m_{Fe}=0.2\cdot127+0.2\cdot2-11.2=14.6\left(g\right)\)
Đúng 1
Bình luận (0)
\(a) Fe + 2HCl \to FeCl_2 + H_2\\ b) n_{H_2} = n_{Fe} = \dfrac{11,2}{56} = 0,2(mol)\\ \Rightarrow V_{H_2} = 0,2.22,4 = 4,48(lít)\\ c)C_1 : n_{HCl} = 2n_{Fe} = 0,4(mol) \Rightarrow m_{HCl} = 0,4.36,5 = 14,6(gam)\\ C_2 : \text{Bảo toàn khối lượng : }\\ m_{Fe} + m_{HCl} = m_{FeCl_2} + m_{H_2}\\ \Rightarrow m_{HCl} = 0,2.127 + 0,2.2 - 11,2 = 14,6(gam) \)
Đúng 1
Bình luận (0)
Hòa tan hoàn toàn 56g sắt bằng dung dịch axit clohiđric(HCl), phản ứng kết thúc thu được muối sắt clorua F e C l 2 và khí hiđro. Tính khối lượng axit clohiđric(HCl) đã tham gia phản ứng.
Cho 22,4g sắt tác dụng với 300 ml dung dịch axit clohiđric 2M thu được muối sắt (II) clorua) và khí hiđro. a. Viết PTHH của phản ứng. b. Tính khối lượng muối sắt (II) clorua tạo thành c. Tính khối lượng chất còn dư sau phản ứng
`a)PTHH:`
`Fe + 2HCl -> FeCl_2 + H_2`
`0,3` `0,6` `0,3` `0,3` `(mol)`
`n_[Fe]=[22,4]/56=0,4(mol)`
`n_[HCl]=0,3.2=0,6(mol)`
Ta có:`[0,4]/1 > [0,6]/2`
`=>Fe` dư
`b)m_[FeCl_2]=0,3.127=38,1(g)`
`c)m_[Fe(dư)]=(0,4-0,3).56=5,6(g)`
Đúng 5
Bình luận (3)
\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\\
n_{HCl}=0,3.2=0,6\left(mol\right)\\
pthh:Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\\
LTL:\dfrac{0,4}{1}>\dfrac{0,6}{2}\)
=> Fe dư
\(n_{FeCl_2}=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\\
m_{FeCl_2}=0,3.127=38,1\left(g\right)\\
n_{Fe\left(p\text{ư}\right)}=\dfrac{1}{2}n_{HCl}=0,3\left(mol\right)\\
m_{Fe\left(d\right)}=\left(0,4-0,3\right).56=5,6\left(g\right)\)
Đúng 3
Bình luận (0)
\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
\(n_{HCl}=0,3.2=0,6\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\)
Xét: \(\dfrac{0,4}{1}>\dfrac{0,6}{2}\) ( mol )
0,3 0,6 0,3 ( mol )
\(m_{FeCl_2}=0,3.127=38,1\left(g\right)\)
\(m_{Fe\left(dư\right)}=\left(0,4-0,3\right).56=5,6\left(g\right)\)
Đúng 3
Bình luận (0)
Xem thêm câu trả lời
Trong phòng thí nghiệm để điều chế khí hiđrô người ta cho kim loại nhôm tác dụng với dung dịch axit clohiđric có chứa 10,95g HCl thu được muối nhôm clorua.
a. Tính thể tích khí hiđrô sinh ra ở đktc.
b. Tính khối lượng sắt thu được khi cho dòng khí hidro sinh ra ở phản ứng trên qua 12
gam bột sắt (III) oxit đun nóng
a.\(n_{HCl}=\dfrac{10,95}{36,5}=0,3mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,3 0,15 ( mol )
\(V_{H_2}=0,15.22,4=3,36l\)
b.\(n_{Fe_2O_3}=\dfrac{12}{160}=0,075mol\)
\(Fe_2O_3+3H_2\rightarrow\left(t^o\right)2Fe+3H_2O\)
\(\dfrac{0,075}{1}\) > \(\dfrac{0,15}{3}\) ( mol )
0,15 0,1 ( mol )
\(m_{Fe}=0,1.56=5,6g\)
Đúng 2
Bình luận (0)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\uparrow\)
1 : 6 : 2 : 3 (mol)
0,05 : 0,3 : 0,1 : 0,15 (mol)
\(n_{HCl}=\dfrac{m}{M}=\dfrac{10,95}{36,5}=0,3\left(mol\right)\)
a. \(V_{H_2\left(đktc\right)}=n.24,79=0,15.24,79=3,7185\left(l\right)\)
b. \(Fe_2O_3+3H_2\rightarrow^{t^0}2Fe+3H_2O\)
1 : 3 : 2 : 3 (mol)
0,075 : 0,15 (mol)
\(n_{Fe_2O_3}=\dfrac{m}{M}=\dfrac{12}{160}=0,075\left(mol\right)\)
-Chuyển thành tỉ lệ: \(\dfrac{0,075}{1}>\dfrac{0,15}{3}=0,05\)
\(\Rightarrow\)H2 phản ứng hết còn Fe2O3 dư.
\(Fe_2O_3+3H_2\rightarrow^{t^0}2Fe+3H_2O\)
1 : 3 : 2 : 3 (mol)
0,05 : 0,15 : 0,1 : 0,15 (mol)
\(\Rightarrow m_{Fe}=n.M=0,1.56=5,6\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 13g kẽm tác dụng hết với 100g dung dịch axit clohiđric a%, thu được muối kẽm clorua và khí hiđro.
a. Tính a.
b. Thể tích khí hiđro thu được ở đktc và khối lượng muối tạo thành.
c. Khi cho lượng kẽm trên tác dụng với 36,5 g axit clohiđric. Tính khối lượng các chất thu được sau phản ứng
\(n_{Zn}=\dfrac{13}{65}=0,2\left(mol\right)\)
Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2|\)
1 2 1 1
0,2 0,4 0,2 0,2
a) \(n_{HCl}=\dfrac{0,2.2}{1}=0,4\left(mol\right)\)
⇒ \(m_{HCl}=0,4.36,5=14,6\left(g\right)\)
\(C_{HCl}=\dfrac{14,6.100}{100}=14,6\)0/0
b) \(n_{H2}=\dfrac{0,4.1}{2}=0,2\left(mol\right)\)
\(V_{H2\left(dktc\right)}=0,2.22,4=4,48\left(l\right)\)
\(n_{ZnCl2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{ZnCl2}=0,2.136=27,2\left(g\right)\)
c) \(n_{HCl}=\dfrac{36,5}{36,5}=1\left(mol\right)\)
Pt : \(Zn+2HCl\rightarrow ZnCl_2+H_2|\)
1 2 1 1
0,2 1 0,2
Lập tỉ số so sánh : \(\dfrac{0,2}{1}< \dfrac{1}{2}\)
⇒ Zn phản ứng hết , Hcl dư
⇒ Tính toán dựa vào số mol của Zn
\(n_{ZnCl2}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
⇒ \(m_{ZnCl2}=0,2.136=27,2\left(g\right)\)
\(n_{HCl\left(dư\right)}=1-\left(0,2.2\right)=0,6\left(mol\right)\)
⇒ \(m_{HCl\left(dư\right)}=0,6.36,5=14,6\left(g\right)\)
Chúc bạn học tốt
Đúng 1
Bình luận (0)
a, Ta có: nZn=\(\dfrac{13}{65}\)=0,2 mol
Zn + 2HCl ---> ZnCl2 + H2
Ta có: nZn=\(\dfrac{1}{2}\)nHCl => nHCl=0,1 mol
=> mHCl=0,1.36,5=3,65 g
=> a%=\(\dfrac{3,65.100}{100}\)=3,65%
b, Ta có: nZn=nZnCl2 = nH2= 0,2 mol
=> VH2=0,2.22,4=4,48 l
=> mZnCl2=0,2.136=27,2 g
c, Zn + 2HCl ---> ZnCl2 + H2
Ta có: nHCl=\(\dfrac{36.5}{36.5}\)=1 mol
Ta có: \(\dfrac{n_{HCl}}{n_{Zn}}=\dfrac{1}{0,2}\) => HCl dư tính theo Zn
Ta có: nZn=nZnCl2 = nH2= 0,2 mol
=> VH2=0,2.22,4=4,48 l
=> mZnCl2=0,2.136=27,2 g
Đúng 0
Bình luận (0)
Bài 6:Thả11,2 gam bột sắt vào dung dịch axit clohiđric HCl đến khi bột sắt tan hết thu được a gam muối sắt (II) clorua FeCl2 và khí hiđro.a.Viết PTHH của phản ứng xảy ra..bTính khối lượng axit clohiđric đã tham gia phản ứng.c.Tính giá trị của a.d.Tính thể tích khí hiđro thu được (ở đktc).Giúp mình với mình cần trong tối nay!
Đọc tiếp
Bài 6:Thả11,2 gam bột sắt vào dung dịch axit clohiđric HCl đến khi bột sắt tan hết thu được a gam muối sắt (II) clorua FeCl2 và khí hiđro.
a.Viết PTHH của phản ứng xảy ra.
.bTính khối lượng axit clohiđric đã tham gia phản ứng.
c.Tính giá trị của a.d.Tính thể tích khí hiđro thu được (ở đktc).
Giúp mình với mình cần trong tối nay!
`a)`
PTHH : `Fe + 2HCl -> FeCl_2 + H_2`
`b)`
`n_{Fe} = (11,2)/(56) = 0,2` `mol`
`n_{HCl} = 2 . n_{Fe} = 0,4` `mol`
`m_{HCl} = 0,4 . 36,5 = 14,6` `gam`
`c)`
`n_{FeCl_2} = n_{Fe} = 0,2` `mol`
`m_{FeCl_2} = 0,2 . 127 = 25,4` `gam`
`n_{H_2} = n_{Fe} = 0,2` `mol`
`V_{H_2} = 0,2 . 22,4 = 4,48` `l`
Đúng 3
Bình luận (2)
Cho 13 g kim loại kẽm ( Zn ) vào dung dịch axit clohiđric ( HCl ) thu được muối kẽm clorua ( ZnCl2 ) và khí hiđro (H2). a. Viết phương trình hóa học của phản ứng. b. Tính khối lượng axit clohiđric cần dùng cho phản ứng? c. Tính thể tích khí hiđro thu được (ở đktc)?
\(n_{Zn}=\dfrac{13}{65}=0,2(mol)\\ a,PTHH:Zn+2HCl\to ZnCl_2+H_2\\ b,n_{HCl}=2n_{Zn}=0,4(mol)\\ \Rightarrow m_{HCl}=0,4.36,5=14,6(g)\\ c,n_{H_2}=n_{Zn}=0,2(mol)\\ \Rightarrow V_{H_2}=0,2.22,4=4,48(l)\)
Đúng 4
Bình luận (1)
b) mHCl = 14,6 (g)
V H2 = 4,48 (l)
Giải thích các bước:
a) PTHH: Zn + 2HCl → ZnCl2 + H2↑
b) nZn = 13 : 65 = 0,2 mol
Theo PTHH: nHCl = 2.nZn = 0,4 mol
mHCl = 0,4 . 36,5 = 14,6(g)
c) nH2 = nZn = 0,2 mol
VH2 = 0,2 . 22,4 = 4,48 (l)
Đúng 1
Bình luận (2)
Hòa tan hoàn toàn một lượng bột sắt Fe vào dung dịch axit clohiđric HCl thu được V lít (đktc) khí hiđro H2 và dung dịch muối sắt (II) clorua FeCl2. Khối lượng muối FeCl2 tăng 7,1 gam so với khối lượng bột sắt Fe. Giá trị của V ứng với
A. 4,48
B. 1,68
C. 1,12
D. 2,24
Gọi \(n_{Fe}=x\left(mol\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
\(n_{FeCl_2}=n_{Fe}=x\left(mol\right)\)
Vì khối lượng muối FeCl2 tăng 7,1g so với khối lượng bột Fe
\(\Rightarrow127x-56x=7,1\\ \Rightarrow x=0,1\)
\(n_{H_2}=n_{Fe}=0,1\left(mol\right)\\ V_{H_2\left(ĐKTC\right)}=0,1.22,4=2,24\left(l\right)\)
Chọn D
Đúng 2
Bình luận (0)