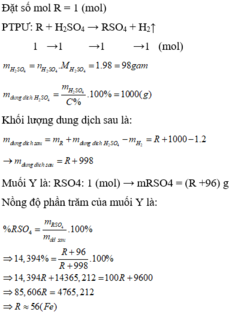Hòa tan 1 kim loại R có hóa trị không đổi trong 1 lượng dung dịch H2SO4 9,8% vừa đủ thu được dung dich muối 15,14%. Xác định kim loại R

Những câu hỏi liên quan
hòa tan một kim loai R có hóa trị không đổi trong một lượng dung dịch h2so4 9,8% vừa đủ thu được dd muối nồng độ 15,14%. Xác định kim loại R
Gọi CTHH oxit kim loại là \(RO\)
Giả sử có 1mol oxit pứ
\(RO+H_2SO_4\rightarrow RSO_4+H_2O\)
\(1-\rightarrow1---\rightarrow1\)
\(m_{ddH_2SO_4}=\dfrac{1.98}{4,9}\cdot100=2000\left(g\right)\\ m_{ddRSO_4}=1\left(R+16\right)+2000=2016+R\left(g\right)\\ C_{\%RSO_4}=\dfrac{1\left(R+96\right)}{2016+R}\cdot100=5,88\%\\ \Rightarrow R\approx24\left(g/mol\right)\)
Vậy R là Mg
Đúng 3
Bình luận (12)
hoà tan một muối cacbonat của kim loại R ( chưa biết hoá trị ) trong một lượng vừa đủ dung dịch H2SO4 12,25% thu được dung dịch muối sunfat của kim loại R có nồng độ 17,431%. Xác định kim loại R
tham khảo
Coi mdd H2SO4=100(gam)mdd H2SO4=100(gam)
nR2(SO4)n=nR2(CO3)n=nH2SO4n=0,1n(mol)nR2(SO4)n=nR2(CO3)n=nH2SO4n=0,1n(mol)
Sau phản ứng ,
mR2(SO4)n=0,1n(2R+96n)=0,2Rn+9,6(gam)mR2(SO4)n=0,1n(2R+96n)=0,2Rn+9,6(gam)
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn một kim loại R có hóa trị II bằng dung dịch
H
2
SO
4
9,8% (loãng) vừa đủ, sau phản ứng thu được dung dịch X chứa muối Y với nồng độ phần trăm là 14,394%. Kim loại R là: A. Mg. B. Fe. C. Zn. D. Cu.
Đọc tiếp
Hòa tan hoàn toàn một kim loại R có hóa trị II bằng dung dịch H 2 SO 4 9,8% (loãng) vừa đủ, sau phản ứng thu được dung dịch X chứa muối Y với nồng độ phần trăm là 14,394%. Kim loại R là:
A. Mg.
B. Fe.
C. Zn.
D. Cu.
hòa tan hoàn toàn b (g) oxit kim loại có hóa trị II bằng 1 lượng vừa đủ dung dịch H2SO4 15,8% thu được dung dịch muối có nồng độ 22,959% . Xác định tên oxit kim loại
CT oxit : MO
Đặt số mol oxit phản ứng là 1 mol
\(MO+H_2SO_4\rightarrow MSO_4+H_2O\)
\(m_{ddH_2SO_4}=\dfrac{1.98}{15,8\%}=620,25\left(g\right)\)
\(m_{ddsaupu}=620,25+M+16=M+636,25\left(g\right)\)
Ta có : \(C\%_{MSO_4}=\dfrac{M+96}{M+636,25}.100=22,959\)
=> M=65 (Zn)
=> Oxit kim loại : ZnO (Kẽm oxit)
Đúng 3
Bình luận (0)
cho 5,4g kim loại R có hóa trị n không đổi tác dụng vừa đủ vs V ml dung dịch H2SO4 loãng 24,5% ( KLR d= 1,08g/ml), sau phản ứng thu được dung dịch A và 6,72l khí H2 ở đktc. Xác định kim loại R, tính V và % khối lượng chất tan trong dung dịch A
Hòa tan 1 oxide kim loại hóa trị II bằng 1 lượng vừa đủ dung dịch H2SO4 10% thu được dung dịch muối có nồng độ 11,8%. Xác định công thức oxide.
\(MO+H_2SO_4->MSO_4+H_2O\\ m_{ddH_2SO_4}=100g\left(tự.chọn\right)\\ C\%_{sau}=\dfrac{11,8}{100}=\dfrac{\dfrac{100.0,1}{98}\left(M+96\right)}{\dfrac{100.0,1}{98}\left(M+16\right)+100}\\ M=24\left(Mg\right)\\ CT:MgO\)
Đúng 3
Bình luận (0)
Hòa tan 54 gam kim loại có hóa trị không đổi vào dung dịch H2SO4 10% vừa đủ thu được 50.4 lít H2 đktc và dung dịch B. Xác địnhtên kim loại và khối lượng dung dịch H2SO4 đã dùng
Xem chi tiết
\(n_{H_2}=\dfrac{50.4}{22.4}=2.25\left(mol\right)\)
\(2M+2nH_2SO_4\rightarrow M_2\left(SO_4\right)_n+nH_2\)
\(\dfrac{4.5}{n}.............................2.25\)
\(M_M=\dfrac{54}{\dfrac{4.5}{n}}=12n\)
\(BL:n=2\Rightarrow M=24\)
\(M:Mg\)
\(n_{H_2SO_4}=n_{H_2}=2.25\left(g\right)\)
\(m_{dd_{H_2SO_4}}=\dfrac{2.25\cdot98\cdot100}{10}=2205\left(g\right)\)
Đúng 2
Bình luận (1)
Giả sử kim loại cần tìm là A có hóa trị n không đổi.
Ta có: \(n_{H_2}=\dfrac{50,4}{22,4}=2,25\left(mol\right)\)
BT e, có: \(n_A=\dfrac{2,25.2}{n}=\dfrac{4,5}{n}\left(mol\right)\)
\(\Rightarrow M_A=\dfrac{54}{\dfrac{4,5}{n}}=12n\)
Với n = 1 ⇒ MA = 12 (loại)
Với n = 2 ⇒ MA = 24 (nhận)
Vậy: A là Magie (Mg).
BTNT H có: \(n_{H_2SO_4}=n_{H_2}=2,25\left(mol\right)\)
\(\Rightarrow m_{H_2SO_4}=2,25.98=220,5\left(g\right)\)
\(\Rightarrow m_{ddH_2SO_4}=\dfrac{220,5.100}{10}=2205\left(g\right)\)
Bạn tham khảo nhé!
Đúng 3
Bình luận (1)
hòa tan 4,9g hỗn hợp gồm Cu và kim loại R có hóa trị (II) vào dung dịch HCL vừa đủ. Sau phản ứng còn lại 3,2g chất rắn không tan, phần dung dịch còn lại đem đi cô cạn thì thu được 4,44g muối khan. Xác định kim loại R
3,2 gam chất rắn không tan là Cu => mCu = 3,2 (g)
=> mR = 4,9 - 3,2 = 1,7 (g)
Gọi hóa trị của R là n => \(n_R=\dfrac{1,7}{M_R}\)
PTHH: 2R + 2nHCl ---> 2RCln + nH2
\(\dfrac{1,7}{M_R}\)--------------->\(\dfrac{1,7}{M_R}\)
=> \(\dfrac{1,7}{M_R}=\dfrac{4,44}{M_R+35,5n}\)
=> MR = 22,025n (g/mol)
Không có giá trị của n nào thỏa mãn
=> Không có kim loại R nào thỏa mãn yêu cầu của bài ra
Đúng 2
Bình luận (0)