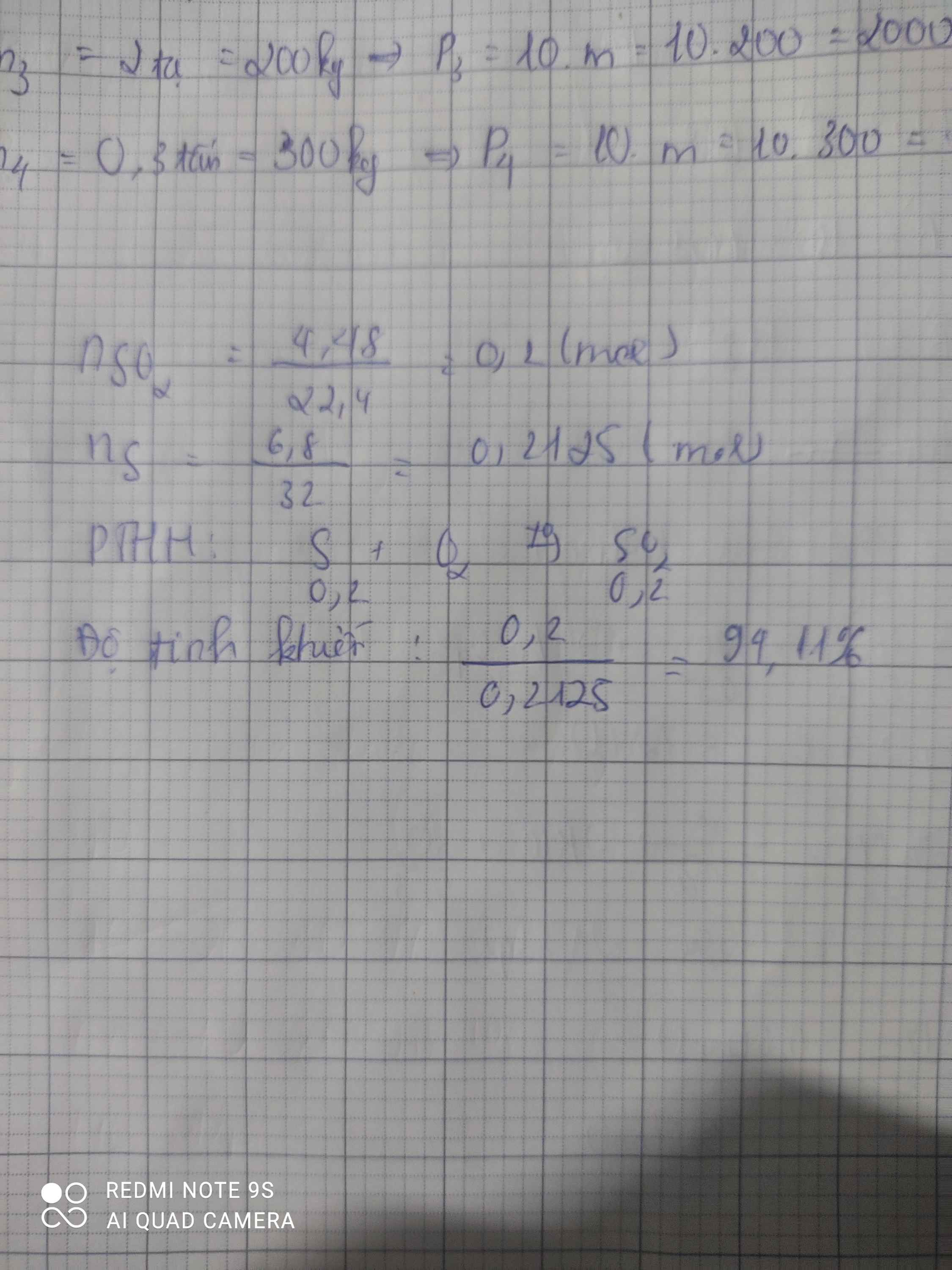Đốt cháy hết 24,11g P có lẫn tạp chất trong oxi tinh khiết thu được 49,7g P205 .Xác định độ tinh khiết của P.

Những câu hỏi liên quan
Đốt cháy hoàn toàn 14,11g P chứa tạp chất trong oxi tinh khiết,thu đc 49,7g P2O5. xác định độ tinh khiết của mẫu phot-pho
đốt cháy 6,8g 1 mẫu lưu huỳnh không tinh khiết trong khí O2 dư người ta thu được 4,48l khí SO2 ở đktc.Hãy xác định độ tinh khiết của mẫu s
\(n_{SO_2}=\dfrac{4.48}{22,4}=0,2\left(mol\right)\)
PTHH : S + O2 ---to---> SO2
0,2 0,2
\(m_S=0,2.32=6,4\left(g\right)\)
Độ tinh khiết của lưu huỳnh là
\(\dfrac{6,4}{6,8}.100\%=94,11\%\)
Đúng 1
Bình luận (0)
S+O2-to>SO2
0,2----------0,2
n SO2=\(\dfrac{4,48}{22,4}\)=0,2 mol
=>m S=0,2.32=6,4g
=>độ tinh khiết là \(\dfrac{6,4}{6,8}\).100=94,11%
Đúng 1
Bình luận (0)
Trong dòng khí H2 thường có lẫn tạp chất là O2 làm thế nào thử độ tinh khiết của khí H2?Làm thế nào để thu đc H2 tinh khiết hơn?
# Cách thử độ tinh khiết của H2: Để tránh hiện tượng nổ mạnh, trước khi thử nghiệm người ta sẽ thử độ tinh khiết của H2H2 bằng cách thu H2 vào ống nghiệm nhỏ rồi đốt ở miệng ống nghiệm. Nếu H2 tinh khiết thì sẽ nghe tiếng nổ nhỏ, còn nếu H2 có lẫn không khí thì có tiếng nổ mạnh.
Đúng 0
Bình luận (1)
Đốt cháy 15 gam một mẫu cacbon không tinh khiết trong khí oxi dư, thu được 17,92 lít khí CO2 (ở đktc). Độ tinh khiết của mẫu cacbon trên là:
Đọc tiếp
Đốt cháy 15 gam một mẫu cacbon không tinh khiết trong khí oxi dư, thu được 17,92 lít khí CO2 (ở đktc). Độ tinh khiết của mẫu cacbon trên là:
\(n_{CO_2}=\dfrac{17,92}{22,4}=0,8\left(mol\right)\)
PT: \(C+O_2\underrightarrow{t^o}CO_2\)
Theo PT: \(n_C=n_{CO_2}=0,8\left(mol\right)\)
\(\Rightarrow m_C=0,8.12=9,6\left(g\right)\)
Độ tinh khiết của mẫu C là: \(\dfrac{9,6}{15}.100\%=64\%\)
Đúng 2
Bình luận (0)
đốt cháy 21 gam 1 mẫu sắt không tinh khiết trong oxi dư người ta thu được 23,2 gam oxit sắt từ Fe3O4. tính độ tinh khiết của mẫu sắt đã dùng
PTHH: 3Fe + 2O2 → Fe3O4
Số mol của Fe3O4 là: 23,2 : 232 = 0,1 (mol)
Số mol của Fe là: 0,1 . 3 = 0,3 (mol)
Khối lượng Fe nguyên chất tham gia phản ứng là:
0,3 . 56 = 16,8 gam
% tinh khiết của mẩu sắt là: (16,8:21).100% = 80%
Đúng 0
Bình luận (1)
Câu 4 (4 điểm): Hòa 99,8 g CuSO4 vào 164 g H2O. Làm lạnh dung dịch tới 100C thu được 30 g tinh thể CuSO4. 5H2O. Biết độ tan của CuSO4 khan ở 100C là 17,4 g.
Xác định xem CuSO4. 5H2O ban đầu có lẫn tạp chất hay tinh khiết? Tính khối lượng tạp chất nếu có.
Đốt cháy 3,25g một mẫu lưu huỳnh không tinh khiết trong không khí có oxi dư, người ta thu được 2,24 lit khí sunfuro(dktc). Bằng cách nào ta có thể tính được nồng độ tinh khiết của mẫu lưu huỳnh đã dùng?
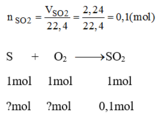
Theo pt: 1 mol S tham gia phản ứng sinh ra 1 mol S O 2
Số mol của lưu huỳnh tham gia phản ứng:
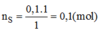
Khối lượng của lưu huỳnh tinh khiết: m S = n S . M S =0,1.32=3,2(g)
Độ tinh khiết của mẫu lưu huỳnh:
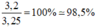
Đúng 0
Bình luận (0)
đốt cháy 21 gam 1 mẫu sắt không tinh khiết trong oxi dư người ta thu được 23,2 gam oxit sắt từ Fe3O4. tính độ tinh khiết của mẫu sắt đã dùng
giúp mình nhá
PTHH: 3Fe + 2O2 → Fe3O4
Số mol của Fe3O4 là: 23,2 : 232 = 0,1 (mol)
Số mol của Fe là: 0,1 . 3 = 0,3 (mol)
Khối lượng Fe nguyên chất tham gia phản ứng là:
0,3 . 56 = 16,8 gam
% tinh khiết của mẩu sắt là: (16,8:21).100% = 80%
Đúng 0
Bình luận (1)
Ta có PT:
3Fe + 2O2 ---> Fe3O4
n\(Fe_3O_4\)=\(\frac{23,2}{232}\)=0,1(mol)
Theo PT ta có:
nFe tinh khiết = 3n\(Fe_3O_4\)= 3.0,1=0,3(mol)
mFe tinh khiết = 0,3.56 = 16,8(g)
Độ tinh khiết của sắt đã dùng
= \(\frac{16,8}{21}\).100%=80%
đốt cháy 4g bột than (chứa C và tạp chất rắn trơ ko cháy ) thu đc 6,72 lít khí CO2 ở đktc.tính độ tinh khiết của than
\(PTHH:C+O_2\underrightarrow{t^o}CO_2\)
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
Từ PTHH ta có
Đốt 1 mol C thì sinh ra 1 mol CO2
=> Đốt 0,3 mol C thì sinh ra 0,3 mol CO2
\(\Rightarrow m_C=0,3.12=3,6\left(g\right)\)
\(\Rightarrow\%C=\dfrac{3,6}{4}=90\%\)
Vậy độ tinh khiết của than là 90%
Đúng 1
Bình luận (0)