A là dung dịch H2SO4 0,2M, B là dung dịch H2SO4 0,5M. Trộn A và B theo tỉ lệ thể tích VA : VB = 2:3 được dung dich C.
a) Xác đinh Nồng độ mol của C
b) Phải trộn A và B theo tỉ lệ thể tích như thế nào để được dung dịch H2SO4 0,3M
Dung dịch H2 SO4 có nồng độ 0,2M (dung dịch A) dung dịch H2 SO4 có nồng độ 0,5M (dung dịch B).a) nếu Trộn A và B theo tỉ lệ thể tích Va: Vb = 2 : 3 được dung dịch C Hãy xác định nồng độ mol của dung dịchC. b) Phải trộn A và B theo tỉ lệ nào về thể tích để được dung dịch H2SO4 có nồng độ 0,3M.
Giải hộ E...^_^
a)
Coi V A = 2(lít) => V B = 3(lít)
Trong dung dịch C, ta có :
V C = V A + V B = 2 + 3 = 5(lít)
n H2SO4 = n H2SO4(trong A) + n H2SO4(trong B) = 2.0,2 + 3.0,5 = 1,9(mol)
Suy ra :
CM H2SO4 = 1,9/5 = 0,38M
b)
Sau khi trộn :
V C = V A + V B
n H2SO4 = 0,2V A + 0,5V B
Suy ra :
CM H2SO4 = (0,2V A + 0,5V B)/(V A + V B ) = 0,3
<=> 0,2V A + 0,5V B = 0,3V A + 0,3V B
<=> 0,1V A = 0,2V B
<=> V A / V B = 0,2/0,1 = 2 / 1
Vậy phải trộn A và B theo tỉ lệ 2 : 1 về thể tích
\(GS:\)
\(V_A=2\left(l\right),V_B=3\left(l\right)\)
\(n_{H_2SO_4\left(1\right)}=0.2\cdot2=0.4\left(mol\right)\)
\(n_{H_2SO_4\left(2\right)}=0.5\cdot3=1.5\left(mol\right)\)
\(C_{M_{H_2SO_4}}=\dfrac{0.4+1.5}{2+3}=0.38\left(M\right)\)
\(b.\)
\(V_{H_2SO_4\left(1\right)}=a\left(l\right)\)
\(V_{H_2SO_4\left(2\right)}=b\left(l\right)\)
\(C_{M_{H_2SO_4}}=\dfrac{0.2a+0.5b}{a+b}=0.3\left(M\right)\)
\(\Leftrightarrow0.2a+0.5b-0.3a-0.3b=0\)
\(\Leftrightarrow0.2b=0.1a\)
\(\Leftrightarrow\dfrac{a}{b}=\dfrac{0.2}{0.1}=2\)
A là dung dịch H 2 S O 4 có nồng độ 0,2M. B là dung dịch H 2 S O 4 có nồng độ 0,5M.
Nếu trộn A và B theo tỉ lệ thể tích V A : V B = 2:3 được dung dịch C. Hãy xác định nồng độ mol của dung dịch C.
Ta có: V A : V B = 2:3
Số mol H 2 S O 4 có trong 2V (l) dung dịch A:
n H 2 S O 4 = C M . V A = 0,2 . 2V = 0,4V (mol)
Số mol H 2 S O 4 có trong 3V (l) dung dịch B:
n H 2 S O 4 = C M . V B = 0,5 . 3V = 1,5V (mol)
Nồng độ mol của dung dịch H 2 S O 4 sau khi pha trộn:
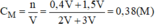
Vậy nồng độ mol của dung dịch C là 0,38M.
A là dung dịch H2SO4 0.2M. B là dung dịch H2SO4 0.5M
a) nếu trộn A và B theo tỉ lệ thể tích Va: Vb= 2:3 thì được dung dịch C có nồng độ bao nhiêu?
b) nếu phải trộn A và B theo tỉ lệ thể tích là bao nhiêu để được dung dịch C có nồng độ là bao nhiêu?
\(a) V_A = 2(lít) \to V_B = 3(lít)\\ \Rightarrow V_{dd} = 2 + 3 = 5(lít)\\ n_{H_2SO_4\ trong\ C} = 0,2.2 + 0,5.3 = 1,9(mol)\\ C_{M_{H_2SO_4}} = \dfrac{1,9}{5} = 0,38M\)
A là dung dịch H 2 S O 4 có nồng độ 0,2M. B là dung dịch H 2 S O 4 có nồng độ 0,5M.
Phải trộn A và B theo tỉ lệ nào về thể tích để được dung dịch H 2 S O 4 có nồng độ 0,3M.
Pha chế dung dịch H 2 S O 4 0,3M.
Gọi x(l) là thể tích của dung dịch axit A.
y(l) là thể tích của dung dịch B.
n H 2 S O 4 ( A ) = C M . V A = 0,2 . x (mol)
n H 2 S O 4 ( B ) = C M . V B = 0,5 . y (mol)
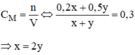
Vậy: ta phải trộn 2 thể tích dung dịch axit A với 1 thể tích dung dịch axit B, ta sẽ được dung dịch H 2 S O 4 có C M = 0,3M.
Câu 5 (2,0 điểm): A là dung dịch H2SO4 0,2M, B là dung dịch H2SO4 0,5M. Phải trộn A và B theo tỉ lệ thể tích như thế nào để được dung dịch H2SO4 0,3M
Đặt a,b lần lượt là thể tích của ddA và ddB
\(\Rightarrow0,2a+0,5b=0,3.\left(a+b\right)\\ \Leftrightarrow0,3a-0,2a=0,5b-0,3b\\ \Leftrightarrow0,1a=0,2b\\ \Leftrightarrow\dfrac{a}{b}=\dfrac{0,2}{0,1}=\dfrac{2}{1}\)
=> Trộn theo tỉ lệ thể tích ddA:ddB=2:1
Bài 3: Một dung dịch CuSO4 có KL riêng D = 1,206 g/ml . Từ 165,84 ml dung dịch này, người ta thu đk 56,25 kết tinh CuSO4. 5H2O. Xác định nồng độ & của dung dịch CUSO4 đã dùng.
Bài 4
A là dung dịch H2SO4 0,2M , B là dung dịch H2SO4 0,5M
a) Trộn A và B theo tỉ lệ thể tích VA : Vb = 2: 3 được dung dịch C. Xác định nồng độ mol của C
b) Phải trộn A và B theo tỉ lệ thể tích ntn để được dung dịch H2SO4 0,3M ?
A là dung dịch H2SO4 có nồng độ 0,2M.
B là dung dịch H2SO4 có nồng độ 0,5M.
a) Nếu trôn A và B theo tỉ lệ thể tích V A : V B = 2 : 3 được dd C. Tính nồng độ mol của dd C.
b) Phải trộn A và B theo tỉ lệ nào về thể tích để được dd H2SO4 có nồng độ 0,3M?
a) Ta có: VA:VB = 2:3
Số mol H2SO4 có trong 2V dung dịch A:
Số mol H2SO4 có trong 3V dung dịch B:
Nồng độ mol của dung dịch H2SO4 sau khi pha trộn:
Vậy nồng độ mol của dung dịch C là 0,38M.
b) Pha chế dung dịch H2SO4 0,3M.
Gọi x(ml) là thể tích của dung dịch axit A.
y(ml) là thể tích của dung dịch B.
→ x = 2y . Vậy nêu y = 1 và x = 2.
Vậy ta phải trộn 2 thể tích dung dịch axit A với 1 thể tích dung dịch axit B, ta sẽ được dung dịch H2SO4 có CM = 0,3M.
Có 2 dung dịch H2SO4 (A) và (B); CM(A) = 5CM(B)
a) Trộn A và B theo tỉ lệ thể tích là 3 : 7 thì thu được dung dịch C có nồng độ 1,672 M. Hãy tính nồng độ mol của A và B.
b) Lấy 100ml dung dịch b (có dư) cho phản ứng với 50ml dung dịch BaCl2, sau khi BaSO4 kết tủa hoàn toàn, dung dịch sau phản ứng có tính axit và khối lượng axit trong dung dịch này là 12,3856 gam (dung dịch D). Thu toàn bộ dung dịch D cho tác dụng tiếp với 177,232 gam dung dịch Na2CO3 10% thì thấy phản ứng xảy ra vừa đủ. Hãy tính nồng độ mol của dung dịch H2SO4; HCl; BaCl2 và khối lượng BaSO4 tạo thành.
Trộn dung dịch A chứa NaOH và dung dịch B chứa Ba(OH)2 theo tỉ lệ thể tích bằng nhau thu được dung dịch C. Trung hoà 100 ml dung dịch C cần dùng hết 35 ml dung dịch H2SO4 2M và thu được 9,32 gam kết tủa. Tính nồng độ mol của các dung dịch A và B. Cần phải trộn bao nhiêu ml dung dịch B với 20 ml dung dịch A để thu được dung dịch D có thể hoà tan vừa hết 20,4 gam bột Al2O3
Gọi \(\left\{{}\begin{matrix}C_{M\left(A\right)}=aM\\C_{M\left(B\right)}=bM\end{matrix}\right.\)
Giả sử trộn 50ml dd A với 50ml dd B để thu được 100ml dd C
=> \(\left\{{}\begin{matrix}n_{NaOH}=0,05a\left(mol\right)\\n_{Ba\left(OH\right)_2}=0,05b\left(mol\right)\end{matrix}\right.\)
\(n_{BaSO_4}=\dfrac{9,32}{233}=0,04\left(mol\right)\)
nH2SO4 = 0,035.2 = 0,07 (mol)
PTHH: Ba(OH)2 + H2SO4 --> BaSO4 + 2H2O
0,04<----0,04<-------0,04
2NaOH + H2SO4 --> Na2SO4 + 2H2O
0,06<----0,03
=> \(\left\{{}\begin{matrix}0,05a=0,06\\0,05b=0,04\end{matrix}\right.\)
=> a = 1,2; b = 0,8
20 ml dd A chứa nNaOH = 0,02.1,2 = 0,024 (mol)
\(n_{Al_2O_3}=\dfrac{20,4}{102}=0,2\left(mol\right)\)
PTHH: 2NaOH + Al2O3 --> 2NaAlO2 + H2O
0,024-->0,012
Ba(OH)2 + Al2O3 --> Ba(AlO2)2 + H2O
0,188<---0,188
=> \(V_{dd.B}=\dfrac{0,188}{0,8}=0,235\left(l\right)=235\left(ml\right)\)