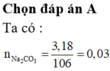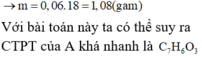Đốt cháy 4,6g A có Ct CXHyO cần 6,72 lít 02 (đktc) thu đc 8,8g CO2 và 1 lượng H2O .Tính khối lượn H2O và CTPT

Những câu hỏi liên quan
2. Đốt cháy hoàn toàn 7,4g este X đơn chức thu đc 6,72 lít khí CO2(đktc) và 5,4g H2O. a) Xác định CTPT của X b) Đun 7,4g X trong dd NaOH vừa đủ đến khi pư hoàn toàn thu đc 3,2g ancol Y và 1 lượng muối Z. Viết công thức cấu tạo của X và tính khối lượng Z?
a) Gọi công thức phân tử của este X là CxHyOz.
a ax a.
y\2 (mol)Ta có :
(mol) ;
(mol)
=> mO = 7,4 – 0,3.12 -0,3.2 = 3,2g ; nO = 0,2 (mol)
=> x : y : z = 3 : 6 : 2
Vì X là este đơn chức nên công thức phân tử của X là C3H6O2
b)
nX = 0,1 mol, nY = 0,1 mol.
MY = 32g/mol => CTPT của Y : CH3OH
CTPT của X : CH3COOCH3.
Đúng 1
Bình luận (0)
52. Đốt cháy hoàn toàn một hợp chất hữu cơ A có dạng CxHyO thu đc sản phẩm cháy chỉ gồm CO2 và H2O với tỉ lệ khối lượng tương ứng là 44:27. CTPT của A là?
Đốt cháy hoàn toàn a(g) HCHC A cần vừa đủ 6,72 lít O2 thu đc 13,2g CO2 và 5,4g H2O.
a) Tính a và % khối lượng các nguyên tố trong A
b) Biết tỉ khối hơi của A so với không khí cân bằng 1,0345. Xác định CTPT của A
2. Đốt cháy hoàn toàn 1,72g một chất hữu cơ A chứa C,H,N thì thu dc 3,52g CO2; 0,1mol H2O và 448cm^3 khí N2(đkc). Khi hóa hơi 1,29g chất A thì có thể bằng đúng thể tích 0,96g oxi cùng đk.
Xem chi tiết
A + O2 --> CO2 + H2O
nCO2 = \(\dfrac{13,2}{44}\)= 0,3 mol = nC
nH2O = \(\dfrac{5,4}{18}\)= 0,3 mol => nH = 0,3 .2 = 0,6 mol
nO2 = 6,72/22,4 = 0,3 mol
Áp dụng định luật BTKL : mA + mO2 = mCO2 + mH2O
=> mA = 13,2 + 5,4 - 0,3.32 = 9 gam
mC + mH = 0,3.12 + 0,6 = 4,2 < 9
=> Trong A có C ; H và O
mO = mA - mC - mH = 4,8 gam
%mC = \(\dfrac{0,3.12}{9}\).100% = 40% %mH = \(\dfrac{0,6}{9}\).100% = 6,67%
=>%mO = 100 - 40 - 6,67 = 53,33%
b) nO = \(\dfrac{4,8}{16}\)= 0,3 mol
Gọi CTĐGN của A là CxHyOz => x : y : z = nC : nH : nO = 1:2:1
=> CTPT của A có dạng (CH2O)n
MA = 1,0345.29 = 30 g/mol
=> n = 1 và CTPT của A là CH2O
Đúng 2
Bình luận (0)
Bài 2 :
nC = nCO2 = \(\dfrac{3,52}{44}\)= 0,08 mol ; nN = 2nN2 = \(\dfrac{0,448.2}{22,4}\)= 0,04 mol
nH = 2nH2O = 0,2 mol
Gọi CTĐGN của A là CxHyNt
=> x : y : t = nC : nH : nN = 2 : 5 : 1
CTPT của A có dạng (C2H5N)n
mà 1,29 gam A có thể tích = 0,96 gam oxi ở cùng đk
=> 1,29 gam A có số mol = 0,96 gam oxi ở cùng đk = \(\dfrac{0,96}{32}\)=0,03 mol
=> MA = \(\dfrac{1,29}{0,03}\)= 43 g/mol
=> (12.2 + 5 + 14)n = 43 <=> n = 1 và A có CTPT là C2H5N
Đúng 2
Bình luận (0)
đốt cháy hoàn toàn 4,6 gam chất A cần vừa đủ 6,72 lít khí Oxi (Đktc) thu được CO2 và H2O có tỉ lệ khối lượng là 44:27 . a) A tạo bởi những nguyên tố nào? b) tìm CT ĐG của A? c) Tìm CTHH của A biết dA/H2 là 23.
Ta có: \(n_{O_2}=0,3\left(mol\right)\)
Giả sử: \(\left\{{}\begin{matrix}n_{CO_2}=x\left(mol\right)\\n_{H_2O}=y\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\dfrac{44x}{18y}=\dfrac{44}{27}\Leftrightarrow3x-2y=0\left(1\right)\)
Theo ĐLBT KL, có: mA + mO2 = mCO2 + mH2O.
\(\Rightarrow44x+18y=4,6+0,3.32\left(2\right)\)
Từ (1) và (2) \(\Rightarrow\left\{{}\begin{matrix}x=n_{CO_2}=0,2\left(mol\right)\\y=n_{H_2O}=0,3\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_C=0,2\left(mol\right)\\n_H=0,6\left(mol\right)\end{matrix}\right.\)
a, Vì đốt cháy A tạo CO2 và H2O nên A chắc chắn có C và H, có thể có O.
BTNT C và H, có: mC + mH = 0,2.12 + 0,6.1 = 3 (g) < mA.
Vậy: A gồm nguyên tố: C, H và O.
b, Ta có: mO = 4,6 - 3 = 1,6 (g)
\(\Rightarrow n_O=\dfrac{1,6}{16}=0,1\left(mol\right)\)
Giả sử CTPT của A là CxHyOz (x, y, z ∈ Z+)
⇒ x : y : z = 0,2 : 0,6 : 0,1 = 2 : 6 : 1
Vậy: CTĐGN của A là C2H6O.
c, Vì: dA/H2 = 23
⇒ MA = 23.2 = 46 (đvC)
Từ p/b, ta có A có dạng (C2H6O)n.
\(\Rightarrow n=\dfrac{46}{12.2+6+16}=1\)
Vậy: A là C2H6O.
Bạn tham khảo nhé!
Đúng 3
Bình luận (0)
a) BTKL mX+mO2=mCO2+mH2O
=>mCO2+mH2O=4,6+6,72/22,4.32=14,2g
b)ĐẶT nCO2=2x nH2O=3x
=>44.2x+18.3x=14,2 =>x=0,1
=>nC=nCO2=0,2 mol
nH2O=0,3 =>nH=2nH2O=2.0,3=0,6 mol
ta co 0,2.12+0,6.1=3g <4,6 => X có oxi =>mO=4,6-3=1,6g=>nO=0,1
gọi CT của X là CxHyOz
x:y:z=0,2:0,6:0,1=2:6:1
vậy CT của X là C2H6O
Đúng 1
Bình luận (0)
Chất hữu cơ A chỉ chứa C, H, O có CTPT trùng CT đơn giản nhất. Cho 2,76 gam A tác dụng với một lượng vừa đủ dung dịch NaOH, chưng khô thì phần bay hơi chỉ có H2O, phần chất rắn khan chứa 2 muối có khối lượng 4,44 gam. Đốt cháy hoàn toàn hai muối này được 3,18 gam Na2CO3; 2,464 lít CO2 (đktc) và 0,9 gam H2O. Nếu đốt cháy 2,76 gam A thì khối lượng H2O thu được là: A. 1,08g. B. 1,2 gam. C. 0,36 gam. D. 0,9 gam.
Đọc tiếp
Chất hữu cơ A chỉ chứa C, H, O có CTPT trùng CT đơn giản nhất. Cho 2,76 gam A tác dụng với một lượng vừa đủ dung dịch NaOH, chưng khô thì phần bay hơi chỉ có H2O, phần chất rắn khan chứa 2 muối có khối lượng 4,44 gam. Đốt cháy hoàn toàn hai muối này được 3,18 gam Na2CO3; 2,464 lít CO2 (đktc) và 0,9 gam H2O. Nếu đốt cháy 2,76 gam A thì khối lượng H2O thu được là:
A. 1,08g.
B. 1,2 gam.
C. 0,36 gam.
D. 0,9 gam.
Đốt cháy hoàn toàn 6g hc có công thức CxxHyO2 cần 4,48 lít O2 (đktc) thu đc 8,8g CO2 và 3,6gH2O. Tìm Ctpt
\(n_{CO_2}=\dfrac{8.8}{44}=0.2\left(mol\right)\)
\(n_{H_2O}=\dfrac{3.6}{18}=0.2\left(mol\right)\)
\(m_O=6-0.2\cdot12-0.2\cdot2=3.2\left(g\right)\)
\(n_O=\dfrac{3.2}{16}=0.2\left(mol\right)\)
\(\Rightarrow n_A=\dfrac{0.2}{2}=0.1\left(mol\right)\)
Số nguyên tử C : \(x=\dfrac{0.2}{0.1}=2\)
Số nguyên tử H : \(y=\dfrac{0.2\cdot2}{0.1}=4\)
\(CT:C_2H_4O_2\)
Đúng 1
Bình luận (0)
đốt cháy hoàn toàn 6g hợp chất hữu cơ A thu đc 4,48l CO2(đktc) và 3,6g h2o a: tính CTPT của A biết MA= 60g/mol b: dẫn toàn bộ lượng CO2 qua dd Ca(OH)2 tính khối lượng khí thu đc
a.Bảo toàn C: \(n_C=n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\)
Bảo toàn H: \(n_H=2.n_{H_2O}=2.\dfrac{3,6}{18}=0,4mol\)
\(n_O=\dfrac{6-\left(0,2.12+0,4.1\right)}{16}=0,2mol\)
=> A gồm C,H và O
\(CTPT:C_xH_yO_z\)
\(x:y:z=0,2:0,4:0,2=2:4:2\)
\(CTĐG:\left(C_2H_4O_2\right)n=60\)
\(\Leftrightarrow n=1\)
Vậy CTPT A: \(C_2H_4O_2\) hay \(CH_3COOH\)
b.\(n_{CO_2}=\dfrac{4,48}{22,4}=0,2mol\)
\(Ca\left(OH\right)_2+CO_2\rightarrow CaCO_3+H_2O\)
0,2 0,2 ( mol )
\(m_{CaCO_3}=0,2.100=20g\)
Đúng 1
Bình luận (1)
Đốt cháy hoàn toàn một hiđrocacbon thu được 6,72 lít co2 (đktc) và 3,6g h2o. Xác định CTPT và viết CTCT
Giúp em với ạ
\(n_{CO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
\(n_{H_2O}=\dfrac{3,6}{18}=0,2\left(mol\right)\)
Có: nCO2 > nH2O → Hidrocacbon là ankin.
⇒ n hidrocacbon = nCO2 - nH2O = 0,1 (mol)
Gọi CTPT của hidrocacbon là CnH2n-2
\(\Rightarrow n=\dfrac{0,3}{0,1}=3\)
→ CTPT là C3H4.
CTCT: \(CH\equiv C-CH_3\)
Đúng 1
Bình luận (0)
Đốt cháy hoàn toàn 7,4 gam este X, thu được 6,72 lít CO2 (ở đktc) và 5,4 gam H2O. Tìm CTPT của X.