Cho 5,4g nhôm phản ứng với 11,2l Oxit
a/ Tính khối lượng nhôm oxit tạo thành
b/ Sắt và Oxit chất nào phản ứng còn dư và dư bao nhiêu gam
Cho 10,8g nhôm tác dụng với 13,44lit khí oxi (đktc) a. Viết PTHH b. Chất nào còn dư sau phản ứng và dư bao nhiêu gam (lít)? c. Khối lượng nhôm oxit tạo thành là bao nhiêu?
\(a,n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\\ n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\)
PTHH: 4Al + 3O2 --to--> 2Al2O3
b, LTL: \(\dfrac{0,4}{4}>\dfrac{0,6}{3}\) => O2 dư
Theo pthh: \(\left\{{}\begin{matrix}n_{O_2\left(pư\right)}=\dfrac{3}{4}n_{Al}=\dfrac{3}{4}.0,4=0,3\left(mol\right)\\n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=\dfrac{1}{2}.0,4=0,2\left(mol\right)\end{matrix}\right.\)
=> VO2 (dư) = (0,6 - 0,3).22,4 = 6,72 (l)
c, mAl2O3 = 0,2.102 = 20,4 (g)
\(n_{Al}=\dfrac{10,8}{17}=0,4\left(mol\right)\\ n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\\ pthh:4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
\(LTL:\dfrac{0,4}{4}< \dfrac{0,6}{3}\)
=> O2 dư P hết
\(n_{Al_2O_3}=\dfrac{1}{2}n_{Al}=0,2\left(mol\right)\\ m_{Al_2O_3}=0,2.102=20,4g\)
\(n_{Al}=\dfrac{10,8}{27}=0,4mol\)
\(n_{O_2}=\dfrac{13,44}{22,4}=0,6mol\)
\(4Al+3O_2\rightarrow\left(t^o\right)2Al_2O_3\)
Xét: \(\dfrac{0,4}{4}\) < \(\dfrac{0,6}{3}\) ( mol )
0,4 0,3 0,2 ( mol )
Chất dư là O2
\(m_{O_2\left(dư\right)}=\left(0,6-0,3\right).32=9,6g\)
\(m_{Al_2O_3}=0,2.102=20,4g\)
Cho 12.395l khí Oxy cho tác dụng với 10.8g Nhôm sau phản ứng thu được Nhôm oxit AI2O3
a) Chất nào còn dư sau phản ứng và dư bao nhiêu g ?
b) Tính khối lượng sản phẩm thu được sau phản ứng
12,395l ở đk nào vậy em?
pthhL
\(3O_2+4Al\underrightarrow{t^o}2Al_2O_3\)
\(nO_2=12,395:24,9=0,5\left(mol\right)\)
\(nAl=\dfrac{10,8}{27}=0,4\left(mol\right)\)
Xét tỉ lê:
\(\dfrac{nO_2}{3}>\dfrac{nAl}{4}\)
=> Oxy dư và dư: \(mO_{2dư}=0,06.32=2g\)
b, tính theo pthh vì nO2 dư nên lấy số mol của Al
=> \(nAl_2O_3=\dfrac{2}{4}.0,4=0,2\left(mol\right)\)
\(\Rightarrow mAl_2O_3=0,2.102=20,4\left(g\right)\)
Cho 58,5 gam nhôm hidroxit tác dụng với 49 gam dd axit sunfuric, sau phản ứng thu
được nhôm sufat và nước.
a. Viết PTHH
b. Sau phản ứng chất nào còn dư ? Khối lượng dư là bao nhiêu gam?
c. Tính khối lượng nhôm sunfat tạo thành.
a. PTHH: 2Al(OH)3 + 3H2SO4 ---> Al2(SO4)3 + 6H2O
b. Ta có: \(n_{Al\left(OH\right)_3}=\dfrac{58,5}{78}=0,75\left(mol\right)\)
\(n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\)
Ta thấy: \(\dfrac{0,75}{2}>\dfrac{0,5}{3}\)
Vậy \(Al\left(OH\right)_3\) dư.
\(m_{dư}=0,75.78-98.0,5=9,5\left(g\right)\)
c. Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{3}.n_{H_2SO_4}=\dfrac{1}{3}.0,5=\dfrac{1}{6}\left(mol\right)\)
=> \(m_{Al_2\left(SO_4\right)_3}=\dfrac{1}{6}.342=57\left(g\right)\)
Cho 58,5 gam nhôm hidroxit tác dụng với 49 gam dd axit sunfuric, sau phản ứng thu
được nhôm sufat và nước.
a. Viết PTHH
b. Sau phản ứng chất nào còn dư ? Khối lượng dư là bao nhiêu gam?
c. Tính khối lượng nhôm sunfat tạo thành.
a, \(n_{Al\left(OH\right)_3}=\dfrac{58,5}{78}=0,75\left(mol\right);n_{H_2SO_4}=\dfrac{49}{98}=0,5\left(mol\right)\)
PTHH: 2Al(OH)3 + 3H2SO4 → Al2(SO4)3 + 6H2O
Mol: \(\dfrac{1}{3}\) 0,5 \(\dfrac{1}{6}\)
b, Ta có: \(\dfrac{0,75}{2}>\dfrac{0,5}{3}\) ⇒ Al(OH)3 dư, H2SO4 hết
⇒ \(m_{Al\left(OH\right)_3}=\left(0,75-\dfrac{1}{3}\right).78=32,5\left(g\right)\)
c, \(m_{Al_2\left(SO_4\right)_3}=\dfrac{1}{6}.342=57\left(g\right)\)
Ta có: \(n_{Al\left(OH\right)_3}=\dfrac{58,5}{78}=0,75\left(mol\right)\)
a. PTHH: 2Al(OH)3 + 3H2SO4 ---> Al2(SO4)3 + 6H2O
b. Không có chất dư (hoặc có thể bn cho sai 49(g) dung dịch là 49(g) H2SO4)
c. Theo PT: \(n_{Al_2\left(SO_4\right)_3}=\dfrac{1}{2}.n_{Al\left(OH\right)_3}=\dfrac{1}{2}.0,75=0,375\left(mol\right)\)
=> \(m_{Al_2\left(SO_4\right)_3}=0,375.342=128,25\left(g\right)\)
1. Cho 32,4 gam kim loại nhôm phản ứng với 21,504 lít khí oxi (đktc).
a. Tính khối lượng Al2O3 tạo thành.
b. Tính khối lượng chất còn dư trong phản ứng.
2. Cho 12,15 gam nhôm và một dung dịch có chứa 54 gam CuSO4.
a. Chất nào dư sau phản ứng và dư bao nhiêu gam?
b. Lọc bỏ chất rắn rồi đem cô cạn dung dịch thì thu được bao nhiêu gam muối khan?
3. Nhiệt phân 29,4 gam kali clorat
a. Tính số milit khí oxi thu được.
b. Nếu đốt 50,4 gam sắt trong lọ đựng lượng khí oxi trên, tính khối lượng sản phẩn thu được?
c. Lấy hết Fe3O4 trên tác dụng với lượng dư Hcl theo sơ đồ sau:
Fe3O4 + HCl → FeCl2 + FeCl3 + H2O
Tính tổng khối lượng muối khan thu được sau khi cô cạn dụng dịch sau.
4. Cho 8,1 gam nhôm tác dụng với dung dịch có chứa 21,9 gam HCl.
a. Sau phản ứng chất nào còn dư, dư bao nhiêu gam?
b. Tính khối lượng AlCl3 thu được.
c. Khí sinh ra có thể khử được bao nhiêu gam CuO và thu được bao nhiêu gam Cu?
1. PTHH: 4Al + 3O2 ---> 2Al2O3
1,2 mol 0,9 mol 0,6 mol
+ Số mol của Al:
nAl = m/M = 32,4/27 = 1,2 (mol)
+ Số mol của O2:
nO2 = V/22,4 = 21,504/22,4 = 0,96 (mol)
a. + Số mol của Al2O3:
nAl2O3 = 1,2.2/4 = 0,6 (mol)
+ Khối lượng của Al2O3:
mAl2O3 = n.M = 0,6.102 = 61,2 (g)
Vậy: khối lượng của Al2O3 là 61,2 g
b. Tỉ lệ: Al O2
nAl/4 nO2/3
1,2/4 0,96/3
0,3 < 0,32
=> O2 dư; Al hết
+ Số mol phản ứng của O2:
nO2pư = 1,2.3/4 = 0,9 (mol)
+ Số mol dư của O2:
nO2dư = nO2 - nO2pư = 0,96 - 0,9 = 0,06 (mol)
+ Khối lượng dư của O2:
mO2dư = nO2dư . MO2 = 0,06 . 32 = 1,92 (g)
Vậy: chất còn dư trong phản ứng là O2 và khối lượng dư là 1,92 g
Note: có gì không rõ trong bài làm thì hỏi mình nha
1. Cho 32,4 gam kim loại nhôm phản ứng với 21,504 lít khí oxi (đktc).
a. Tính khối lượng Al2O3 tạo thành.
b. Tính khối lượng chất còn dư trong phản ứng.
2. Cho 12,15 gam nhôm và một dung dịch có chứa 54 gam CuSO4.
a. Chất nào dư sau phản ứng và dư bao nhiêu gam?
b. Lọc bỏ chất rắn rồi đem cô cạn dung dịch thì thu được bao nhiêu gam muối khan?
3. Nhiệt phân 29,4 gam kali clorat
a. Tính số milit khí oxi thu được.
b. Nếu đốt 50,4 gam sắt trong lọ đựng lượng khí oxi trên, tính khối lượng sản phẩn thu được?
c. Lấy hết Fe3O4 trên tác dụng với lượng dư Hcl theo sơ đồ sau:
Fe3O4 + HCl → FeCl2 + FeCl3 + H2O
Tính tổng khối lượng muối khan thu được sau khi cô cạn dụng dịch sau.
4. Cho 8,1 gam nhôm tác dụng với dung dịch có chứa 21,9 gam HCl.
a. Sau phản ứng chất nào còn dư, dư bao nhiêu gam?
b. Tính khối lượng AlCl3 thu được.
c. Khí sinh ra có thể khử được bao nhiêu gam CuO và thu được bao nhiêu gam Cu?
a)nAl=32,4/27=1,2(mol)
4Al+3O2---------->2Al2O3
TPT:4. 3. 2
TB:1,2. ? ?(mol)
Theo phương trình và bài ra ta có:
n Al2O3=1,2×2/4=0,6(mol)
m Al2O3=0,6×102=61,2(g)
Nhôm (III) oxit tác dụng với axit sunfuric theo phương trình phản ứng sau :
Al2O3 + 3H2SO4 → Al2(SO4)3 + 3H2O
Tính lượng muối nhôm sunfat được tạo thành nếu đã sử dụng 49g axit sunfuric nguyên chất tác dụng với 60g nhôm oxit. Sau phản ứng chất nào còn dư ? Lượng dư của chất đó là bao nhiêu ?
Phương trình hóa học của phản ứng:
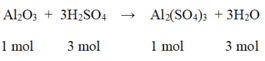
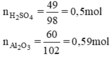
So sánh tỉ lệ 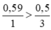 → Vậy Al2O3 dư
→ Vậy Al2O3 dư
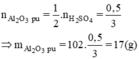
mAl2O3 (dư) = 60 - 17 = 43(g)
Đốt cháy hoàn toàn 16,2g nhôm trong bình chứa 13,44lit oxi (ĐKTC) thu được nhôm oxit Al2O3
a/ Viết PTHH?
b/ Chất nào còn dư sau phản ứng và dư bao nhiêu g?
c/Tính khối lượng nhôm oxit thu được ?
Bài này anh giúp rồi mà em. Em không hiểu chỗ nào nhỉ?
\(n_{Al}=\dfrac{16,2}{27}=0,6mol\)
\(n_{O_2}=\dfrac{13,44}{22,4}=0,6mol\)
\(4Al+3O_2\underrightarrow{t^o}2Al_2O_3\)
0,6 0,6
Theo pt: \(n_{Al}=\dfrac{0,6}{4}=0,15< \dfrac{0,6}{3}=0,2=n_{O_2}\)
\(\Rightarrow O_2\) dư và dư \(0,6-\dfrac{0,6}{4}\cdot3=0,15mol\)
\(n_{Al_2O_3}=n_{Al}=0,15mol\)
\(m_{Al_2O_3}=0,15\cdot102=15,3g\)
8/
Đốt 8,1 Al với 6,72 lít khí (đktc) thu được Nhôm oxit ( )
a) Viết phương trình hoá học xảy ra
b) Tính khối lượng Nhôm oxit thu được sau phản ứng
c) Sau phản ứng chất nào dư và khối lượng là bao nhiêu gam
a)
$4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3$
b)
$n_{Al} = \dfrac{8,1}{27} = 0,3(mol) ; n_{O_2} = \dfrac{6,72}{22,4} = 0,3(mol)$
Ta thấy :
$n_{Al} : 4 < n_{O_2} : 3$ nên $O_2$ dư
$n_{Al_2O_3} = \dfrac{1}{2}n_{Al} = 0,15(mol)$
$m_{Al_2O_3} = 0,15.102 = 15,3(gam)$
c) $n_{O_2\ pư} = \dfrac{3}{4}n_{Al} = 0,225(mol)$
$\Rightarrow m_{O_2\ dư} = (0,3 - 0,225).32 = 2,4(gam)$