Cho 100ml dung dịch NaCl 0,1M vào 150ml dung dịch AgNO3 0,1M. Tính nồng đọ mol các ion trong dung dịch thu được

Những câu hỏi liên quan
Cho 100ml dung dịch NaCl 1M tác dụng với 150ml dung dịch AgNO3 0,1M
a) Tính khối lượng kết tủa thu được
b) Tính nồng độ mol các chất sau phản ứng
PTHH: \(NaCl+AgNO_3\rightarrow NaNO_3+AgCl\)
a) Ta có: \(\left\{{}\begin{matrix}n_{NaCl}=1\cdot0,1=0,1\left(mol\right)\\n_{AgNO_3}=0,1\cdot0,15=0,015\left(mol\right)\end{matrix}\right.\)
Xét tỷ lệ: \(\frac{0,1}{1}>\frac{0,015}{1}\) \(\Rightarrow\) \(AgNO_3\) p/ứ hết
\(\Rightarrow n_{AgCl}=0,015mol\) \(\Rightarrow m_{AgCl}=0,015\cdot143,5=2,1525\left(g\right)\)
b) Ta có: \(\left\{{}\begin{matrix}n_{NaNO_3}=0,015mol\\n_{NaCl\left(dư\right)}=0,085mol\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}C_{M_{NaNO_3}}=\frac{0,015}{0,25}=0,06\left(M\right)\\C_{M_{NaCl\left(dư\right)}}=\frac{0,085}{0,25}=0,34\left(M\right)\end{matrix}\right.\) (Coi như thể tích dd không đổi)
Đúng 1
Bình luận (0)
Cho 100ml dung dịch BaCl2 0,1M vào 200ml dung dịch Na2SO4 0,05M. Tính
a. Khối lượng kết tủa thu được
b. Nồng độ mol của các chất trong dung dịch tạo thành
c. Nồng độ mol của các ion trong dung dịch sau phản ứng
a)
$BaCl_2 + Na_2SO_4 \to BaSO_4 + 2NaCl$
$n_{BaCl_2} = 0,01 = n_{Na_2SO_4} = 0,01 \Rightarrow $ Vừa đủ
$n_{BaSO_4} = n_{Na_2SO_4} = 0,01(mol)$
$m_{BaSO_4} = 0,01.233 = 0,233(gam)$
b)
$n_{NaCl} = 2n_{Na_2SO_4} = 0,02(mol)$
$V_{dd} = 0,1 + 0,2 = 0,3(lít)$
$C_{M_{NaCl}} = \dfrac{0,02}{0,3} = 0,067M$
c)
$[Na^+] = [Cl^-] = C_{M_{NaCl}} = 0,067M$
Đúng 2
Bình luận (0)
\(n_{BaCl_2}=0.1\cdot0.1=0.01\left(mol\right)\)
\(n_{Na_2SO_4}=0.2\cdot0.05=0.01\left(mol\right)\)
\(BaCl_2+Na_2SO_4\rightarrow BaSO_4+2NaCl\)
\(0.01..........0.01............0.01..............0.02\)
\(m_{BaSO_4}=0.01\cdot233=2.33\left(g\right)\)
\(C_{M_{NaCl}}=\dfrac{0.01}{0.1+0.2}=0.03\left(M\right)\)
\(\left[Na^+\right]=\left[Cl^-\right]=0.03\left(M\right)\)
Đúng 1
Bình luận (0)
Tính nồng độ mol/l các ion trong mỗi dd sau:
a) 100ml dd chứa 4,26 gam Al(NO3)3.
b) Tính nồng độ mol của ion Na+ trong dung dịch chứa NaNO3 0,1M,
Na2SO4 0,02M và NaCl 0,3M.
c) Dung dịch H2SO4 15% ( d= 1,1g/ml)
a) Ta có: \(n_{Al\left(NO_3\right)_3}=\dfrac{4,26}{213}=0,02\left(mol\right)\) \(\Rightarrow\left\{{}\begin{matrix}n_{Al^+}=0,02\left(mol\right)\\n_{NO_3^-}=0,06\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\left[Al^+\right]=\dfrac{0,02}{0,1}=0,2\left(M\right)\\\left[NO_3^-\right]=\dfrac{0,06}{0,1}=0,6\left(M\right)\end{matrix}\right.\)
b) Ta có: \(\left[Na^+\right]=0,1+0,02\cdot2+0,3=0,304\left(M\right)\)
c) Bạn xem lại đề !!
Đúng 0
Bình luận (0)
Trộn 150ml dung dịch BaCl2 0,2M vào 100ml dung dịch Ba(OH)2 1,5M thu được dung dịch Y. Tính nồng độ mol của các ion có trong dung dịch Y.
Cho 3,9g K vào 100ml dung dịch KOH 0,1M. Tính nồng độ mol của dung dịch thu được.
Ta có: nK = \(\dfrac{3,9}{39}=0,1\left(mol\right)\)
PTHH: 2K +2H2O ---> 2KOH + H2.
Đổi 100ml = 0,1 lít
Theo PT: nKOH = nK = 0,1(mol)
=> \(C_{M_{KOH}}=\dfrac{0,1}{0,1}=1M\)
Đúng 1
Bình luận (0)
Bn xem lại đề, K không tác dụng đc với KOH nha
Đúng 0
Bình luận (2)
1)Trộn lẫn 100ml dung dịch K2SO4 0,5M và 200ml dung dịch Fe2(SO4)3 0,1M và với 100ml dung dịch MgCl2 0,2M. Tính nồng độ mol/l của các ion trong dung dịch sau cùng.2) Một dung dịch KOH có nồng độ mol/l ion OH- gấp 4 lần trong dung dịch Ba(OH)2 0,1M.a) Tính nồng độ dung dịch KOH.b) Nếu trộn mỗi dung dịch 200ml với nhau thì được dung dịch mơi có nồng độ ion OH- bao nhiêu?
Đọc tiếp
1)Trộn lẫn 100ml dung dịch K2SO4 0,5M và 200ml dung dịch Fe2(SO4)3 0,1M và với 100ml dung dịch MgCl2 0,2M. Tính nồng độ mol/l của các ion trong dung dịch sau cùng.
2) Một dung dịch KOH có nồng độ mol/l ion OH- gấp 4 lần trong dung dịch Ba(OH)2 0,1M.
a) Tính nồng độ dung dịch KOH.
b) Nếu trộn mỗi dung dịch 200ml với nhau thì được dung dịch mơi có nồng độ ion OH- bao nhiêu?
Điện phân 2 bình điện phân có màng ngăn mắc nối tiếp. Bình 1 chứa 100ml dung dịch CuSO4 0,1M, bình 2 chứa 100ml dung dịch NaCl 0,1M. Ngừng điện phân khi dung dịch thu được trong bình 2 có pH 13. Nồng độ ion Cu2+ còn lại trong bình 1 (thể tích dung dịch coi như không đổi) là A. 0,04M B. 0,1M C. 0,08M D. 0,05M
Đọc tiếp
Điện phân 2 bình điện phân có màng ngăn mắc nối tiếp. Bình 1 chứa 100ml dung dịch CuSO4 0,1M, bình 2 chứa 100ml dung dịch NaCl 0,1M. Ngừng điện phân khi dung dịch thu được trong bình 2 có pH = 13. Nồng độ ion Cu2+ còn lại trong bình 1 (thể tích dung dịch coi như không đổi) là
A. 0,04M
B. 0,1M
C. 0,08M
D. 0,05M
Đáp án D
Phản ứng điện phân hai dung dịch:

Vì hai bình điện phân mắc nối tiếp nên cường độ dòng điện qua hai bình điện phân là như nhau.
Do đó số mol electron trao đổi ở hai bình điện phân bằng nhau.
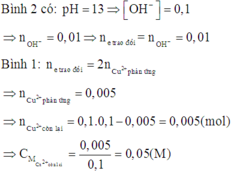
Đúng 0
Bình luận (0)
cho 150 ml dung dịch kcl 0,1M vào dung dịch CACL2 0,1 M thu được dung dịch A . tình nồng độ mol của ion cl- trong A
\(n_{Cl^-}=n_{KCl}+2n_{CaCl_2}=0,15.0,1+0,15.0,1.2=0,045\left(mol\right)\\ \Rightarrow\left[Cl^-\right]=\dfrac{0,045}{0,15}=0,3M\)
Đúng 1
Bình luận (0)
Trộn 200ml dung dịch NaC1 0,1M với 300ml dung dịch Na2CO3 0,1M. Tính nồng độ các ion trong dung dịch thu được? Cần gấppp ạa
\(n_{NaCl}=0,1.0,2=0,02\left(mol\right)\)
\(m_{Na_2CO_3}=0,1.0,3=0,03\left(mol\right)\)
\(\left\{{}\begin{matrix}n_{Na^+}=0,02+0,03.2=0,08\left(mol\right)\\n_{Cl^-}=0,02\left(mol\right)\\n_{CO_3^{2-}}=0,03\left(mol\right)\end{matrix}\right.\)
=> \(\left\{{}\begin{matrix}C_{M\left(Na^+\right)}=\dfrac{0,08}{0,2+0,3}=0,16M\\C_{M\left(Cl^-\right)}=\dfrac{0,02}{0,2+0,3}=0,04M\\C_{M\left(CO_3^{2-}\right)}=\dfrac{0,03}{0,2+0,3}=0,06M\end{matrix}\right.\)
Đúng 1
Bình luận (0)






















