tính % khối lượng của đồng vị 35 Cl trong axit pecloric HCLO4 . Cho H=1;O=16

Những câu hỏi liên quan
Nguyên tử khối trung bình của Clo là 35,5. Clo trong tự nhiên có hai đồng vị là 35 Cl và 37 Cl. Tính phần trăm về khối lượng của 37 Cl chứa trong HClO4 (với Hidro đồng vị là 1 H, oxi đồng vị là 16 O)
\(\%^{35}Cl=x\%\Rightarrow\%^{37}Cl=\left(100-x\right)\%\)
\(\overline{M}=\dfrac{35x+37\cdot\left(100\%-x\right)}{100\%}=35.5\left(g\text{/}mol\right)\)
\(\Rightarrow x=75\%\)
\(\%^{37}Cl_{\left(HClO_4\right)}=\dfrac{25\%\cdot37}{1+35.5+16\cdot4}\cdot100\%=9.2\%\)
Đúng 3
Bình luận (1)
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có:
, vậy x = 75%.
Phần trăm khối lượng của 37Cl trong HClO4=
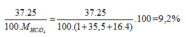
Đúng 1
Bình luận (2)
Khối lượng nguyên tử trung bình của Cl là 35,5 đvC . Clo có 2 đồng vị là 35Cl và 37Cl .
a, Hỏi có bao nhiêu % về khối lượng của 35Cl chứa trong axit pecloric HClO4.
b, Có bao nhiêu % về khối lượng của 37Cl chứa trong muối kaliccloratKClO3 ; canxiclorat Ca(ClO3)2.
- Gọi % 35Cl là x\(\rightarrow\)100-x là phần trăm 37Cl
\(\overline{M}_{Cl}=\dfrac{35.x+37\left(100-x\right)}{100}=35,5\)
3700-2x=3550\(\rightarrow\)2x=150\(\rightarrow\)x=75
% đồng vị 35Cl là 75%
%37Cl=25%
Đúng 0
Bình luận (4)
Trong phân tử HClO4 chứa đồng vị O(z=8,A=16) ; H(z=1,A=1); Cl(z=17,A=35) Cl(z=17,A=37). Tính % về khối lượng của đồng vị Cl(z=17,A=37) trong HClO4 biết \(_{M_{Cl}}\)=35,5?
giúp e với ạ
Gọi P2 là % của đồng vị Cl(z=17,A=37)
=> 100-P1 là % của đồng vị Cl( z = 17,A = 35)
Theo giả thuyết ta có : \(35,5=\frac{35\cdot\left(100-P2\right)+37\cdot P2}{100}\)=> P2 = 25%
% về khối lượng của đồng vị Cl(z=17,A= 37) trong HClO4 là :
\(\frac{25\%\cdot37}{1+35,5+16\cdot4}\cdot100\)= 9,2 %
Đúng 0
Bình luận (1)
Khối lượng nguyên tử trung bình của Clo là 35,5. Clo trong tự nhiên có 2 đồng vị là 35 và 37. Hỏi \(\frac{37}{17}\)Cl chiếm bao nhiêu % về khối lượng trong phân tử axit pecloric HClO4
Gọi: x là % nguyên tử \(\frac{35}{17}Cl\) và (100-x ) là % nguyên tử \(\frac{37}{17}Cl\)
Ta có : x + y = 100 (1)
Mặt khác :
\(\overline{M}=\frac{35x+37y}{100}=35.5\)
<=> 35x + 37y = 3550 (2)
Giải (1) và (2) :
x = 75
y = 25
Vậy: \(\frac{37}{17}Cl\) chiếm 25% khối lượng trong phân tử HClO4
Đúng 0
Bình luận (0)
Coi %Cl(37) =x thì %Cl(35)=1-x
Theo bài ra : 37x+35(1-x)=35,5
Suy ra x= 0,25
Vậy %Cl(37) = 37.0,25.100%/1+35,5+16.4 = 9,2%
Đúng 0
Bình luận (0)
Nguyên tử khối trung bình của clo là 35,5. Clo trong tự nhiên có 2 đồng vị là 35 Cl và 37Cl. Phần trăm khối lượng của 3717Cl chứa trong HClO4 ?(với hidro là đồng vị 11H, oxi là đồng vị 168O) là.
Tham thảo :
Phần trăm đồng vị 35Cl = x, thì % đồng vị 37Cl = 100 - x
Ta có:
![]() , vậy x = 75%.
, vậy x = 75%.
Phần trăm khối lượng của 37Cl trong HClO4= 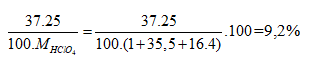
Đúng 0
Bình luận (0)
Trong tự nhiên đồng vị 1737Cl chiếm 24,23% số nguyên tử clo, còn lại là 1735Cl. Tính thành phần % về khối lượng 1737Cl có trong HClO4(H đồng vị 1, O đồng vị 16. Nguyên tử khối trung bình của Cl là 35,5
Đặt số mol HClO4 là 1 mol ⇒ có 0,2423 mol 37Cl ( Vì đồng vị 37Cl chiếm 24,23% số nguyên tử clo mà số nguyên tử\(=n.N_A\)
\(\%m^{37}Cl=\dfrac{0,2423.37}{1+35,5+16.4}.100\%\approx8,92\%\)
Đúng 0
Bình luận (0)
Trong tự nhiên đồng vị 37Cl chiếm 24,23% số nguyên tử clo. Tính thành phần % về khối lượng 37Cl có trong HClO4(H đồng vị 1, O đồng vị 16. Nguyên tử khối trung bình của Cl là 35,5
Đặt số mol HClO4 là 1 mol thì có 0,2423 mol 37Cl
\(\%m_{^{37}Cl}=\dfrac{37.0,2423}{1+35,5+16.4}.100\%\approx8,9205\%\)
Đúng 0
Bình luận (0)
Trong tự nhiên clo có hai đồng vị bền: 37Cl chiếm 24,23% tổng số nguyên tử, còn lại là 35Cl (Cl có số hiệu nguyên tử là 17). Thành phần % theo khối lượng của 37Cl trong HClO4 là (Cho: H 1, O 16): A. 8,92% B. 8,43% C. 8,56% D. 8,79%
Đọc tiếp
Trong tự nhiên clo có hai đồng vị bền: 37Cl chiếm 24,23% tổng số nguyên tử, còn lại là 35Cl (Cl có số hiệu nguyên tử là 17).
Thành phần % theo khối lượng của 37Cl trong HClO4 là (Cho: H = 1, O = 16):
A. 8,92%
B. 8,43%
C. 8,56%
D. 8,79%
Đáp án A
• %35Cl = 100% - 24,23% = 75,77%
→ MCl = 37 x 0,2423 + 35 x 0,7577 = 35,4846.
→ Thành phần % của 37Cl trong HClO4 là
![]()
Đúng 0
Bình luận (0)
Số oxi hoá của clo trong axit pecloric HClO 4 là
A. +3. B.+5.
C.+7. D.-1.























