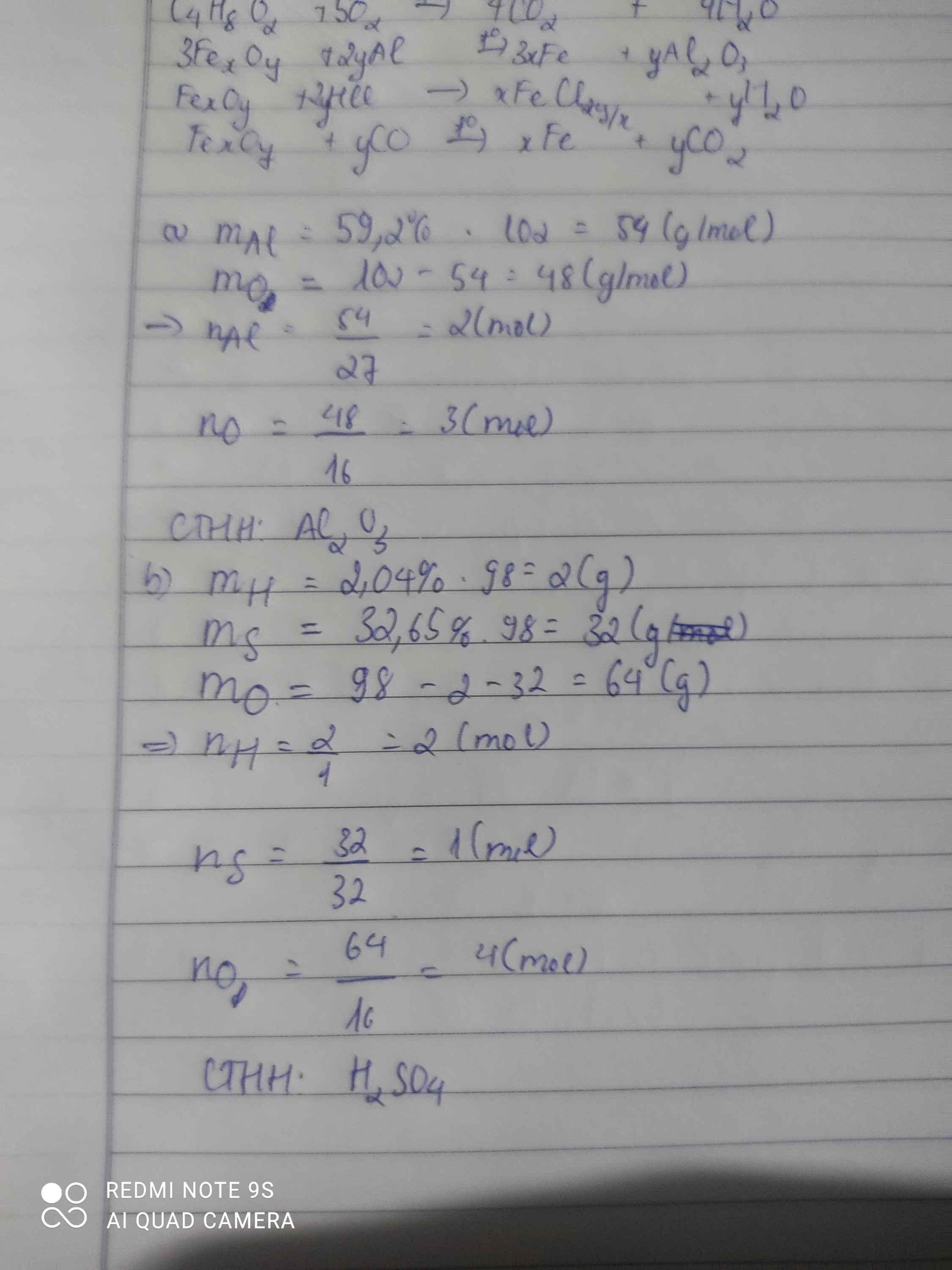nêu cách tính phần trăm nguyên tố trong hợp chất khi biết công thức hóa học của hợp chất.

Những câu hỏi liên quan
a/ nêu các bước tính phần trăm theo khối lượng của các nguyên tố trong hợp chất
b/ nêu các bước xác định công thức hóa học của hợp chất khi biết thành phần nguyên tố
GIÚP MÌNH VỚI MAI THI RÒI . CẢM ƠN MNG!!!
Nêu các bước giải toán xác định công thức hóa học của hợp chất khi biết thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất.
Các bước giải :
B1 : Tìm khối lượng của mỗi nguyên tố có trong 1 mol hợp chất.
B2 : Tìm số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
B3 : Lập CTHH.
Đúng 0
Bình luận (0)
Nêu các bước giải bài toán xác định thành phần phần trăm theo khối lượng của các nguyên tố tron hợp chất khi biết công thức hóa học của hợp chất.
Các bước giải :
B1 : Tính khối lượng mol của hợp chất.
B2 : Tính số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
B3 : Tính khối lượng của mỗi nguyên tố có trong 1 mol hợp chất.
B4 : Tính thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất.
Đúng 0
Bình luận (2)
Các bước giải:
Bước 1:Tính khối lượng M của hợp chất.
Bước 2 :Tính số M nguyên tử của mỗi nguyên tố có trong 1 M hợp chất.
Bước 4:Tính phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất.
☆♡CHÚC BẠN HỌC TỐT♡☆
Đúng 0
Bình luận (0)
Bước 1 : tính khối lượng của hợp chất (đvC)
Bước 2 : tính khối lượng các nguyên tố trong hợp chất(đvC)
Bước 3 : tính % khối lượng của nguyên tố trong hợp chất theo công thức :
%mnguyên tố = (NTKnguyên tố * số nguyên tử nguyên tố đó trong hợp chất) : PTKhợp chất
Đúng 0
Bình luận (0)
Xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất.Hợp chấtkhối lượng mình mol( M )Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chấtKhối lượng của mỗi nguyên tố có trong 1 mol hợp chấtThành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chấtKMnO4 -Nêu các bước giải bài toán xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất ....
Đọc tiếp
Xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất.
| Hợp chất | khối lượng mình mol( M ) | Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất | Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất | Thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất |
| KMnO4 |
-Nêu các bước giải bài toán xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất .
-Viết công thức tính thành phần phần trăm theo khối lượng của 1 nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất.
Khối lượng mol :
MKMnO4 = 39 + 55 + 64 = 158 (g/mol)
Số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất :
nK = 1 mol
nMn = 1 mol
nO = 4 mol
Khối lượng của mỗi nguyên tố có trong 1 mol hợp chất :
mK = 39.1 = 39 (g)
mMn = 55.1 = 55 (g)
mO = 16.4 = 64 (g)
Thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất :
\(\%m_K=\frac{m_K}{M_{KMnO_4}}.100\%=\frac{39}{158}.100\%=24,7\%\)
\(\%m_{Mn}=\frac{m_{Mn}}{M_{KMnO_4}}.100\%=\frac{55}{158}.100\%=34,8\%\)
\(\%m_O=\frac{m_O}{m_{KMnO_4}}.100\%=\frac{64}{158}.100\%=40,5\%\)
Đúng 0
Bình luận (5)
Các bước giải bài toán xác định thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất :
B1 : Tính khối lượng mol (M) của hợp chất.
B2 : Tính số mol nguyên tử của mỗi nguyên tố có trong 1 mol hợp chất.
B3 : Tính khối lượng của mỗi nguyên tố có trong 1 mol hợp chất.
B4 : Tính thành phần phần trăm theo khối lượng của mỗi nguyên tố trong hợp chất.
Đúng 0
Bình luận (0)
Công thức tính thành phần phần trăm theo khối lượng của 1 nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất :
\(\%m_A=\frac{m_A}{M_{h\text{/}c}}.100\%\)
Đúng 0
Bình luận (7)
Biết vận dụng lập công thức hóa học của hợp chất và tính được phần trăm các nguyên tố trong hợp chất ( kết nối tri thức )
Viết công thức tính thành phần phần trăm theo khối lượng của 1 nguyên tố trong hợp chất khi biết công thức hoá học của hợp chất
Nếu biết công thức của hợp chất ta có thể tính thành phần phần trăm theo khối lượng của các nguyên tố trong hợp chất đó theo các bước sau:
- Tính khối lượng mol của hợp chất AxBy:
- Xác định số mol nguyên tử của từng nguyên tố có trong 1 mol hợp chất AxBy.
1 mol AxBy có: x mol nguyên tử A và y mol nguyên tử B.
- Tìm khối lượng các nguyên tố trong 1 mol hợp chất AxBy.
mA=x.MA
mB=y.MB
- Tính phần trăm theo khối lượng của từng nguyên tố theo công thức:
%A= mA .100%= .100%
%B= .mB . 100%= .100%
Hoặc %B=100%-%A
Đúng 0
Bình luận (1)
Theo mình còn có một cách khác có thể giải tất cả dạng bài kiểu này
B1 : Gọi CTHH cần tìm la AxByCz
B2 : Ta có : x: y :z = %A/ MA : %B / MB : %C/ MC = a :b :c
B3 Chọn x=a ; y=b ; z=c
B4 Đưa ra công thức đơn giản AaBbCc
B5 Dựa vào PTK đưa ra CT phân tử
Làm tương tự với các bài hpas chỉ có 2 nguyên tố hóa học
Chúc bạn học tốt nha
Đúng 0
Bình luận (0)
1. Một hợp chất của nguyên tố R (hóa trị IV) với oxi có phần trăm khối lượng của nguyên tố R là 50%. Xác định nguyên tố R và công thức hóa học của hợp chất?2. Xác định công thức hóa học của hợp chất tạo kim loại M ( hóa trị II) với nhóm SO4? Biết rằng M chiếm 20% khối lượng của phân tử?3. Hợp chất A ở thể khí có %mC 75% và còn lại là H. Xác định CTHH của A? Biết tỉ khối của khí A với khí oxi là 0,54. Hợp chất B tạo bởi hidro và nhóm nguyên tử ( XOy) hóa trị III. Biết rằng phân tử B nặng bằng p...
Đọc tiếp
1. Một hợp chất của nguyên tố R (hóa trị IV) với oxi có phần trăm khối lượng của nguyên tố R là 50%. Xác định nguyên tố R và công thức hóa học của hợp chất?
2. Xác định công thức hóa học của hợp chất tạo kim loại M ( hóa trị II) với nhóm SO4? Biết rằng M chiếm 20% khối lượng của phân tử?
3. Hợp chất A ở thể khí có %mC = 75% và còn lại là H. Xác định CTHH của A? Biết tỉ khối của khí A với khí oxi là 0,5
4. Hợp chất B tạo bởi hidro và nhóm nguyên tử ( XOy) hóa trị III. Biết rằng phân tử B nặng bằng phân tử H2SO4 và nguyên tố oxi chiếm 65,31% về khối lượng của B.
a. Xác định chỉ số y và nguyên tử khối của nguyên tố X?
b. Cho biết tên, kí hiệu hóa học của X và công thức hóa học của B?
1. CT của hợp chất : RO2 (do R hóa trị IV)
Ta có : \(\%R=\dfrac{R}{R+16.2}.100=50\)
=> R=32
Vậy R là lưu huỳnh (S), CTHH của hợp chất : SO2
Đúng 2
Bình luận (1)
2. CTHH của hợp chất tạo kim loại M ( hóa trị II) với nhóm SO4 là MSO4 (do M hóa trị II)
Ta có : \(\%M=\dfrac{M}{M+96}.100=20\)
=>M=24
Vây M là Magie (Mg), CTHH của hợp chất MgSO4
Đúng 2
Bình luận (0)
3. Đặt CTHH của A là CxHy
\(M_A=0,5M_{O_2}=16\left(đvC\right)\)
Ta có : \(\%C=\dfrac{12x}{16}.100=75\Rightarrow x=1\)
Mặc khác : 12x + y = 16
=> y=4
Vậy CTHH của A là CH4
Đúng 2
Bình luận (0)
Xem thêm câu trả lời
1) Một hợp chất chứa 59,2 % Al về khối lượng, còn lại là oxi. Xác định công thức hóa học của hợp chất biết khối lượng mol của hợp chất là 102 g/mol.
2) Xác định công thức hóa học của hợp chất A. Biết thành phần phần trăm về khối lượng các nguyên tố: 2,04% H, 32,65% S, còn lại là oxi, MA = 98 g/mol.
Bài 2:
\(Đặt.CTTQ.của.A:H_xS_yO_z\left(x,y,z:nguyên,dương\right)\\ Ta.có:\left\{{}\begin{matrix}x=\dfrac{98.2,04\%}{1}=2\\y=\dfrac{98.32,65\%}{32}=1\\z=\dfrac{98.\left(100\%-2,04\%-32,65\%\right)}{16}=4\end{matrix}\right.\\ \Rightarrow x=2;y=1;z=4\\ \Rightarrow CTHH:H_2SO_4\)
Đúng 5
Bình luận (1)
Bài 1: Sửa đề 59,2% Al thành 52,9% Al
\(Đặt.CTTQ:Al_xO_y\left(x,y:nguyên,dương\right)\\ x=\dfrac{52,9\%.102}{27}\approx2\\ \Rightarrow y\approx\dfrac{\left(100\%-52,9\%\right).102}{16}\approx3\\ \Rightarrow CTHH:Al_2O_3\)
Đúng 5
Bình luận (0)
1) \(m_{Al}=102.\dfrac{59,2}{100}=60,384\) (g)
\(m_O=102.\dfrac{100-59,2}{100}=41,616\) (g).
\(n_{Al}=\dfrac{m}{M}=\dfrac{60,384}{27}\approx2\) (mol).
\(n_O=\dfrac{m}{M}=\dfrac{41,616}{16}\approx3\) (mol).
-Công thức hóa học của hợp chất: \(Al_2O_3\).
2) \(m_H=98.\dfrac{2,04}{100}=1,9992\) (g).
\(m_S=98.\dfrac{32,65}{100}=31,997\) (g).
\(m_O=98.\dfrac{100-2,04-32,65}{100}=64,0038\) (g).
\(n_H=\dfrac{m}{M}=\dfrac{1,9992}{1}\approx2\) (mol).
\(n_S=\dfrac{m}{M}=\dfrac{31,997}{32}\approx1\) (mol).
\(n_O=\dfrac{m}{M}=\dfrac{64,0038}{16}\approx4\) (mol).
-Cộng thức hóa học của hợp chất A: \(H_2SO_4\)
Đúng 1
Bình luận (3)
a) Một hợp chất chứa 59,2 % Al về khối lượng, còn lại là oxi. Xác định công thức hóa học của hợp chất biết khối lượng mol của hợp chất là 102 g/mol.
b) Xác định công thức hóa học của hợp chất A. Biết thành phần phần trăm về khối lượng các nguyên tố: 2,04% H, 32,65% S, còn lại là oxi, MA = 98 g/mol.
Một hợp chất được tạo bởi nguyên tố A và nguyên tố oxi, biết thành phần phần trăm khối lượng là 70%A , còn lại là nguyên tố oxi. Lập công thức hóa học của hợp chất?
CTHH: AxOy
Có: \(\dfrac{x.M_A}{x.M_A+16y}.100\%=70\%\)
=> \(M_A=\dfrac{112y}{3x}=\dfrac{2y}{x}.\dfrac{56}{3}\)
Xét \(\dfrac{2y}{x}\) = 1 => L
Xét \(\dfrac{2y}{x}=2\) => L
Xét \(\dfrac{2y}{x}=3\) => MA = 56 (Fe) => \(\dfrac{x}{y}=\dfrac{2}{3}\) => CTHH: Fe2O3
Đúng 1
Bình luận (0)
Ta có:
\(\%A=70\%\rightarrow\%O=100\%-70\%=30\%\)
Theo quy tắc hóa trị mở rộng:
\(\dfrac{70}{MA}.a=\dfrac{30}{16}.2\) với \(a\) là hóa trị của \(M\)
\(\rightarrow\dfrac{70}{MA}.a=3,75\\ \rightarrow\dfrac{70}{MA}=\dfrac{3,75}{a}\\ \rightarrow3,75.M.A=70a\\ \rightarrow MA=18,6.a\)
Bảng biện luận chạy từ \(1->7\)
| \(a\) | \(1\) | \(2\) | \(3\) | \(4\) | \(5\) | \(6\) |
| \(MA=18,6a\) | \(19\left(loại\right)\) | \(38\left(loại\right)\) | \(56\left(nhận\right)\) | \(74\left(loại\right)\) | \(93\left(loại\right)\) | \(112\left(loại\right)\) |
\(\rightarrow\) Với \(a=3\) thì \(MA=56\) là \(Fe\) mang hóa trị \(III\)
\(\rightarrow CTHH\) của \(A\) là \(Fe_2O_3\)
Đúng 0
Bình luận (0)