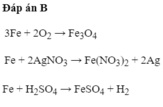Kim loại magnesium có phản ứng được với dung dịch muối copper(II) nitrate không? Giải thích.

Những câu hỏi liên quan
cho 3,2g kim loại copper tác dụng với dung dịch silver nitrate agno3 thu đc muối copper (ll) nitrate vf a gm chất rắn
a/ lập phương trình hóa hc
b/ tính khối lượng muối tạo thành
c/ tính a
d/ tính thể tính dung dịch silver nitrate agno3 0,5M đã tham gia phản ứng
a
\(Cu+2AgNO_3\rightarrow Cu\left(NO_3\right)_2+2Ag\downarrow\)
0,05 --> 0,1-----------> 0,05------>0,1
b
\(n_{Cu}=\dfrac{3,2}{64}=0,05\left(mol\right)\)
\(m_{Cu\left(NO_3\right)_2}=0,05.188=9,4\left(g\right)\)
c
\(a=m_{Ag}=108.0,1=10,8\left(g\right)\)
d
\(V_{AgNO_3}=\dfrac{0,1}{0,5}=0,2\left(l\right)\)
Đúng 1
Bình luận (0)
a,Cho 5,6 gam kim loại Magnesium phản ứng hoàn toàn với dung dịch HCL 2M.
Tính thể thích dung dịch HCL đã tham gia phản ứng
b,Ở nhiệt độ 25'C, khi cho 10 gam muối X vào 300 gam nước, khuấy kĩ thì còn lại 4 gam muối không tan.Tính độ tan muối X
Câu 12: Hãy nêu hiện tượng và viết PTHH xảy ra ở thí nghiệm Copper(II) oxide phản ứng với dung dịch HCl. Nếu thay dung dịch HCl bằng dung dịch H2SO4 thì có phản ứng hoá học xảy ra không? Giải thích?
Cả hai phản ứng đều làm cho CuO tan, tạo dung dịch xanh lam
\(CuO+2HCl->CuCl_2+H_2O\\ CuO+H_2SO_4->CuSO_4+H_2O\)
Đúng 3
Bình luận (0)
Cho 16,8 gam irontacs dụng hoàn toàn với nitric acid , sau phản ứng thu được muối iron(II) nitrate và khí h2 C)cho muối iron(II) nitrate thu được ở phản ứng trên vào ống nghiệm chứa 300ml dung dịch NaOH. Tính nồng độ mol dung dịch NaOH cần dùng
Fe + HNO3 thường không sinh khí H2 nha em
Đúng 0
Bình luận (0)
Kim loại X có những tính chất hóa học sau- Phản ứng với oxi khi nung nóng- Phản ứng với dung dịch
A
g
N
O
3
- Phản ứng với dung dịch
H
2
S
O
4
loãng giải phóng khí
H
2
và muối của k...
Đọc tiếp
Kim loại X có những tính chất hóa học sau
- Phản ứng với oxi khi nung nóng
- Phản ứng với dung dịch A g N O 3
- Phản ứng với dung dịch H 2 S O 4 loãng giải phóng khí H 2 và muối của kim loại hóa trị II. Kim loại X là
A. Cu
B. Fe
C. Al
D. Na
Đáp án B
A loại vì Cu không phản ứng với H2SO4 loãng
C loại vì Al có hóa trị III trong hợp chất D loại vì Na có hóa trị I trong hợp chấ
Đúng 0
Bình luận (0)
Kim loại X có những tính chất hóa học sau:
- Phản ứng với oxit khi nung nóng.
- Phản ứng với dung dịch A g N O 3 .
- Phản ứng với dung dịch H 2 S O 4 loãng giải phóng khí và H 2 muối của kim loại hóa trị II. Kim loại X là:
A. Cu
B. Fe
C. Al
D. Na
Câu 8: Nhiệt phân copper(II) nitrate Cu(NO3)2 thu được copper(II) oxide CuO, nitrogen dioxide NO2 và khí oxygen O2.a. Lập phương trình hóa học của phản ứng. b. Nếu nhiệt phân hoàn toàn 28,2 gam copper(II) nitrate với hiệu suất phản ứng 100% thì thu được bao nhiêu gam copper(II) oxide và bao nhiêu lít khí oxygen ở đkc?c. Muốn thu được 6,1975 lít (đkc) hỗn hợp 2 khí NO2 và O2 thì phải nhiệt phân bao nhiêu gam copper(II) nitrate, biết hiệu suất phản ứng đạt 80%.
Đọc tiếp
Câu 8: Nhiệt phân copper(II) nitrate Cu(NO3)2 thu được copper(II) oxide CuO, nitrogen dioxide NO2 và khí oxygen O2.
a. Lập phương trình hóa học của phản ứng.
b. Nếu nhiệt phân hoàn toàn 28,2 gam copper(II) nitrate với hiệu suất phản ứng 100% thì thu được bao nhiêu gam copper(II) oxide và bao nhiêu lít khí oxygen ở đkc?
c. Muốn thu được 6,1975 lít (đkc) hỗn hợp 2 khí NO2 và O2 thì phải nhiệt phân bao nhiêu gam copper(II) nitrate, biết hiệu suất phản ứng đạt 80%.
a, \(2Cu\left(NO_3\right)_2\underrightarrow{t^o}2CuO+4NO_2+O_2\)
b, \(n_{Cu\left(NO_3\right)_2}=\dfrac{28,2}{188}=0,15\left(mol\right)\)
Theo PT: \(\left\{{}\begin{matrix}n_{CuO}=n_{Cu\left(NO_3\right)_2}=0,15\left(mol\right)\\n_{O_2}=\dfrac{1}{2}n_{Cu\left(NO_3\right)_2}=0,075\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow m_{CuO}=0,15.80=12\left(g\right)\)
\(V_{O_2}=0,075.24,79=1,85925\left(l\right)\)
c, Ta có: \(n_{NO_2}+n_{O_2}=\dfrac{6,1975}{24,79}=0,25\left(mol\right)\)
Gọi: nO2 = x (mol)
Theo PT: \(n_{NO_2}=4n_{O_2}=4x\left(mol\right)\)
⇒ 4x + x = 0,25 ⇒ x = 0,05 (mol)
Theo PT: \(n_{Cu\left(NO_3\right)_2\left(LT\right)}=2n_{O_2}=0,1\left(mol\right)\)
\(\Rightarrow m_{Cu\left(NO_3\right)_2\left(LT\right)}=0,1.188=18,8\left(g\right)\)
Mà: H = 80% \(\Rightarrow m_{Cu\left(NO_3\right)_2\left(TT\right)}=\dfrac{18,8}{80\%}=23,5\left(g\right)\)
Đúng 5
Bình luận (0)
Lập PTHH cho các phản ứng sau:a. Đốt cháy dây kim loại magnesium trong khí oxygen O2 thu được magnesium oxide MgOb. Đốt cháy kim loại iron trong khí oxygen thu được iron (II,III) oxide Fe3O4.c. Cho viên kim loại zinc vào cốc đựng dung dịch hydrochloric acid HCl sinh ra khí hydrogen H2 và muối zinc chloride ZnCl2.Mọi người có thể giúp em được không ạ
Đọc tiếp
Lập PTHH cho các phản ứng sau:
a. Đốt cháy dây kim loại magnesium trong khí oxygen O2 thu được magnesium oxide MgO
b. Đốt cháy kim loại iron trong khí oxygen thu được iron (II,III) oxide Fe3O4.
c. Cho viên kim loại zinc vào cốc đựng dung dịch hydrochloric acid HCl sinh ra khí hydrogen H2 và muối zinc chloride ZnCl2.
Mọi người có thể giúp em được không ạ![]()
a) $2Mg + O_2 \xrightarrow{t^o} 2MgO$
b)
$2Fe + O_2 \xrightarrow{t^o} 2FeO$
$4Fe + 3O_2 \xrightarrow{t^o} 2Fe_2O_3$
$3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4$
c)
$Zn + 2HCl \to ZnCl_2 + H_2$
Đúng 5
Bình luận (1)
Viết công thức của các muối sau: potassium sulfate, sodium hydrogensulfate, sodium hydrogencarbonate, sodium chloride, sodium nitrate, calcium hydrogenphosphate, magnesium sulfate, copper(II) sulfate.
- Potassium sulfate: K2SO4
- Sodium hydrogensulfate: NaHSO4
- Sodium hydrogencarbonate: NaHCO3
- Sodium chloride: NaCl
- Sodium nitrate: NaNO3
- Calcium hydrogenphosphate: CaHPO4
- Magnesium sulfate: MgSO4
- Copper (II) sulfate: CuSO4
Đúng 1
Bình luận (0)
Cho 4 kim loại X, Y, Z, T đứng sau Mg trong dãy hoạt động hóa học, biết rằng: - X, Y tác dụng được với dung dịch HCl giải phóng khí Hidro - Z, T không có phản ứng với dung dịch HCl - Y tác dụng với dung dịch muối của X và giải phóng kim loại X - T tác dụng được với dung dịch muối của Z là giải phóng kim loại Z Kim loại có tính khử yếu nhất trong 4 kim loại là: A. T B. Y C. Z D. X
Đọc tiếp
Cho 4 kim loại X, Y, Z, T đứng sau Mg trong dãy hoạt động hóa học, biết rằng:
- X, Y tác dụng được với dung dịch HCl giải phóng khí Hidro
- Z, T không có phản ứng với dung dịch HCl
- Y tác dụng với dung dịch muối của X và giải phóng kim loại X
- T tác dụng được với dung dịch muối của Z là giải phóng kim loại Z
Kim loại có tính khử yếu nhất trong 4 kim loại là:
A. T
B. Y
C. Z
D. X
Đáp án C
X, Y phản ứng được với HCl => X, Y đứng trước H trong dãy hoạt động hóa học
Z, T không phản ứng với HCl => Z, T đứng sau H trong dãy hoạt động hóa học
=> X, Y có tinh khử mạnh hơn Z, T. Giờ chỉ so sánh Z và T
T đẩy được Z ra khỏi muối của Z => T có tính khử mạnh hơn Z
=> Z là có tính khử yếu nhất
Đúng 0
Bình luận (0)