Có cách nào để biết hoá trị qua khối lượng mol không ạ? VD oxygen thì mình có thể suy ra hoá trị khi biết O = 16 không ạ?

Những câu hỏi liên quan
Cho biết nikem có khối lượng mol nguyên tử là 58,7 và hoá trị. Nếu cho dòng điện không đổi có cường độ 5A chạy qua một bình điện phân chứa dung dịch muối niken trong khoảng thời gian 1 giờ thì khối lượng niken giải phóng ra ở catot của bình điện phân là A. 5,47g B. 2,73g C. 547g D. 273g
Đọc tiếp
Cho biết nikem có khối lượng mol nguyên tử là 58,7 và hoá trị. Nếu cho dòng điện không đổi có cường độ 5A chạy qua một bình điện phân chứa dung dịch muối niken trong khoảng thời gian 1 giờ thì khối lượng niken giải phóng ra ở catot của bình điện phân là
A. 5,47g
B. 2,73g
C. 547g
D. 273g
Đáp án A
Khối lượng niken giải phóng ra ở catot của bình điện phân là:
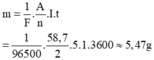
Đúng 0
Bình luận (0)
Cho biết nikem có khối lượng mol nguyên tử là 58,7 và hoá trị. Nếu cho dòng điện không đổi có cường độ 5A chạy qua một bình điện phân chứa dung dịch muối niken trong khoảng thời gian 1 giờ thì khối lượng niken giải phóng ra ở catot của bình điện phân là A. 5,47g B. 2,73g C. 547g D. 273g
Đọc tiếp
Cho biết nikem có khối lượng mol nguyên tử là 58,7 và hoá trị. Nếu cho dòng điện không đổi có cường độ 5A chạy qua một bình điện phân chứa dung dịch muối niken trong khoảng thời gian 1 giờ thì khối lượng niken giải phóng ra ở catot của bình điện phân là
A. 5,47g
B. 2,73g
C. 547g
D. 273g
Đáp án: A
Khối lượng niken giải phóng ra ở catot của bình điện phân là:

Đúng 0
Bình luận (0)
Ai giúp mình với ạ Tính thể tích không khí cần để oxi hoá hết: - 0,1 mol CH4 - 0.1 mol C4H10 cho biết oxi chiếm 1/5 thể tích không khí. Hỏi trường hợp nào hết nhiều không khí hơn?
a) \(CH_4+2O_2\rightarrow CO_2+2H_2O\)
0,1 0,2
\(V_{O_2}=0,2\cdot22,4=4,48l\)
\(\Rightarrow V_{kk}=5V_{O_2}=5\cdot4,48=22,4l\)
b) \(C_4H_{10}+\dfrac{13}{2}O_2\rightarrow4CO_2+5H_2O\)
0,1 0,65
\(V_{O_2}=0,65\cdot22,4=14,56l\)
\(V_{kk}=5V_{O_2}=5\cdot14,56=72,8l\)
Dùng \(0,1molC_4H_{10}\) cần nhiều lượng không khí hơn.
Đúng 4
Bình luận (0)
Hoà tan một lượng muối cacbonat của kim loại hoá trị III bằng dung dịch H2SO4 nồng
độ 16%. Sau khi khí không thoát ra nữa, thu được dung dịch chứa 20% muối sunfat tan. Xác
định kim loại đó.
GIÚP MÌNH VỚI Ạ!!!!!!!!!!!!!!!!!!!!!!!!!!
\(Đặt.muối:A_2\left(CO_3\right)_3\\ n_{A_2\left(CO_3\right)_3}=a\left(mol\right)\Rightarrow n_{H_2SO_4}=3a\left(mol\right)\\ m_{ddH_2SO_4}=\dfrac{3a.98.100}{16}=1837,5a\left(g\right)\\ A_2\left(CO_3\right)_3+3H_2SO_4\rightarrow A_2\left(SO_4\right)_3+3CO_2+3H_2O\\ m_{ddsau}=\left(M_A.2+180\right).a+1837,5a-44a.3=1885,5a+2M_A.a\left(g\right)\\ Vì:C\%_{dd.muối.sunfat}=16\%\\ \Leftrightarrow\dfrac{\left(2M_A+288\right).a}{\left(1885,5+2M_A\right).a}.100\%=16\%\\ \Leftrightarrow M_A=8,14\left(loại\right)\)
Không có kim loại thỏa
Đúng 0
Bình luận (0)
Cho 4g hỗn hợp hai chất là R( hoá trị 2) và M(hoá trị 3) tác dụng với 170 ml dung dịch HCl 2M a) tính khối lượng muối khan thu được
* Các bạn chỉ mình khối lượng của HCL là khối lượng chất tan đúng không , không phải dung dịch . Vì tính ra số mol HCl là số mol chất tan!
nHCl = 0,17.2 = 0,34 (mol) \(\Rightarrow\) mHCl = 0,34.36,5 = 12,41 (g)
PTHH : \(R+2HCl-->RCl_2+H_2\uparrow\) (1)
\(2M+6HCl-->2MCl_3+3H_2\uparrow\) (2)
Theo pthh (1) và (2) : nH2 = nHCl/2 = 0,17 (mol)
=> mH2 = 0,17.2 = 0,34 (g)
Theo ĐLBTKL : mhhKL + mHCl = mmuối khan + mH2
=> 4 + 12,41 = mmuối khan + 0,34
=> mmuối khan = 16,07 (g)
còn cách nữa tìm đc nHCl -> nCl , từ đó lấy mCl + mKL cũng ra kl muối khan
Đúng 0
Bình luận (3)
Hai bình điện phân: (
CuSO
4
/
Cu
và
AgNO
3
/
Ag
) mắc nối tiếp. Trong một mạch điện. Sau một thời gian điện phân, khối lượng catôt của hai bình tăng lên 2,8g. Biết đồng có khối lượng mol nguyên tử là 64 g/mol, hoá trị 2 và bạc có khối lượng mol nguyên tử là 108 g/mol, hoá trị 1.a) Tính điện lượng qua các bình điện phân và khối lượng Cu và Ag được giải phóng ở...
Đọc tiếp
Hai bình điện phân: ( CuSO 4 / Cu và AgNO 3 / Ag ) mắc nối tiếp. Trong một mạch điện. Sau một thời gian điện phân, khối lượng catôt của hai bình tăng lên 2,8g. Biết đồng có khối lượng mol nguyên tử là 64 g/mol, hoá trị 2 và bạc có khối lượng mol nguyên tử là 108 g/mol, hoá trị 1.
a) Tính điện lượng qua các bình điện phân và khối lượng Cu và Ag được giải phóng ở catôt.
b) Nếu cường độ dòng điện bằng 0,5 A. Tính thời gian điện phân.
a) m = m 1 + m 2 = 1 F . A 1 n 1 I t + 1 F . A 2 n 2 . I t = A 1 n 1 + A 2 n 2 . 1 F I t
⇒ q = I t = m F A 1 n 1 + A 2 n 2 = 2 , 8 . 96500 64 2 + 108 1 = 1930 ( C ) .
Khối lượng đồng được giải phóng ở catôt: m 1 = 1 F . A 1 n 1 q = 0 , 64 g
Khối lượng bạc được giải phóng ở catôt: m 2 = 1 F . A 2 n 2 q = 2 , 16 g
b) Thời gian điện phân: t = q I = 3860 s = 1 giờ 4 phút 20 giây.
Đúng 0
Bình luận (0)
Help me lập công thức hoá học của P hoá trị V vào O. từ đó tính phần trăm khối lượng của nguyên tố P có trong hợp chất đó. cho biết P = 31amu,O =16 amu
Gọi ct chung: \(P^V_xO^{II}_y\)
Theo qui tắc hóa trị: \(x.V=II.y=\dfrac{II}{V}\)
\(\Rightarrow x=2,y=5\)
\(\Rightarrow CTHH:P_2O_5\)
\(K.L.P.T_{P_2O_5}=31.2+16.5=142< amu>.\)
\(\%P=\dfrac{31.2.100}{142}\approx43,66\%\)
Đúng 4
Bình luận (0)
Help me
lập công thức hoá học của P hoá trị V và O. từ đó tính phần trăm khối lượng của nguyên tố P có trong hợp chất đó?
cho biết P = 31amu,O =16 amu
Đúng 0
Bình luận (0)
Các bạn chỉ mình chỗ khoanh màu đỏ có phải là số mol phản ứng từ số mol của H2 mà suy ra số mol của các chất khá ( số mol phản ứng ) đúng không ạ . Ở đây có cả cách nữa là dùng số mol phản ứng này để biết chất dư chất hết ạ

Ta thấy :
$2n_{H_2} = 0,04< n_{HCl} = 0,6$ nên HCl dư.
Đúng 1
Bình luận (0)
Một bình điện phân có anôt là
Ag
nhúng trong dung dịch
AgNO
3
, một bình điện phân khác có anôt là Cu nhúng trong dung dịch
CuSO
4
. Hai bình đó mắc nối tiếp nhau vào một mạch điện. Sau 2 giờ, khối lượng của cả hai catôt tăng lên 4,2 g. Tính cường độ dòng điện đi qua hai bình điện phân và khối lượng Ag và Cu bám vào catôt mỗi bình. Biết đồng có khối lượng mol nguyên tử là 64 g/mol, hoá trị...
Đọc tiếp
Một bình điện phân có anôt là Ag nhúng trong dung dịch AgNO 3 , một bình điện phân khác có anôt là Cu nhúng trong dung dịch CuSO 4 . Hai bình đó mắc nối tiếp nhau vào một mạch điện. Sau 2 giờ, khối lượng của cả hai catôt tăng lên 4,2 g. Tính cường độ dòng điện đi qua hai bình điện phân và khối lượng Ag và Cu bám vào catôt mỗi bình. Biết đồng có khối lượng mol nguyên tử là 64 g/mol, hoá trị 2 và bạc có khối lượng mol nguyên tử là 108 g/mol, hoá trị 1.
Ta có: m 1 = A 1 I t F n 1 ; m 2 = A 2 I t F n 2 ; m 1 + m 2 = ( A 1 n 1 + A 2 n 2 ) . I t F
⇒ I = ( m 1 + m 2 ) F A 1 n 1 + A 2 n 2 t = 0 , 4 A ; m 1 = A 1 I t F n 1 = 3 , 24 g ; m 2 = m - m 1 = 0 , 96 g
Đúng 0
Bình luận (0)
Mắc nối tiếp một bình điện phân chứa dung dịch đồng sunphat (
CuSO
4
) có anôt bằng đồng (Cu) với một bình điện phân chứa dung dịch bạc nitrat (
AgNO
3
) có anôt bằng bạc (Ag). Sau môt khoảng thời gian có dòng điện không đổi chạy qua hai bình này, thì khối lượng anôt của bình chứa dung dịch
CuSO
4
bị giảm bớt 2,3 g. Xác...
Đọc tiếp
Mắc nối tiếp một bình điện phân chứa dung dịch đồng sunphat ( CuSO 4 ) có anôt bằng đồng (Cu) với một bình điện phân chứa dung dịch bạc nitrat ( AgNO 3 ) có anôt bằng bạc (Ag). Sau môt khoảng thời gian có dòng điện không đổi chạy qua hai bình này, thì khối lượng anôt của bình chứa dung dịch CuSO 4 bị giảm bớt 2,3 g. Xác định khối lượng bạc tới bám vào catôt của bình chứa dung dịch AgNO 3 . Đồng có khối lượng mol là A1 = 63,5 g/mol và hoá trị n 1 = 2, bạc có khối lượng mol là A 2 = 108 g/mol và hoá trị n 2 = 1. Khối lượng bạc tới bám vào catot của bình chứa dung dịch AgNO 3 là
A. 0,67g B. 1,95g C. 2,66g D. 7,82g

















