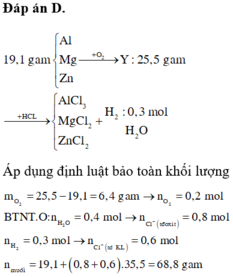
cho 19,1 hỗn hợp X(Mg,Al,Zn;biết tỉ lệ mol Al:Zn=2:1) phản ứng vừa đủ với 2 lít dd HNO3 xM sau phản ứng thu được hỗn hợp khí gồm 0,1 mol N2 và 0,05 mol N2O và dd Y/
a,% khối lượng của Mg trong X là
b,giá trị của x là

Những câu hỏi liên quan
Hỗn hợp X gồm Al, Mg, Zn. Cho 19,1 gam hỗn hợp X tác dụng với oxi, sau một thời gian thu được 25,5 gam chất rắn Y. Hòa tan hoàn tan Y trong dung dịch HCl dư, thu được 6,72 lít khí H2 (đktc) và dung dịch Z. Cô cạn Z, thu được m gam hỗn hợp muối khan, Giá trị của m là
\(19,1gam\) \(:\left\{{}\begin{matrix}Al\\Mg\\Zn\end{matrix}\right.\)\(\underrightarrow{+O_2}\)\(Y:25,5gam\)\(\underrightarrow{+HCl}\left\{{}\begin{matrix}AgCl_3\\MgCl_2\\ZnCl_2\end{matrix}\right.\) + H2 : 0,3 mol
H2O
Áp dụng định luật bảo toàn khối lượng:
\(mO_2=25,5-19,1=6,4gam\) \(\Rightarrow nO_2=0,2\left(mol\right)\)
BTNT O : nH2O = 0,4mol
\(\rightarrow nHCl^-\left(tdOxi\right)=0,8\left(mol\right)\)
\(nH_2=0,3\left(mol\right)\rightarrow nCl^-\left(tdKl\right)=0,6\left(mol\right)\)
\(m_{muối}=19,1+\left(0,8+0,6\right).35,5=68,8\left(g\right)\)
Đúng 2
Bình luận (4)
Hỗn hợp X gồm Al, Mg, Zn. Cho 19,1 gam hỗn hợp X tác dụng với oxi, sau một thời gian thu được 25,5 gam chất rắn Y. Hòa tan hoàn tan Y trong dung dịch HCl dư, thu được 6,72 lít khí H2 (đktc) và dung dịch Z. Cô cạn Z, thu được m gam hỗn hợp muối khan, Giá trị của m là
A. 47,5
B. 40,4.
C. 53,9.
D. 68,8.
Đáp án D.
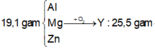
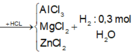
Áp dụng định luật bảo toàn khối lượng
![]()
![]()
![]()
→ n C l - ( t d o x i ) = 0 , 8 m o l
![]()
![]()
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Al, Mg, Zn. Cho 19,1 gam hỗn hợp X tác dụng với oxi, sau một thời gian thu được 25,5 gam chất rắn Y. Hòa tan hoàn tan Y trong dung dịch HCl dư, thu được 6,72 lít khí H2 (đktc) và dung dịch Z. Cô cạn Z, thu được m gam hỗn hợp muối khan, Giá trị của m là A. 47,5 B. 40,4. C. 53,9. D. 68,8.
Đọc tiếp
Hỗn hợp X gồm Al, Mg, Zn. Cho 19,1 gam hỗn hợp X tác dụng với oxi, sau một thời gian thu được 25,5 gam chất rắn Y. Hòa tan hoàn tan Y trong dung dịch HCl dư, thu được 6,72 lít khí H2 (đktc) và dung dịch Z. Cô cạn Z, thu được m gam hỗn hợp muối khan, Giá trị của m là
A. 47,5
B. 40,4.
C. 53,9.
D. 68,8.
Hỗn hợp X gồm Al, Mg, Zn. Cho 19,1 gam hỗn hợp X tác dụng với oxi, sau một thời gian thu được 25,5 gam chất rắn Y. Hòa tan hoàn toàn Y trong dung dịch HCl dư, thu được 6,72 lít khí H2 (đktc) và dung dịch Z. Cô cạn Z, thu được m gam hỗn hợp muối khan. Giá trị của m là A. 47,5 B. 40,4 C. 53,9 D. 68,8
Đọc tiếp
Hỗn hợp X gồm Al, Mg, Zn. Cho 19,1 gam hỗn hợp X tác dụng với oxi, sau một thời gian thu được 25,5 gam chất rắn Y. Hòa tan hoàn toàn Y trong dung dịch HCl dư, thu được 6,72 lít khí H2 (đktc) và dung dịch Z. Cô cạn Z, thu được m gam hỗn hợp muối khan. Giá trị của m là
A. 47,5
B. 40,4
C. 53,9
D. 68,8
cho 3,6g hỗn hợp X gồm Zn,Al,Fe,Mg. Trong đó số mol Mg=Tổng số mol 3 chất còn lại . Hòa tan hết X trong HCl thu được 2,464l H2. Mặt khác khi cho 3,6g X nói trên tác dụng với lượng dư Cl2 đun nóng thì thu được 11,765g hỗn hợp muối gồm AlCl3,FeCl3,ZnCl2 và MgCl2. Tính khối lượng mỗi loại có trong 3,6 gam X
Gọi số mol Zn, Al, Fe, Mg lần lượt là a;b;c;d
Ta có: $d=a+b+c;65a+27b+56c+24d=3,6$
Bảo toàn e ta có: $2a+3b+2c+2d=0,22$
Bảo toàn Zn, Al, Fe, Mg ta có: $136a+133,5b+162,5c+95d=11,765$
Giải hệ 4 ẩn ta được $a=b=0,02;c=0,01;d=0,05$
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 11,9 gam hỗn hợp X gồm Zn và Al vào dung dịch H2SO4 thu được 8,96 lít khí hiđro (đktc) và a gam hỗn hợp 2 muối.
a, Tính % khối lượng của Zn và Al trong hỗn hợp X?
b, Tính a?
(Biết H = 1, Fe = 56, Cu = 64, Zn = 65, Mg = 24, Ba = 137, O = 16, Al = 27, S = 32, Cl = 35,5)
2Al + 3H2SO4 →Al2(SO4)3 + 3H2 (1)
Zn + H2SO4 →ZnSO4 + H2 (2)
a;nH2=
Đúng 2
Bình luận (0)
Đốt cháy hết x gam hỗn hợp gồm Mg, Fe, Al, Zn thu được 28,1 hỗn hợp gam oxit. Cho hỗn hợp oxit này phản ứng vưa đủ với 200ml dd HCl 4M. Giá trị x là
\(n_{HCl}=0,2.4=0,8\left(mol\right)\)
=> \(n_{H_2O}=0,4\left(mol\right)\)
=> \(n_O=0,4\left(mol\right)\)
mkim loại = moxit - mO = 28,1 - 0,4.16 = 21,7 (g)
Đúng 4
Bình luận (0)
Câu IV.1. Cho 5,6g hỗn hợp Mg, Zn, Al tác dụng với 100g dung dịch HCl 25,55% . Hỗn hợp kim loại có bị hoà tan hết không? Vì sao?2. Nung 10,2g hỗn hợp Al, Mg, Na trong khí Oxi dư. Sau phản ứng kết thúc thu được 17g hỗn hợp chất rắn . Mặt khác cho hỗn hợp các kim loại trên tác dụng với dung dịch HCl dư thì thấy thoát ra V lít khí và dung dịch A. Cô cạn A thì thu được mg muối Clorua khan. Tính V và m ?
Đọc tiếp
Câu IV.
1. Cho 5,6g hỗn hợp Mg, Zn, Al tác dụng với 100g dung dịch HCl 25,55% . Hỗn hợp kim loại có bị hoà tan hết không? Vì sao?
2. Nung 10,2g hỗn hợp Al, Mg, Na trong khí Oxi dư. Sau phản ứng kết thúc thu được 17g hỗn hợp chất rắn . Mặt khác cho hỗn hợp các kim loại trên tác dụng với dung dịch HCl dư thì thấy thoát ra V lít khí và dung dịch A. Cô cạn A thì thu được mg muối Clorua khan. Tính V và m ?
1)
mHCl = 25,55.100/100=25,55(g)
=> nHCl = 25,55/36,5=0,7(mol)
Pt: Mg + 2HCl --> MgCl2 + H2
Zn + 2HCl --> ZnCl2 + H2
2Al + 6HCl --> 2AlCl3 + 3H2
+Giả sử trong hh chỉ có Mg
nMg = 5,624=0,235,624=0,23 mol
Pt: Mg +......2HCl
0,23 mol-> 0,46 mol < 0,7 (mol)
=> HCl dư
<=> Hh Mg, Zn, Al bị hòa tan hết
Đúng 1
Bình luận (0)
cho 5,6g hỗn hợp Mg, Zn, Al tác dụng với dung dịch có chứa 25,55g HCl. hỗn hợp kim loại có bị hòa tan hết không. vì sao
\(n_{HCl} = \dfrac{25,55}{36,5} = 0,7(mol)\\ M_{Mg} = 24 < M_{Al} = 27 < M_{Zn} = 65\\ \Rightarrow n_{\text{hỗn hợp max}} = n_{Mg} = \dfrac{5,6}{24} = \dfrac{7}{30}(mol)\\ Mg + 2HCl \to MgCl_2 + H_2\\ n_{HCl\ pư} = 2n_{Mg} = \dfrac{7}{15} = 0,467 < 0,7\\ \Rightarrow \text{Kim loại tan hết}\)
Đúng 1
Bình luận (0)