Sưu tầm tài liệu và trình bày về các ứng dụng của sulfuric acid trong các ngành sản xuất và đời sống. Vì sao sulfuric acid là hóa chất có tầm quan trọng bậc nhất?

Những câu hỏi liên quan
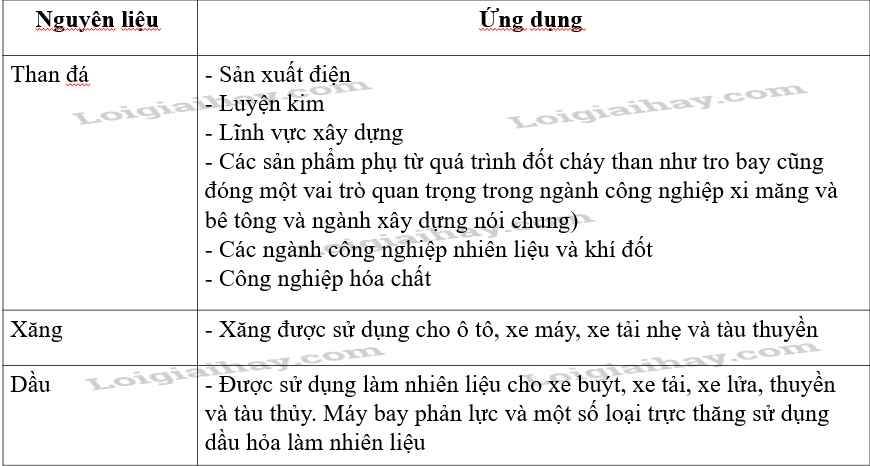
Than, xăng, dầu, … là nhiên liệu hoá thạch, được sử dụng chủ yếu cho các ngành sản xuất và hoạt động nào của con người? Em hãy sưu tầm hình ảnh và trình bày ứng dụng của các nhiên liệu này trong đời sống.
Than, xăng, dầu... là nhiên liệu hóa thạch, được sử dụng chủ yếu cho các ngành sản xuất và các hoạt động của con người như: dùng làm chất đốt, xăng dầu là nhiên liệu cho các phương tiện giao thông.
Ứng dụng của nhiên liệu trong đời sống:
Đúng 0
Bình luận (0)
Sulfuric acid là hoá chất hàng đầu trong nhiều ngành sản xuất, được mệnh danh là “máu” của các ngành công nghiệp. Sản lượng sulfuric acid của một quốc gia là một trong những chỉ số đánh giá sức mạnh công nghiệp hoá chất của quốc gia đó. Sulfuric acid có tính chất và ứng dụng gì trong đời sống?
- Tính chất của sulfuric acid:
+ Tính chất vật lí: chất lỏng sánh như dầu, không màu, không bay hơi, nặng gần gấp hai lần nước (H2SO4 98% có khối lượng riêng là 1,84 g/mL),
+ Tính chất hóa học:
• Dung dịch sulfuric acid loãng là một trong các acid mạnh và có đầy đủ tính chất của acid:
Đổi màu quỳ tím thành đỏ.
Tác dụng với kim loại hoạt động trong dãy hoạt động hoá học.
Tác dụng với basic oxide và base.
Tác dụng với nhiều muối.
• Dung dịch sulfuric acid đặc có tính oxi hoá mạnh và tính háo nước.
- Ứng dụng: dùng trong sản xuất phân bón, thuốc trừ sâu, chất tẩy rửa tổng hợp, tơ sợi hoá học, chất dẻo, sơn màu,...
Đúng 0
Bình luận (0)
Sử dụng Hình 8.1 để trình bày về các ứng dụng của sulfuric acid.
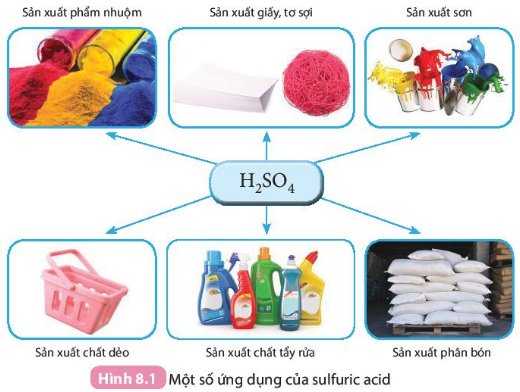
- Ứng dụng của sulfuric acid:
+ Sản xuất phẩm nhuộm
+ Sản xuất giấy, tơ sợi
+ Sản xuất sơn
+ Sản xuất chất dẻo
+ Sản xuất chất rửa tay
+ Sản xuất phân bón
Đúng 1
Bình luận (0)
Sưu tầm, tìm hiểu thông tin và trình bày một số ứng dụng của phenol trong đời sống và sản xuất.
Sản xuất phẩm nhuộm, sản xuất thuốc nổ (2,4,6 – trinitrophenol), chất diệt cỏ 2,4 – D (2,4 – dichlorophenoxyacetic acid); chất diệt nấm mốc (các đồng phân của nitrophenol),… Do có tính diệt khuẩn nên phenol được dùng làm chất khử trùng, tẩy uế.
Đúng 0
Bình luận (0)
Phân tử Sulfuric acid là 98 amu. Trong phân tử Sulfuric acid có 2H, 1S, 4O .
a. Tính nguyên tử khối của sulfr, Cho biết nguyên tử khối của H =1amu, O =16 amu
b. Phân tử Sulfuric acid là đơn chất hay hợp chất vì sao
\(\text{#TNam}\)
`a,` Gọi `NTK` của Sulfur là `x`
Ta có: `PTK= 2*1+x+16*4=98 <am``u>`
`2+x+64=98`
`-> 2+x=98-64`
`->2+x=34`
`-> x=34 - 2`
`-> x= 32 <am``u>`
Vậy, `NTK` của \(\text{Sulfur}\) là `32 am``u.`
`b,` Phân tử \(\text{Sulfuric acid}\) là hợp chất
Vì phân tử \(\text{Sulfuric acid}\) được cấu tạo từ `3` nguyên tố hóa học.
Đúng 3
Bình luận (0)
Sulfuric acid (H2SO4) là hóa chất hàng đầu được dùng trong nhiều ngành công nghiệp như: sản xuất sắt thép, dệt nhuộm, xử lý nước, bình ắc quy...a. Viết PTHH khi hòa tan hoàn toàn một lượng kim loại M( trong các hợp chất, M có hóa trị n ; n có thể là I, II, III) bằng dung dịch H2SO4 loãng vừa đủ.b. Khi phân tích thành phần muối sulfate ( SO4) thu được ở trên thì thấy M chiếm 20% về khối lượng. Hãy xác định kim loại M.
Đọc tiếp
Sulfuric acid (H2SO4) là hóa chất hàng đầu được dùng trong nhiều ngành công nghiệp như: sản xuất sắt thép, dệt nhuộm, xử lý nước, bình ắc quy...
a. Viết PTHH khi hòa tan hoàn toàn một lượng kim loại M( trong các hợp chất, M có hóa trị n ; n có thể là I, II, III) bằng dung dịch H2SO4 loãng vừa đủ.
b. Khi phân tích thành phần muối sulfate ( SO4) thu được ở trên thì thấy M chiếm 20% về khối lượng. Hãy xác định kim loại M.
a)
2M + nH2SO4 --> M2(SO4)n + nH2
b)
Có: \(\%M=\dfrac{2.M_M}{2.M_M+96n}.100\%=20\%\)
=> MM = 12n (g/mol)
Xét n = 2 thỏa mãn => MM = 24 (g/mol)
=> M là Mg
Đúng 2
Bình luận (0)
Trong Thí nghiệm 1, chất lỏng xuất hiện ở đáy cốc có phải là benzene không? Vì sao?Thí nghiệm 1. Nitro hóa Benzene Cho từ từ 2 mL dung dịch sulfuric acid đặc vào ống nghiệm đã chứa sẵn 1,5 mL dung dịch nitric acid đặc và làm lạnh trong chậu nước đá để tạo hỗn hợp nitro hóa. Nhỏ tiếp từ từ 1 mL benzene vào ống nghiệm và lắc ống nghiệm trong 6 đến 10 phút. Sau đó, rót từ từ hỗn hợp trong ống nghiệm vào cốc chứa 20 đến 30 ml nước lạnh (khoảng 0 °C - 10 °C). Dùng đũa thuỷ tinh khuấy đều hỗn hợp rồi...
Đọc tiếp
Trong Thí nghiệm 1, chất lỏng xuất hiện ở đáy cốc có phải là benzene không? Vì sao?
Thí nghiệm 1. Nitro hóa Benzene
Cho từ từ 2 mL dung dịch sulfuric acid đặc vào ống nghiệm đã chứa sẵn 1,5 mL dung dịch nitric acid đặc và làm lạnh trong chậu nước đá để tạo hỗn hợp nitro hóa. Nhỏ tiếp từ từ 1 mL benzene vào ống nghiệm và lắc ống nghiệm trong 6 đến 10 phút. Sau đó, rót từ từ hỗn hợp trong ống nghiệm vào cốc chứa 20 đến 30 ml nước lạnh (khoảng 0 °C - 10 °C). Dùng đũa thuỷ tinh khuấy đều hỗn hợp rồi để yên. Quan sát màu của chất lỏng ở đáy cốc.
- Trong Thí nghiệm 1, chất lỏng xuất hiện ở đáy cốc không phải là benzene (benzene không màu).
- Vì benzene phản ứng với dung dịch nitric acid tạo nitrobenzene có màu vàng nhạt .
PTHH: C6H6 + HNO3 → C6H5NO2 + H2O
Đúng 0
Bình luận (0)
Câu 4. Cho một lượng 5,6g Iron – sắt tác dụng với dung dịch Acid Sulfuric (H2SO4) sau phản ứng thuđược 0,1g khí hydrogen (H2) và 15,2g muối sắt (FeSO4).a. Viết phương trình chữ và phương trình hóa họcb. Tính khối lượng Acid sulfuric cần dùng cho phản ứng.Câu 5. Cho 0,2g khí hydrogen tác dụng với 16g Iron (III) oxide (Fe2O3), sau phản ứng thu được chất X và1,8g nướca. Tính khối lượng chất Xb. Xác định công thức của chất X, biết X là hợp chất gồm 2 nguyên tố Fe và O, biết phân tử khối củaX 80dvC....
Đọc tiếp
Câu 4. Cho một lượng 5,6g Iron – sắt tác dụng với dung dịch Acid Sulfuric (H2SO4) sau phản ứng thu
được 0,1g khí hydrogen (H2) và 15,2g muối sắt (FeSO4).
a. Viết phương trình chữ và phương trình hóa học
b. Tính khối lượng Acid sulfuric cần dùng cho phản ứng.
Câu 5. Cho 0,2g khí hydrogen tác dụng với 16g Iron (III) oxide (Fe2O3), sau phản ứng thu được chất X và
1,8g nước
a. Tính khối lượng chất X
b. Xác định công thức của chất X, biết X là hợp chất gồm 2 nguyên tố Fe và O, biết phân tử khối của
X < 80dvC.
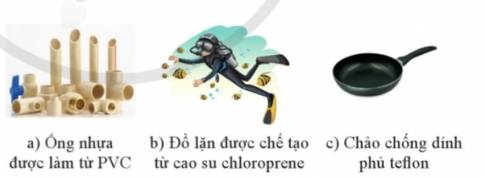
Sưu tầm tranh, ảnh, tài liệu minh hoạ cho các ứng dụng của dẫn xuất halogen trong thực tế cuộc sống.