Hòa tan 11,53g hỗn hợp gồm Ba , K vào lượng nước dư , sau phản ứng xảy ra hoàn toàn thu được dung dịch và 2,464 lít khí H2 điều kiện tiêu chuẩn . Khối lượng chất tan trong dung dịch là ? Giúp em với ạ , em cần gấp

Những câu hỏi liên quan
Hòa tan hoàn toàn 21,6 g hỗn hợp Fe và Fe2 O3 bằng dung dịch H2 SO4 loãng dư sau phản ứng thu được 2,24 lít khí H2 ở điều kiện tiêu chuẩn a viết các phương trình hóa học xảy ra .Tính %khối lượng từng chất trong hỗn hợp đều
a, PT: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
\(Fe_2O_3+3H_2SO_4\rightarrow Fe_2\left(SO_4\right)_3+3H_2O\)
b, Ta có: \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Theo PT: \(n_{Fe}=n_{H_2}=0,1\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,1.56}{21,6}.100\%\approx25,93\%\\\%m_{Fe_2O_3}\approx100-25,93=74,07\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
a, PT: Fe+H2SO4→FeSO4+H2��+�2��4→����4+�2
Fe2O3+3H2SO4→Fe2(SO4)3+3H2O��2�3+3�2��4→��2(��4)3+3�2�
b, Ta có: ⇒⎧⎪⎨⎪⎩%mFe=0,1.5621,6.100%≈25,93%%mFe2O3≈100−25,93=74,07%
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn 35 g hỗn hợp gồm Na,k, và Ba vào nước thu được dung dịch X và 22,4 lít khí H2 điều kiện tiêu chuẩn .Dung dịch Y gồm HCl và H2 SO4 với tỉ lệ mol tương ứng là 1:3 trung hòa dung dịch X bởi dung dịch Y tính tổng khối lượng các muối tạo thành
nH2 = 1 mol => nH+ cần trung hòa = 2nH2 = 2 mol
Gọi nH2SO4 = 3a mol => nHCl = a mol
=> nH+ = 3a.2 + a = 2 => a = \(\dfrac{2}{7}\)
=> nSO4= nH2SO4= 3.\(\dfrac{2}{7}\) = \(\dfrac{6}{7}\)mol; nCl = nHCl= \(\dfrac{2}{7}\) mol
Ta có
mmuối = mKim loại + mCl + mSO4
= 35 + \(\dfrac{2}{7}\).35,5 + \(\dfrac{6}{7}\).96 = 127,42 gam
Đúng 3
Bình luận (0)
Tham khảo :
nH2 = 1 mol => nH+ cần trung hòa = 2nH2 = 2 mol
Gọi nHCl = 3a mol => nH2SO4 = a mol
=> nH+ = 3a + 2a = 2 => a = 0,4
=> nCl = nHCl = 3.0,4 = 1,2 mol; nSO4 = nH2SO4 = 0,4 mol
Ta có mmuối = mKim loại + mCl + mSO4 = 35 + 1,2.35,5 + 0,4.96 = 116 gam
Đúng 0
Bình luận (4)
Hòa tan 21,9 gam hỗn hợp A gồm Na, Na2O, Ba, BaO vào nước dư, phản ứng hoàn toàn thu được dung dịch B chứa 20,52 gam Ba(OH)2 và có 1,12 lít khí thoát ra ở điều kiện tiêu chuẩn. Tính có khối lượng của dung dịch NaOH có trong dung dịch B.
\(n_{Ba\left(OH\right)_2}=\dfrac{20.52}{171}=0.12\left(mol\right)\)
\(n_{H_2}=\dfrac{1.12}{22.4}=0.05\left(mol\right)\)
\(n_{NaOH}=a\left(mol\right)\)
\(n_H=0.12\cdot2+a+0.05\cdot2=0.34+a\left(mol\right)\)
\(\Rightarrow n_{H_2O}=0.17+0.5a\left(mol\right)\)
\(BTKL:\)
\(21.9+\left(0.17+0.5a\right)\cdot18=20.52+40a+0.05\cdot2\)
\(\Rightarrow a=0.14\)
\(m_{NaOH}=0.14\cdot40=5.6\left(g\right)\)
Đúng 2
Bình luận (0)
Quy đôi A gồm : Na,Ba và O
n Ba = n Ba(OH)2 = 20,52/171 = 0,12(mol)
Gọi n Na = a(mol) ; n O = b(mol)
=> 23a + 16b + 0,12.137 = 21,9(1)
n H2 = 1,12/22,4 = 0,05(mol)
Bảo toàn e :
$Na^0 \to Na^+ + 1e$
$Ba^0 \to Ba^{+2} + 2e$
$O^0 + 2e \to O^{-2}$
$2H^+ 2e \to H_2$
=> a + 0,12.2 = 2b + 0,05.2(2)
Từ (1)(2) suy ra a = b = 0,14
n NaOH = n Na = 0,14 mol
=> m NaOH = 0,14.40 = 5,6(gam)
Đúng 1
Bình luận (0)
Tiến hành phản ứng nhiệt nhôm với Fe2O3 trong điều kiện không có không khí. Chia hỗn hợp sau phản ứng thành hai phần. Phần một có khối lượng 67 gam cho tác dụng với lượng dư dung dịch NaOH thấy có 16,8 lít H2 bay ra. Hòa tan phần hai bằng một lượng dư dung dịch HCl thấy có 84 lít H2 bay ra. Biết các phản ứng xảy ra hoàn toàn và các thể tích khí đo ở điều kiện tiêu chuẩn. Khối lượng Fe thu được trong quá trình nhiệt nhôm là A. 112 B. 84 C. 168 D. 56
Đọc tiếp
Tiến hành phản ứng nhiệt nhôm với Fe2O3 trong điều kiện không có không khí. Chia hỗn hợp sau phản ứng thành hai phần. Phần một có khối lượng 67 gam cho tác dụng với lượng dư dung dịch NaOH thấy có 16,8 lít H2 bay ra. Hòa tan phần hai bằng một lượng dư dung dịch HCl thấy có 84 lít H2 bay ra. Biết các phản ứng xảy ra hoàn toàn và các thể tích khí đo ở điều kiện tiêu chuẩn. Khối lượng Fe thu được trong quá trình nhiệt nhôm là
A. 112
B. 84
C. 168
D. 56
Đáp án A
Hỗn hợp rắn gồm Al, Al2O3, Fe với n Fe = 2 n Al 2 O 3 . Chia thành 2 phần không bằng nhau:
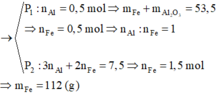
Đúng 0
Bình luận (0)
Tiến hành phản ứng nhiệt nhôm với Fe2O3 trong điều kiện không có không khí. Chia hỗn hợp sau phản ứng thành hai phần. Phần một có khối lượng 67 gam cho tác dụng với lượng dư dung dịch NaOH thấy có 16,8 lít H2 bay ra. Hòa tan phần hai bằng một lượng dư dung dịch HCl thấy có 84 lít H2 bay ra. Biết các phản ứng xảy ra hoàn toàn và các thể tích khí đo ở điều kiện tiêu chuẩn. Khối lượng Fe thu được trong quá trình nhiệt nhôm là A. 112. B. 84. C. 168. D. 56.
Đọc tiếp
Tiến hành phản ứng nhiệt nhôm với Fe2O3 trong điều kiện không có không khí. Chia hỗn hợp sau phản ứng thành hai phần. Phần một có khối lượng 67 gam cho tác dụng với lượng dư dung dịch NaOH thấy có 16,8 lít H2 bay ra. Hòa tan phần hai bằng một lượng dư dung dịch HCl thấy có 84 lít H2 bay ra. Biết các phản ứng xảy ra hoàn toàn và các thể tích khí đo ở điều kiện tiêu chuẩn. Khối lượng Fe thu được trong quá trình nhiệt nhôm là
A. 112.
B. 84.
C. 168.
D. 56.
Hòa tan 20 gam hỗn hợp Zn và Ag trong dung dịch H2SO4 loãng dư sau khi phản ứng xảy ra hoàn toàn thu được 3,36 lít khí điều kiện tiêu chuẩn .Phần trăm khối lượng của AG trong hỗn hợp là
\(n_{H_2}=\dfrac{3,36}{22,4}=0,15(mol)\\ PTHH:Zn+H_2SO_4\to ZnSO_4+H_2\\ \Rightarrow n_{Zn}=n_{H_2}=0,15(mol)\\ \Rightarrow \%_{Ag}=\dfrac{20-0,15.65}{20}.100\%=51,25\%\)
Đúng 0
Bình luận (0)
Hỗn hợp X gồm Na và Ba trong đó Na chiếm 14,375% về khối lượng. Hòa tan hoàn toàn m gam X vào nước thu được 1,344 lít khí H2 (đktc) và dung dịch Y. Hấp thụ hoàn toàn 2,016 lít khí CO2 (đktc) vào dung dịch Y. Các phản ứng xảy ra hoàn toàn. Khối lượng kết tủa thu được là: A. 7,88 gam B. 2,14 gam C. 5,91 gam D. 3,94 gam
Đọc tiếp
Hỗn hợp X gồm Na và Ba trong đó Na chiếm 14,375% về khối lượng. Hòa tan hoàn toàn m gam X vào nước thu được 1,344 lít khí H2 (đktc) và dung dịch Y. Hấp thụ hoàn toàn 2,016 lít khí CO2 (đktc) vào dung dịch Y. Các phản ứng xảy ra hoàn toàn. Khối lượng kết tủa thu được là:
A. 7,88 gam
B. 2,14 gam
C. 5,91 gam
D. 3,94 gam
Đáp án C
Ba+ 2H2O → Ba(OH)2+ H2
Na + H2O → NaOH + ½ H2
Đặt nBa = x mol; nNa = y mol → mhỗn hợp = 137x + 23y
→ % m N a = 23 y 137 x + 23 y . 100 % = 14 , 375 %
n H 2 = x+ ½ y =1,344/22,4 = 0,06mol ; n O H - = 2. n H 2 = 0,12 mol; n C O 2 = 0,09 mol
Giải hệ trên ta có: x = 0,04 mol; y = 0,04 mol
ta thấy : T = n O H - n C O 2 = 0 , 12 0 , 09 = 1 , 333 → CO2 phản ứng với OH- theo PT sau:
CO2 + OH- → HCO3-
a a a mol
CO2 + 2OH- → CO32- + H2O
b 2b b mol
Có n C O 2 = a+ b = 0,09 mol;
n O H - = a+ 2b = 0,12 suy ra a = 0,06 mol; b = 0,03 mol
Ba2+ + CO32- → BaCO3↓
0,04 0,03 mol 0,03 mol
m B a C O 3 = 0,03. 197 = 5,91(gam)
Đúng 0
Bình luận (1)
Hòa tan 2,78 gam hỗn hợp gồm nhôm và sắt tác dụng với dung dịch HCl dư. Sau khi phản ứng xảy ra hoàn toàn thu được 1,568 (lít) khí ở điều kiện tiêu chuẩn. Khối lượng của muối sắt thu được sau phản ứng là
Biết Al=27, Fe=56, H=1, S=32, O=16
A.2,54 gam
B.2,45 gam
C.5,08 gam
D.5,8 gam
\(n_{H_2}=\dfrac{1,568}{22,4}=0,07\left(mol\right)\)
Gọi số mol Al, Fe là a, b
=> 27a + 56b = 2,78
2Al + 6HCl --> 2AlCl3 + 3H2
a------------------------->1,5a
Fe + 2HCl --> FeCl2 + H2
b--------------->b----->b
=> 1,5a + b = 0,07
=> a = 0,02; b = 0,04
=> mFeCl2 = 0,04.127 = 5,08 (g)
=> C
Đúng 1
Bình luận (0)
Cho 20,16 lít khí CO phản ứng với một lượng oxit MxOy nung nóng. Sau khi phản ứng xảy ra hoàn toàn, thu được 25,2 gam kim loại M và hỗn hợp khí X. Cho toàn bộ lượng hỗn hợp khí X qua bình chứa dung dịch Ca(OH)2 dư tạo ra m gam kết tủa và có 6,72 lít khí thoát ra. Hòa tan hoàn toàn lượng kim loại trên trong dung dịch HCl dư, thấy thoát ra 10,08 lít khí H2. Xác định công thức oxit và tính m. Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
Đọc tiếp
Cho 20,16 lít khí CO phản ứng với một lượng oxit MxOy nung nóng. Sau khi phản ứng xảy ra hoàn toàn, thu được 25,2 gam kim loại M và hỗn hợp khí X. Cho toàn bộ lượng hỗn hợp khí X qua bình chứa dung dịch Ca(OH)2 dư tạo ra m gam kết tủa và có 6,72 lít khí thoát ra. Hòa tan hoàn toàn lượng kim loại trên trong dung dịch HCl dư, thấy thoát ra 10,08 lít khí H2. Xác định công thức oxit và tính m. Biết thể tích các khí đo ở điều kiện tiêu chuẩn.
Dung dịch Ca(OH)2 không hấp thụ khí CO nên 6,72 lít khí thoát ra chính là khí CO dư.

Đúng 0
Bình luận (0)

























