Thay .?. bằng l hay ml?

Trong mạch điện RLC thay đổi,giá trị của L có thể bằng 0 hay không?
Bằng cách nào để xác định sự thay đổi Kiểu hình là do ĐB hay Thường biến
Cho 5 gam kẽm viên vào cốc đựng 50ml dung dịch H2SO4 4M ở nhiệt độ thường ( 25 o C ). Có các tác động sau:
(a) Thay 5 gam kẽm viên bằng 5 gam kẽm bột.
(b) Thêm 50 ml dung dịch H2SO4 4M nữa.
(c) Thay 50 ml dung dịch H2SO4 4M bằng 100 ml dung dịch H2SO4 2M.
(d) Đun nóng dung dịch.
Số trường hợp tốc độ phản ứng không đổi là
A. 3
B. 1
C. 4
D. 2
A. Kẽm bột sẽ tiếp xúc với H2SO4 nhiều hơn nên tốc độ phản ứng nhanh hơn
B. Thêm 50 ml H2SO4 nhưng với nồng độ không đổi thì không làm thay đổi tốc độ phản ứng.
C. Thay bằng H2SO4 có nồng độ thấp hơn thì phản ứng sẽ xảy ra chậm hơn
D. Đun nóng dung dịch làm tốc độ phản ứng nhanh hơn
→ Đáp án B
cho 11,2 lít khí SO2 phản ứng với 200 ml dung dịch NaOH 2M
a,Nếu thay NaOH bằng Ca(OH)2 thì muối nào được tạo thành?Tính khối lượng?
Trung hòa 200ml dd H2SO4 1.5M bằng dd NaOH 20%
a. Tính KL dd NaOH
b. Nếu thay dd NaOH bằng dd KOH 5.6% có khối lượng riêng là D= 1.045g/ml thì phải dùng bao nhiêu ml KOH.
Đổi 200ml=0,2 l
nH2SO4= 0,2 * 1,5=0,3 mol
PTHH: 2NaOH + H2SO4 ---> Na2SO4 + 2H2O
0,6mol<--- 0,3mol
a)=> mNaOH(PƯ) = 0,6*40=24g
=> mNaOH(BĐ) = 24*100/20%=120g
b) PTHH: 2KOH + H2SO4 ---> K2SO4 + 2H2O
0,6mol<--- 0,3mol
=> mKOH(pư) = 0,6 * 56 = 33,6g
=> mKOH(BĐ) = 33,6*100/5,6% = 600g
=> VKOH= 600/1,045 = 574,16ml
( mk k chắc là đúng không nhưng theo công thức thì đúng ^.^)
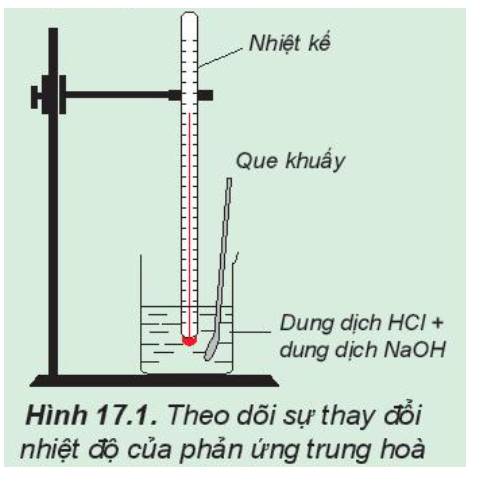
Theo dõi sự thay đổi nhiệt độ của phản ứng trung hòa
Chuẩn bị: dung dịch HCl 0,5 m, dung dịch NaOH 0,5 M, 1 cốc 150 mL, giá treo nhiệt kế, nhiệt kế (có dải đo đến 1000C), que khuấy và 2 ống đong 100 ml.
Tiến hành:
- Dùng ống đong lấy 50 mL dung dịch HCl 0,5 M cho vào cốc phản ứng, lắp nhiệt kế lên giá sao cho đầu nhiệt kế nhúng vào dung dịch trong cốc (Hình 17.1). Đọc nhiệt độ dung dịch.
- Dùng ống đong khác lấy 50 mL dung dịch NaOH 0,5M cho vào cốc phản ứng. Khuấy nhẹ.
Theo dõi sự thay đổi nhiệt độ của dung dịch và trả lời câu hỏi:
1. Nhiệt độ trên nhiệt kế thay đổi như thế nào sau khi rót dung dịch NaOH vào cốc?
Phản ứng trung hòa là tỏa nhiệt hay thu nhiệt?
2. Trong thí nghiệm trên, nếu thay các dung dịch HCl và NaOH bằng các dung dịch loãng hơn thì nhiệt độ thay đổi như thế nào so với thí nghiệm trên
1.
Phản ứng hóa học: NaOH + HCl → NaCl + H2O
Nhiệt độ đo được (HCl) lúc ban đầu thấp hơn so với nhiệt độ sau phản ứng
=> Phản ứng trung hòa là phản ứng tỏa nhiệt
2.
Trong thí nghiệm trên, nếu thay các dung dịch HCl và NaOH bằng các dung dịch loãng hơn thì nhiệt độ sau phản ứng vẫn tăng nhưng tăng ít hơn so với thí nghiệm trên.
các bạn giúp mình với
trung hòa 300 ml dd h2so4 1,5M bằng dung dịch naoh 40 %
A) tính khối lượng dung dịch naoh cần dùng
B) nếu thay đổi dung dịch naoh bằng koh 5.6% (1.045g/ml) thì khối lượng naoh là bao nhiêu
các bạn giải chi tiết nha
mình cảm ơn nhiều
a) nH2SO4 = 0,3.1,5 = 0,45 mol
H2SO4 + 2NaOH --> Na2SO4 + 2H2O
0,45 ---> 0,9
=>mNaOH = 0,9.40 = 36 g
=>mdd NaOH = (36.100)/40 = 90 g
b) H2SO4 + 2KOH --> K2SO4 + 2H2O
0,45 -----> 0,9
=>mKOH = 0,9.56 = 50,4 g
=> mddKOH = (50,4.100)/5,6 = 900 g
A) nH2SO4=0,3.1,5=0,45 (mol)
H2SO4+ 2NaOH➝ Na2SO4+H2O
0,45 0,9 0,45 (mol)
mNaOH = 0,9.40 = 36 (g)
m dd NaOH= \(\frac{36.100}{40}\) = 90 (g)
B) Không hiểu đề ![]() ..
..
Đem trung hòa 600ml dd HCl 1M bằng dd NaOH 30%.
a) Tính m dd NaOH đã dùng.
b) Nếu thay dd NaOH 30% bằng dd Ca(OH)2 7.351% ( D= 1.045g/ml ) thì V dd Ca(OH)2 cần dùng là bnh?
nHCl=CM.V=1.0,6=0,6(mol)
Pt: HCl+ NaOH-> NaCl + H2O
cứ:1.............1.............1 (mol)
vậy:0,6----->0,6------>0,6(mol)
=> mNaOH=0,6.40=24(g)
\(\Rightarrow m_{ddNaOH}=\dfrac{m_{NaOH}.100\%}{C\%}=\dfrac{24.100}{30}=80\left(g\right)\)
b) Nếu thay NaOH bằng Ca(OH)2 thì ta có PT:
PT: 2HCl + Ca(OH)2 -> CaCl2 +2H2O
Cứ:2................1.................1 (mol)
Vậy: 0,6------->0,3----------->0,3(mol)
=> mCa(OH)2=n.M=0,3.74=22,2(g)
\(\Rightarrow m_{ddCa\left(OH\right)_2}=\dfrac{m_{Ca\left(OH\right)_2}.100\%}{C\%}=\dfrac{22,2.100}{7,351}\approx302\left(g\right)\)
\(\Rightarrow V_{ddCa\left(OH\right)_2}=\dfrac{m_{ddCa\left(OH\right)_2}}{D}=\dfrac{302}{1,045}\approx289\left(ml\right)=0,289\left(lít\right)\)
CÁC BẠN ƠI!NGOÀI MI-LI-LÍT(ml),lít(l) CÒN CÁI NÀO NỮA KHÔNG?HAY HẾT?