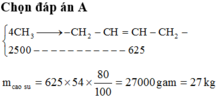Tính hiệu suất phản ứng, biết rằng từ 1,6 kg metan thì thu được 1,04 kg axetilen?

Những câu hỏi liên quan
Khi thực hiện phản ứng nhiệt phân metan điều chế axetilen thu được hỗn hợp X gồm axetilen, hiđro và metan chưa phản ứng hết. Tỉ khối của X so với H2 bằng 4,44. Tính hiệu suất của phản ứng.
Ta có: dhỗn hợp/H2 = 4,44 ⇒ Mhỗn hợp = 4,44.2 = 8,88
Gọi nCH4 ban đầu là là 1
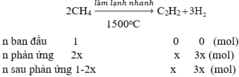
Tổng số mol khí sau phản ứng: 1 - 2x + x + 3x = 1 + 2x (mol)
MX = 2. 4,44 = 8,88
Áp dụng định luật bảo toàn khối lượng ta có:
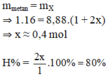
Đúng 0
Bình luận (0)
Cho sơ đồ tổng hợp cao su buna:Metan
→
Axetilen
→
Vinyl axetilen
→
Buta-1,3-đien
→
Cao su bunaTừ 40 kg metan có thể điều chế được bao nhiêu kg cao su buna (biết hiệu suất của cả quá trình bằng 80%)? A. 27 kg. B. 54 kg. C. 34 kg. D. 26 kg.
Đọc tiếp
Cho sơ đồ tổng hợp cao su buna:Metan → Axetilen → Vinyl axetilen → Buta-1,3-đien → Cao su buna
Từ 40 kg metan có thể điều chế được bao nhiêu kg cao su buna (biết hiệu suất của cả quá trình bằng 80%)?
A. 27 kg.
B. 54 kg.
C. 34 kg.
D. 26 kg.
Khi thực hiện phản ứng nhiệt phân metan điều chế axetilen thu được hỗn hợp X gồm axetilen, hidro và metan chưa phản ứng hết. Tỉ khối của X so với He bằng 2,22. Hiệu suất phản ứng trên là:
A. 81,18%.
B. 80,18%.
C. 49,01%.
D. 40,09%.
Phương trình hóa học: ![]()
Lấy số mol CH4 là 1 mol
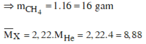
Sơ đồ phản ứng: 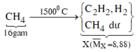
![]()
![]()
Theo (*) cứ 2 phân tử CH4 mất đi sẽ sinh ra 1 phân tử C2H2 và 3 phân tử H2
=> Số phân tử khí tăng = 1 + 3 – 2 = 2
=> Số phân tử khí tăng = Số phân tử khí CH4 mất đi.
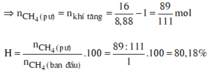
Đáp án B
Đúng 0
Bình luận (0)
Câu 8. Nung một tấn đá vôi thì thu được 478,8 kg vôi sống. Tính tỉ lệ phần trăm tạp chất trong đá vôi biết rằng hiệu suất của phản ứng nung vôi là 90%.
Ta có :
$n_{CaO} = \dfrac{478,8}{56} = 8,55(kmol)$
\(CaCO_3\xrightarrow[]{t^o}CaO+CO_2\)
8,55 8,55 (mol)
$n_{CaCO_3\ pư} = 8,55 : 90\% = 9,5(kmol)$
$m_{CaCO_3} = 9,5.100 = 950(kg)$
$m_{tạp\ chất} = 1000 - 950 = 50(kg)$
$\%m_{tạp\ chất} = \dfrac{50}{1000}.100\% = 5\%$
Đúng 1
Bình luận (0)
Khi điều chế axetilen bằng phương pháp nhiệt phân nhanh metan thu được hỗn hợp A gồm axetilen, hidro và một phần metan chưa phản ứng. Tỉ khối của hỗn hợp A so với hidro bằng 5. Vậy hiệu suất chuyển hóa metan thành axetilen là:
A. 50%
B. 60%
C. 70%
D. 80%
Đáp án B
Hướng dẫn Phương trình phản ứng:
2 C 2 H 4 → 1500 C 0 , l à m l ạ n h n h a n h C 2 H 2 + 3 H 2 B a n đ ầ u : 1 m o l P / ư : x s a u p / ư : 1 - x x 2 3 x 2
M - = 16 . ( 1 - x ) + 26 . x 2 . 2 . 3 x 2 1 - x + x 2 + 3 x 2
=> x = 0,6
=> Vậy hiệu suất chuyển hóa là 60%
Đúng 0
Bình luận (0)
Cho sắt tác dụng với oxygen tạo ra oxit sắt theo sơ đồ
Fe + O² -> Fe³O⁴
a)Tính hiệu suất của phản ứng khi đốt cháy 11kg Fe .biết lượng oxit sắt sau phản ứng là 200kg
b)Biết kg oxit sắt thu được sau phản ứng là 23,2kg;hiệu suất đạt 85%,hãy tính kg sắt đã tham gia phản ứng giúp vs ạ
PT: \(3Fe+2O_2\underrightarrow{t^o}Fe_3O_4\)
a, \(n_{Fe}=\dfrac{11}{56}\left(kmol\right)\)
Theo PT: \(n_{Fe_3O_4\left(LT\right)}=\dfrac{1}{3}n_{Fe}=\dfrac{11}{168}\left(kmol\right)\)
\(\Rightarrow m_{Fe_3O_4\left(LT\right)}=\dfrac{11}{168}.232=\dfrac{319}{21}\left(kg\right)\) > mFe3O4 (TT) = 200 (kg)
→ vô lý
Bạn xem lại đề phần a nhé.
b, \(n_{Fe_3O_4}=\dfrac{23,2}{232}=0,1\left(kmol\right)\)
Theo PT: \(n_{Fe\left(LT\right)}=3n_{Fe_3O_4}=0,3\left(kmol\right)\)
\(\Rightarrow m_{Fe\left(LT\right)}=0,3.56=16,8\left(kg\right)\)
Mà: H = 85%
\(\Rightarrow m_{Fe\left(TT\right)}=\dfrac{16,8}{85\%}=\dfrac{336}{17}\left(kg\right)\)
Đúng 1
Bình luận (0)
Trong công nghiệp, nhôm được sản xuất từ aluminium oxide (Al2O3) theo phương trình hoá học sau:a) Tính hiệu suất phản ứng khi điện phân 102 kg Al2O3, biết khối lượng nhôm thu được sau phản ứng là 51,3 kg.b*) Biết khối lượng nhôm thu được sau điện phân là 54 kg và hiệu suất phản ứng là 92%, tính khối lượng Al2O3 đã dùng.
Đọc tiếp
Trong công nghiệp, nhôm được sản xuất từ aluminium oxide (Al2O3) theo phương trình hoá học sau:

a) Tính hiệu suất phản ứng khi điện phân 102 kg Al2O3, biết khối lượng nhôm thu được sau phản ứng là 51,3 kg.
b*) Biết khối lượng nhôm thu được sau điện phân là 54 kg và hiệu suất phản ứng là 92%, tính khối lượng Al2O3 đã dùng.
\(2Al_2O_3\rightarrow\left(đpnc,criolit\right)4Al+3O_2\\ a,m_{Al\left(TT\right)}=\dfrac{4.27}{102.2}.102=54\left(kg\right)\\ H=\dfrac{51,3}{54}.100\%=95\%\\ b,m_{Al_2O_3\left(LT\right)}=\dfrac{102.2}{4.27}.54=102\left(kg\right)\\ m_{Al_2O_3\left(TT\right)}=\dfrac{102}{92\%}\approx110,87\left(kg\right)\)
Đúng 1
Bình luận (0)
HF được sản xuất bằng phản ứng giữa
C
a
F
2
và
H
2
S
O
4
. Dùng 6,00 kg
C
a
F
2
và
H
2
S
O
4
đặc, dư thu được 2,86 kg HF. Tính hiệu suất của phản ứng.
Đọc tiếp
HF được sản xuất bằng phản ứng giữa C a F 2 và H 2 S O 4 . Dùng 6,00 kg C a F 2 và H 2 S O 4 đặc, dư thu được 2,86 kg HF. Tính hiệu suất của phản ứng.
C a F 2 + H 2 S O 4 → 2HF↑ + C a S O 4 ↓
Theo phản ứng cứ 78,0 kg C a F 2 sẽ thu được 40,0 kg HF (hiệu suất 100%)
Nếu dùng 6 kg C a F 2 thì được:
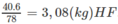
Vậy hiệu suất của phản ứng:
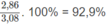
Đúng 0
Bình luận (0)
a) Từ 1 tấn nước mía chứa 12% saccarozo có thể thu được bao nhiêu Kg saccarozo , biết hiệu suất thu hồi đường là 80% b) Thủy phân 85,5 tấn saccarozơ (C12H22O11) trong dung dịch axit có đun nhẹ, thu được 36 tấn glucozơ. Tính hiệu suất của phản ứng thủy phân.
a)
m saccarozo = 1.12% = 0,12(tấn) = 120(kg)
b) 85,5 tấn = 85500(kg)
$C_{12}H_{22}O_{11} + H_2O \xrightarrow{t^o,H^+} C_6H_{12}O_6 + C_6H_{12}O_6$
Theo PTHH :
n saccarozo pư = n glucozo = 36.1000/180 = 200(kg)
Vậy :
H = 200.342/85500 .100% = 80%
Đúng 1
Bình luận (1)