Mô tả sự tạo thành liên kết trong phân tử chlorine bằng sự xen phủ của các AO.

Những câu hỏi liên quan
Vận dụng thuyết lai và sự xen phủ AO, mô tả sự hình thành liên kết trong các phân tử N2, CO2 (thẳng), C2H4 (góc HCH=1200) , BF3 (FBF=1200), NH3 (HNH=1070)
Các liên kết trong phân tử Nitơ được tạo thành là do sự xen phủ của : A. Các obitan s với nhau và các obitan p với nhau B. 3 obitan p với nhau C. 1 obitan s và 2 obitan p với nhau D. 3 obitan p giống nhau về hình dạng kích thước nhưng khác nhau về định hướng không gian với nhau
Đọc tiếp
Các liên kết trong phân tử Nitơ được tạo thành là do sự xen phủ của :
A. Các obitan s với nhau và các obitan p với nhau
B. 3 obitan p với nhau
C. 1 obitan s và 2 obitan p với nhau
D. 3 obitan p giống nhau về hình dạng kích thước nhưng khác nhau về định hướng không gian với nhau
Hãy mô tả sự hình thành liên kết cộng hóa trị trong phân tử khí chlorine, khí nitrogen
`Cl_2`
Mỗi nguyên tử `Cl` có `7e` ở lớp ngoài cùng. Để có cấu trúc electron bền vững giống khí hiếm `Ar`, `2` nguyên tử `Cl` đã liên kết với nhau bằng cách mỗi nguyên tử `Cl` góp chung `1e` ở lớp ngoài cùng tạo thành `1` cặp electron dùng chung.
`N_2`
Mỗi nguyên tử `N` có `5e` ở lớp ngoài cùng. Để có cấu trúc electron bền vững giống khí hiếm `Ne`,`2` nguyên tử `N` đã liên kết với nhau bằng cách mỗi nguyên tử `N` góp chung `3e` ở lớp ngoài cùng tạo thành `3` cặp electron dùng chung.
Đúng 2
Bình luận (0)
Sơ đồ sau mô tả sự hình thành liên kết cộng hóa trị trong phân tử HCl:
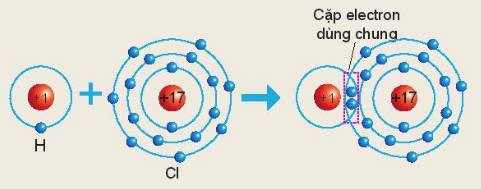
Xác định hóa trị của chlorine trong hợp chất trên
Nguyên tử `Cl` dùng chung `1` cặp electron với nguyên tử `H`
`->` Trong phân tử muối `HCl,` nguyên tử nguyên tố `Cl` sẽ có hóa trị là `I`.
Đúng 1
Bình luận (0)
đơn chất magnesium và đơn chất chlorine phản ứng với nhau tạo thành hợp chất magnesium chloride ,là hợp chất có cấu trúc tinh thể vẽ sơ đồ mô tả sự hình thành liên kết ion trong hợp chất MgCl2 từ các nguyên tử Mg và Cl . Cho biết số proton trong hạt nhân của Mg là 12 và của Cl là 17
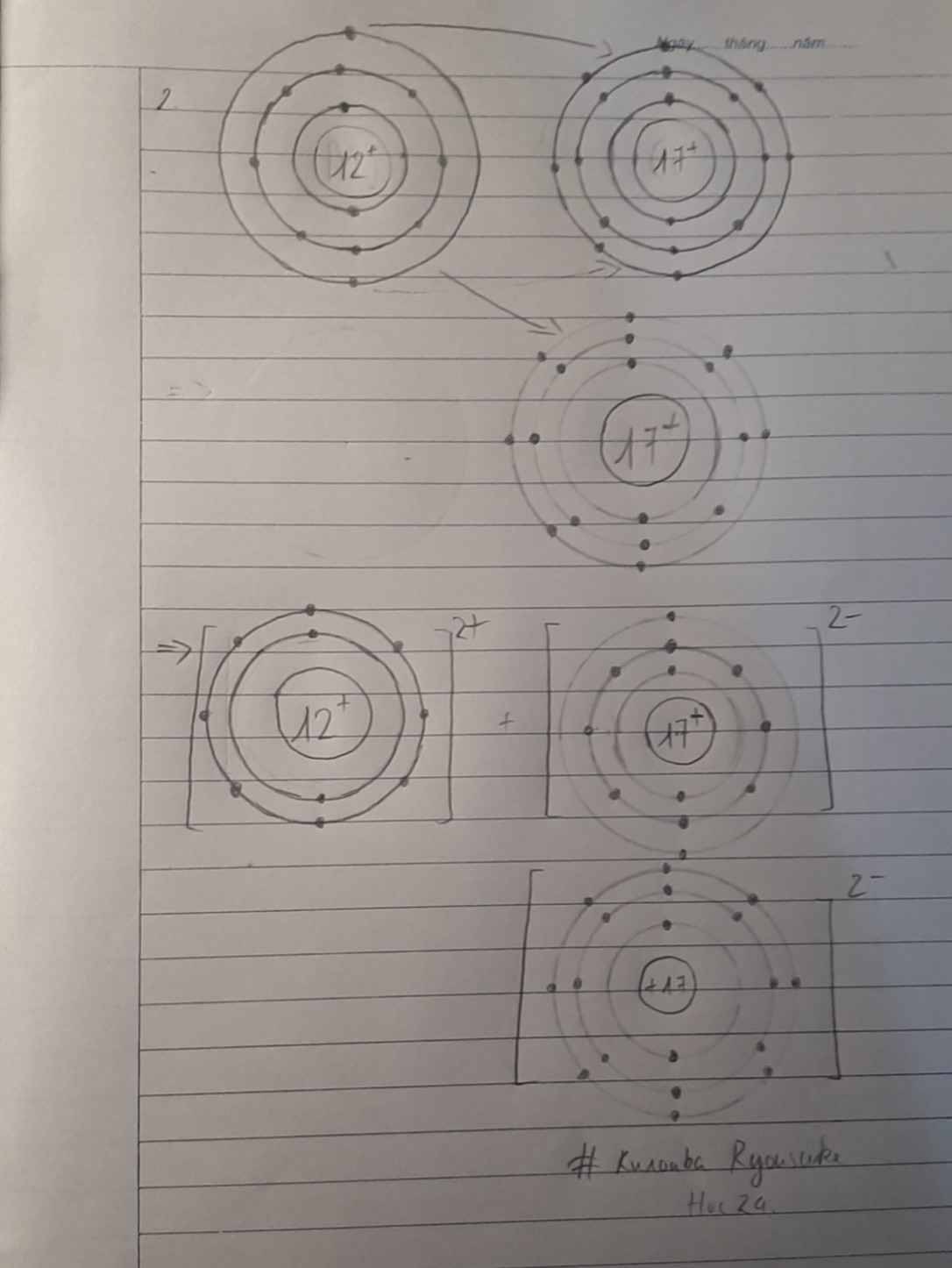
*chỉ vẽ sơ đồ thôi bạn nhỉ?
Đúng 5
Bình luận (7)
Mô tả sự tạo thành liên kết trong phân tử F2, HBr, HCl, C2H4, CO2, N2 theo quan điểm hình thành các cặp electron dùng chung
Viết ô orbital của lớp electron ngoài cùng cho nguyên tử N. Từ đó chỉ ra những AO nào có thể xen phủ tạo liên kết ba trong các phân tử N2.
Bước 1: Viết cấu hình electron và ô orbital của lớp electron ngoài cùng cho nguyên tử H, F
N (Z = 7): 1s22s22p3
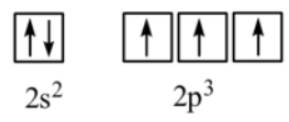
Bước 2: Chỉ ra các AO có thể xen phủ tạo liên kết ba trong phân tử N2.
Trong phân tử N2, liên kết ba được hình thành do:
- 2 AO p xen phủ trục tạo 1 liên kết .
- 4 AO p xen phủ bên tạo 2 liên kết .
Đúng 0
Bình luận (0)
Viết ô orbital của lớp electron ngoài cùng cho nguyên tử H và F. Từ đó chỉ ra những AO nào có thể xen phủ tạo liên kết đơn trong các phân tử H2, F2 và HF.
Tham khảo:
Bước 1: Viết cấu hình electron và ô orbital của lớp electron ngoài cùng cho nguyên tử H, F
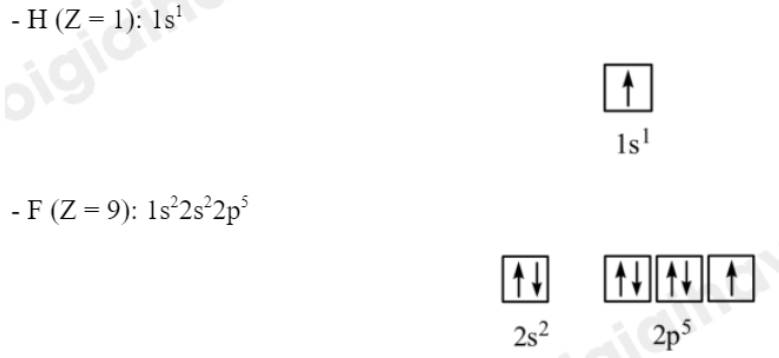
Bước 2: Chỉ ra các AO có thể xen phủ tạo liên kết đơn trong các phân tử H2, F2, HF.
- Trong phân tử H2: 2 AO s xen phủ trục tạo liên kết đơn.
- Trong phân tử F2: 2 AO p xen phủ trục tạo liên kết đơn.
- Trong phân tử HF: 1 AO s của H và 1 AO p của F xen phủ trục tạo liên kết đơn
Đúng 0
Bình luận (0)
Hãy mô tả sự hình thành liên kết cộng hóa trị trong phân tử carbon dioxide, ammonia (gồm một nguyên tử N liên kết với ba nguyên tử H)
`-` Khi hình thành liên kết cộng hóa trị trong phân tử `CO_2`, các nguyên tử đã liên kết với nhau như sau:
Mỗi nguyên tử `C` và `O` lần lượt có `12e` và `16e`. Để hình thành phân tử `CO_2`, nguyên tử `C` đã liên kết với `2` nguyên tử `O` bằng cách nguyên tử `C` góp chung với mỗi nguyên tử `O` là `2e` ở lớp ngoài cùng tạo thành các cặp electron dùng chung.
`NH_3`
Mỗi nguyên tử `N` và `H` lần lượt có `14e` và `1e`. Để hình thành phân tử ammonia, nguyên tử `N` liên kết với nguyên tử `H` bằng cách nguyên tử `N` góp chung với nguyên tử `H` là `1e` ở lớp ngoài cùng tạo thành `3` cặp electron dùng chung.
Đúng 2
Bình luận (0)














