Để giải thích sự hình thành liên kết Cl−Cl, có thể dựa vào cấu hình electron của mỗi nguyên tử clo:
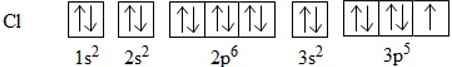
Sự hình thành liên kết giữa hai nguyên tử chlorine là do sự xen phủ giữa hai obitan p chứa electron độc thân của mỗi nguyên tử chlorine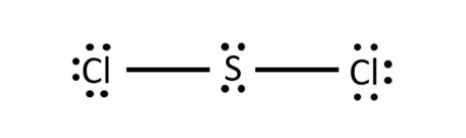
Để giải thích sự hình thành liên kết Cl−Cl, có thể dựa vào cấu hình electron của mỗi nguyên tử clo:

Sự hình thành liên kết giữa hai nguyên tử chlorine là do sự xen phủ giữa hai obitan p chứa electron độc thân của mỗi nguyên tử chlorine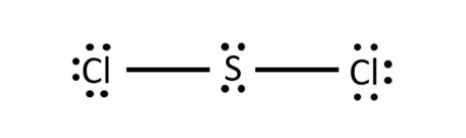
Quan sát các Hình từ 10.5 đến 10.8, cho biết liên kết nào trong mỗi phân tử được tạo thành bởi sự xen phủ trục hoặc xen phủ bên của các orbital.
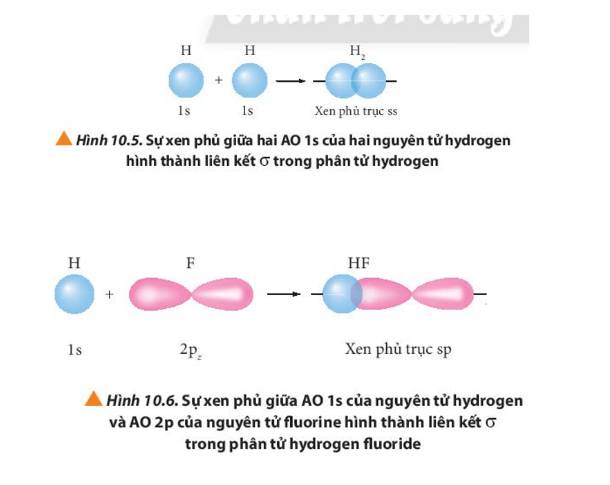
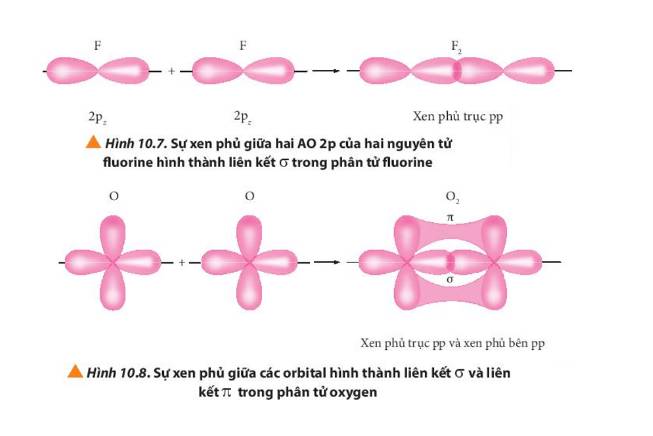
Sự xen phủ giữa hai orbital p trong trường hợp nào sẽ tạo thành liên kết σ? Trong trường hợp nào sẽ tạo thành liên kết п? Cho ví dụ.
Sự xen phủ có sự tham gia của orbital nào luôn là xen phủ trục?
Vẽ sơ đồ xen phủ orbital giữa 2 nguyên tử carbon hình thành liên kết đôi trong phân tử ethylene (C2H4).
Mô tả sự hình thành liên kết σ.
Mô tả sự hình thành liên kết п.
Hydrogen sulfide (H2S) và phosphine (PH3) đều là những chất có mùi khó ngửi và rất độc. Trình bày sự tạo thành liên kết cộng hóa trị trong phân tử các chất trên.
Trình bày sự hình thành liên kết cộng hóa trị trong phân tử Cl2.
Trình bày sự hình thành liên kết cộng hóa trị trong phân tử NH3.