Đề : Dùng khí hidro khử hoàn toàn 2.32 gam oxit kim loại X, thu được m gam kim loại và 0.04 mol hơi nước. Cho hết m kim loại vào dd HCl dư, thoát ra 0.672 lít khí H2( đktc). Xác định công thức của oxit

Những câu hỏi liên quan
Khử hoàn toàn 2.4 gam hỗn hợp gồm CuO và FexOy cùng số mol như nhau bằng H2 thu được 1.76 gam kim loại . Hòa tan kim loại đó bằng dung dịch HCL dư thấy thoát ra 0.448 lít khí H2 ( đktc ) . Xác định công thức của sắt oxit.
CuO + H2 => Cu +H2O
a => a => a
FexOy +yH2 => xFe + yH2O
a => ay => ax
Fe + 2Hcl => FeCl2 + h2
0,02 <= 0,02
Ta có n O p/ư= (2,4-1,76): 16=0,04= ay +y => a = 0,04/(y+1)
Mặt khác : ax= 0,02 => a =0,02/x
=> x = 2 , y =3
Fe2O3
Đúng 0
Bình luận (2)
Khối lượng chất rắn giảm chính là khối lượng oxi.
-->nO= (2,4 - 1,76)/16 = 0,04 mol -->mO=0,64(g)
Ta có nFe=nH2=0,02.-->mFe=1,12(g)
Ta có m(hỗn hợp BĐ)= mCu+mFe+mO=2,4
-->mcu= 0,64 -->nCu=0,01mol
Hỗn hợp ban đầu có: CuO: 0,01 mol
FexOy: a mol
Ta có nO=0,01+ya=0,04-->ya=0,03
nFe=xa=0,02
Ta có nFe/nO=2/3
Vậy oxit sắt là Fe2O3.
Đúng 1
Bình luận (0)
Khử hoàn toàn 2,784 gam một oxit kim loại bằng 1,344 lít CO (đktc), sau phản ứng thu được hỗn hợp khí có tỉ khối so với H2 là 20,4. Lấy toàn bộ lượng kim loại thoát ra cho vào dung dịch HCl dư thu được 806,4 ml H2(đktc). Xác định công thức của oxit kim loại đã dùng?
PTHH: AxOy + yCO --to--> xA + yCO2
Có: nCO(dư) + nCO2 = nCO(bd) = \(\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
Mà \(\dfrac{28.n_{CO\left(dư\right)}+44.n_{CO_2}}{n_{CO}+n_{CO_2}}=20,4.2=40,8\)
=> nCO2 = 0,048 (mol)
\(n_{A_xO_y}=\dfrac{2,784}{x.M_A+16y}\left(mol\right)\)
AxOy + yCO --to--> xA + yCO2
=> \(\left\{{}\begin{matrix}n_{CO_2}=\dfrac{2,784y}{x.M_A+16y}=0,048\left(mol\right)\left(1\right)\\n_A=\dfrac{2,784x}{x.M_A+16y}\left(mol\right)\end{matrix}\right.\)
(1) => \(M_A=\dfrac{42y}{x}=>\dfrac{y}{x}=\dfrac{M_A}{42}\) (2)
PTHH: 2A + 2nHCl --> 2ACln + nH2
=> \(n_{H_2}=\dfrac{1,392xn}{x.M_A+16y}=0,036\left(mol\right)\)
=> \(1,392n=0,036.M_A+\dfrac{0,576y}{x}\) (3)
(2)(3) => MA = 28n
Xét n = 1 => L
Xét n = 2 => MA = 56 (Fe) => \(\dfrac{x}{y}=\dfrac{3}{4}\) => CTHH: Fe3O4
Đúng 1
Bình luận (0)
Xin cảm ơn mọi người đã đọc câu hỏi này nhưng em đã nghĩ ra đáp án cho bài tập này rồi ạ
Đúng 0
Bình luận (0)
Khử hoàn toàn 24 gam Oxit của một kim loại hóa trị II cần dùng hết 6,72 lít khí Hidro( đktc) ở nhiệt độ cao thu được kim loại và nước. Xác định kim loại, Công thức Oxit và gọi tên Oxít trên
Gọi CTHH oxit là RO
\(n_{H_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: RO + H2 --to--> R + H2O
0,3<-0,3
=> \(M_{RO}=\dfrac{24}{0,3}=80\left(g/mol\right)\)
=> MR = 64 (g/mol)
=> R là Cu
CTHH của oxit là CuO (đồng(II) oxit)
Đúng 2
Bình luận (0)
gọi cthh là R
nH2 = 6,72 : 22,4 = 0,3 (mol)
pthh : RO + H2 -t--> R +H2O
0,3<-0,3 (mol)
=> M Oxit = 24 : 0,3 = 80 (g/mol)
=> M R = 80 - 16 = 64 (g/mol )
=> R là Cu
=> CTHH của Oxit là CuO ( đồng (!!) Oxit)
Đúng 0
Bình luận (0)
Gọi công thức của oxit cần tìm là RO.
RO (0,3 mol) + H2 (0,3 mol) \(\underrightarrow{t^o}\) R + H2O.
Phân tử khối của oxit là 24/0,3=80 (g/mol).
Kim loại và công thức của oxit lần lượt là đồng (Cu) và CuO (đồng (II) oxit).
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
Khử 3,48 gam một oxit kim loại M cần dùng 1,344 lít khí hiđro (ở đktc). Toàn bộ lượng kim loại thu được tác dụng với dung dịch HCl dư cho 1,008 lít khí hiđro (ở đktc). Xác định kim loại M và công thức hóa học của oxit trên?
CTHH: AxOy
\(n_{H_2}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\)
PTHH: AxOy + yH2 --to--> xA + yH2O
\(\dfrac{0,06}{y}\)<--0,06---->\(\dfrac{0,06x}{y}\)
2A + 2nHCl --> 2ACln + nH2
\(\dfrac{0,06x}{y}\)---------------->\(\dfrac{0,03xn}{y}\)
=> \(\dfrac{0,03xn}{y}=\dfrac{1,008}{22,4}=0,045\left(mol\right)\)
=> \(\dfrac{y}{x}=\dfrac{2}{3}n\)
\(M_{A_xO_y}=\dfrac{3,48}{\dfrac{0,06}{y}}=58y\left(g/mol\right)\)
=> \(x.M_A=42y\)
=> \(M_A=\dfrac{42y}{x}=28n\left(g/mol\right)\)
Xét n = 2 thỏa mãn => MA = 56 (g/mol)
=> A là Fe
\(\dfrac{x}{y}=\dfrac{3}{2n}=\dfrac{3}{4}\) => CTHH: Fe3O4
Đúng 4
Bình luận (0)
Hòa tan hoàn toàn 4 gam hỗn hợp gồm Fe và một kim loại M có hóa trị II trong hợp chất vào dd HCl dư thu được 2,24l khí H2 ( đktc).Nếu chỉ dùng 2,4 gam kim loại M trên cho vào dd HCl thì dùng không hết 0,5 mol HCl. Xác định kim loại M.
\(Fe\left(x\right)+2HCl\left(2x\right)\rightarrow FeCl_2+H_2\left(x\right)\)
\(M\left(y\right)+2HCl\left(2y\right)\rightarrow MCl_2+H_2\left(y\right)\)
Gọi số mol của Fe, M lần lược là x,y thì ta có
\(56x+My=4\left(1\right)\)
\(n_{H_2}=\frac{2,24}{22,4}=0,1\)
\(\Rightarrow x+y=0,1\left(2\right)\)
Nếu chỉ dùng 2,4 g M thì
\(n_{HCl}=2n_M=\frac{2.2,4}{M}=\frac{4,8}{M}< 0,5\left(3\right)\)
Từ (1), (2), (3) ta có hệ: \(\left\{\begin{matrix}56x+My=4\\x+y=0,1\\\frac{4,8}{M}< 0,5\end{matrix}\right.\)
\(\Leftrightarrow\left\{\begin{matrix}56\left(0,1-y\right)+My=4\\x=0,1-y\\\frac{4,8}{M}< 0,5\end{matrix}\right.\)
\(\Leftrightarrow\left\{\begin{matrix}y\left(56-M\right)=1,6\\x=0,1-y\\M>9,6\end{matrix}\right.\)
\(\Rightarrow9,6< M< 56\)
Tới đây thì chọn kim loại nào có hóa trị II mà nằm trong khoản đó và kiểm tra thỏa mãn hệ phương trình là xong.
Đúng 1
Bình luận (8)
Hung Nguyen: giải thích hộ mình ở chỗ dấu ngoặc nhọn thứ 2 đc ko. mình ko hiểu từ dấu ngoặc nhọn thứ nhất làm thế nào để ra đc dấu ngoặc nhọn thứ 2. cảm ơn trước nha ![]()
Đúng 0
Bình luận (2)
Dùng khí H2 dư khử hoàn toàn 2,4 gam hỗn hợp CuO và FexOy có số mol như nhau thu được hỗn hợp 2 kim loại. Hòa tan hỗn hợp kim loại này bằng dung dịch HCl dư, thoát ra 448cm3 H2 (đkt). Xác định công thức phân tử của oxit sắt.
Gọi \(\left\{{}\begin{matrix}n_{CuO}=a\left(mol\right)\\n_{Fe_xO_y}=a\left(mol\right)\end{matrix}\right.\)
=> 80a + 56ax + 16ay = 2,4 (1)
\(n_{H_2}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
FexOy + yH2 --to--> xFe + yH2O
a---------------->ax
Fe + 2HCl --> FeCl2 + H2
ax--------------------->ax
=> \(ax=0,02\left(mol\right)\)
=> a = \(\dfrac{0,02}{x}\)
Thay vào (1)
\(80.\dfrac{0,02}{x}+56.0,02+\dfrac{16.0,02y}{x}=2,4\)
=> \(\dfrac{1,6}{x}+\dfrac{0,32y}{x}=1,28\)
=> 1,28x = 0,32y + 1,6
Chọn x = 2; y = 3 thỏa mãn
=> CTHH: Fe2O3
Đúng 1
Bình luận (0)
khử 3,48 gam oxit một kim loại M cần dùng 1,344 lít H2(đktc). Toàn bộ lượng kim loại thu được cho tác dụng với dd HCl dư thu được 1,008 lít H2(đktc). Xác định M và oxit của nó.
Đặt a là hoá trị kim loại M cần tìm (a: nguyên, dương)
\(M_2O_a+aH_2\rightarrow\left(t^o\right)2M+aH_2O\left(1\right)\\ 2M+2aHCl\rightarrow2MCl_a+aH_2\left(2\right)\\Ta.có:n_{H_2\left(2\right)}=\dfrac{1,008}{22,4}=0,045\left(mol\right)\\ n_{H_2\left(1\right)}=\dfrac{1,344}{22,4}=0,06\left(mol\right)\\ \Rightarrow n_{O\left(trong.oxit\right)}=n_{H_2O}=n_{H_2\left(1\right)}=0,06\left(mol\right)\\ \Rightarrow m_M=3,48-0,06.16=2,52\left(g\right)\\ n_{H_2\left(2\right)}=0,045\left(mol\right)\\ \Rightarrow n_{M\left(2\right)}=\dfrac{0,045.2}{a}=\dfrac{0,09}{a}\left(mol\right)\\ \Rightarrow M_M=\dfrac{2,52}{\dfrac{0,09}{a}}=28a\left(\dfrac{g}{mol}\right)\)
Xét các TH: a=1; a=2; a=3; a=8/3 thấy a=2 thoả mãn khi đó MM=56(g/mol), tức M là Sắt (Fe=56)
Đặt CTTQ của oxit sắt cần tìm là FemOn (m,n: nguyên, dương)
\(n_{Fe}=\dfrac{2,52}{56}=0,045\left(mol\right)\\n_O=0,06\left(mol\right)\)
=> m:n= 0,045:0,06=3:4
=>m=3;n=4
=> CTHH oxit: Fe3O4 (Sắt từ oxit)
Đúng 1
Bình luận (2)
Khử hoàn toàn 4,06 gam một oxit kim loại bằng khí CO ở nhiệt độ cao thành kim loại. Dẫn toàn bộ khí sinh ra vào bình đựng dung dịch Ca(OH)2 (dư) tạo thành 7,00 gam kết tủa. Nếu lấy lượng kim loại sinh ra hòa tan hết vào dung dịch HCl (dư) thì thu được 1,176 lít khí H2 (đktc). Công thức của oxit kim loại là A. FeO. B. CrO. C. Fe2O3. D. Fe3O4
Đọc tiếp
Khử hoàn toàn 4,06 gam một oxit kim loại bằng khí CO ở nhiệt độ cao thành kim loại. Dẫn toàn bộ khí sinh ra vào bình đựng dung dịch Ca(OH)2 (dư) tạo thành 7,00 gam kết tủa. Nếu lấy lượng kim loại sinh ra hòa tan hết vào dung dịch HCl (dư) thì thu được 1,176 lít khí H2 (đktc). Công thức của oxit kim loại là
A. FeO.
B. CrO.
C. Fe2O3.
D. Fe3O4
Gọi công thức oxit ban đầu là MxOy.
Có phản ứng khử hoàn toàn oxit MxOy thành kim loại:
![]()
Dẫn khí CO2 sinh ra hấp thụ vào dung dịch Ca(OH)2 dư:
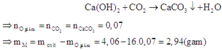
Cần lưu ý: Hóa trị của kim loại M trong oxit ban đầu và hóa trị của M trong sản phẩm của phản ứng giữa M với axit HCl có thể khác nhau.
Do đó ta gọi n là hóa trị của M thể hiện khi phản ứng với axit HCl.
![]()
Áp dụng định luật bào toàn mol electron, ta có:
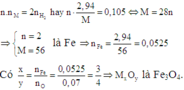
Đáp án D.
Đúng 1
Bình luận (0)
khử hoàn toàn 2,552 gam một oxit kim loại cần 985,6 ml H2 (đktc), lấy toàn bộ lượng kim loại thoát ra cho vào dung dịch HCl dư thu được 739,2 ml H2 (đktc). Xác định oxit của oxit kim loại đã dùng?
Giải giúp tui nha tui giải nó ko có ra
CTHH: RxOy
\(n_{H_2}=\dfrac{0,9856}{22,4}=0,044\left(mol\right)\)
PTHH: RxOy + yH2 --to--> xR + yH2O
\(\dfrac{0,044}{y}\)<-0,044--->\(\dfrac{0,044x}{y}\)
=> \(M_{R_xO_y}=x.M_R+16y=\dfrac{2,552}{\dfrac{0,044}{y}}=58y\left(g/mol\right)\)
=> \(M_R=\dfrac{42y}{x}\left(g/mol\right)\) (1)
Gọi hóa trị của R trong hợp chất muối clorua là n
\(n_{H_2}=\dfrac{0,7392}{22,4}=0,033\left(mol\right)\)
PTHH: 2R + 2nHCl --> 2RCln + nH2
\(\dfrac{0,066}{n}\)<------------------0,033
=> \(\dfrac{0,066}{n}=\dfrac{0,044x}{y}\)
=> \(\dfrac{y}{x}=\dfrac{2n}{3}\) (2)
(1)(2) => MR = 28n (g/mol)
- Nếu n = 1 => Loại
- Nếu n = 2 => MR = 56 (g/mol) --> Fe
- Nếu n = 3 => Loại
Vậy R là Fe
\(\dfrac{x}{y}=\dfrac{3}{4}\) => CTHH: Fe3O4
Đúng 3
Bình luận (3)
Bài 24*: Khử hoàn toàn m gam một oxit sắt cần dùng 5,376 lít khí H2 (đktc), thu lấy kim loại sắt sinh ra cho tác dụng với dung dịch HCl dư thì thấy thoát ra 4,032 lít H2 (đktc). Tìm công thức hóa học của oxit sắt và tính giá trị m. Biết phản ứng của Fe với dung dịch HCl tạo ra muối sắt (II).
\(CT:Fe_xO_y\)
\(Fe_xO_y+yH_2\underrightarrow{^{t^o}}xFe+yH_2O\left(1\right)\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\left(2\right)\)
\(n_{Fe}=n_{H_2\left(2\right)}=\dfrac{4.032}{22.4}=0.18\left(mol\right)\)
\(n_{H_2\left(1\right)}=\dfrac{y}{x}\cdot n_{Fe}=\dfrac{5.376}{22.4}=0.24\left(mol\right)\)
\(\Leftrightarrow\dfrac{y}{x}\cdot0.18=0.24\)
\(\Leftrightarrow\dfrac{x}{y}=\dfrac{3}{4}\)
\(CT:Fe_3O_4\)
\(m_{Fe_3O_4}=\dfrac{0.18}{3}\cdot232=13.92\left(g\right)\)
Đúng 1
Bình luận (0)


























