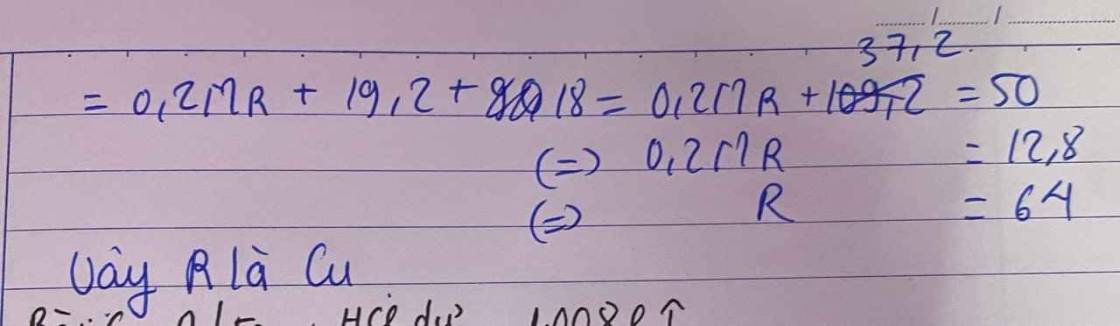Hoà tan sắt II sunfua vào dd HCl thu được khí A đốt hoàn toàn khí A thu được khí C có mùi hắc. Khí A,C lần lượt là?

Những câu hỏi liên quan
Đốt cháy m gam đồng (II) sunfua trong khí oxi dư, thu được chất rắn X có khối lượng bằng (m – 4,8) gam. Nung X trong khí CO dư tới khối lượng không đổi, thu được chất rắn Y. Hoà tan Y trong dung dịch
HNO
3
loãng dư, thu được V lít một chất khí Z (đktc) không màu, hóa nâu đỏ trong không khí. Các phản ứng xảy ra hoàn toàn. Giá trị của m và V lần lượt là A. 28,80 và 4,48. B. 19,20 và 2,24. C. 19,20 và 4,48. D. 28,80 và 2,24.
Đọc tiếp
Đốt cháy m gam đồng (II) sunfua trong khí oxi dư, thu được chất rắn X có khối lượng bằng (m – 4,8) gam. Nung X trong khí CO dư tới khối lượng không đổi, thu được chất rắn Y. Hoà tan Y trong dung dịch HNO 3 loãng dư, thu được V lít một chất khí Z (đktc) không màu, hóa nâu đỏ trong không khí. Các phản ứng xảy ra hoàn toàn. Giá trị của m và V lần lượt là
A. 28,80 và 4,48.
B. 19,20 và 2,24.
C. 19,20 và 4,48.
D. 28,80 và 2,24.
Đốt cháy hoàn toàn 17,92 lít khí H2 đktc trong 15,68 lít O2 đktc. Ngưng tụ sản phẩm thu được chất lỏng A và khí B. Cho toàn bộ khí B pư hết với 16,2g Al, thu được hỗn hợp chất rắn C. Hoà tan hoàn toàn chất rắn C trong dung dịch có chứa 73g HCl thu được dung dịch D và khí E. Xác định các chất trong A,B,C,D và E. Tính khối lượng các chất trong A, C và số mol các chất trong dd DBiết: Al2O3 + 6HCl -- 2AlCl3 + 3H2O
Đọc tiếp
Đốt cháy hoàn toàn 17,92 lít khí H2 đktc trong 15,68 lít O2 đktc. Ngưng tụ sản phẩm thu được chất lỏng A và khí B. Cho toàn bộ khí B pư hết với 16,2g Al, thu được hỗn hợp chất rắn C. Hoà tan hoàn toàn chất rắn C trong dung dịch có chứa 73g HCl thu được dung dịch D và khí E.
Xác định các chất trong A,B,C,D và E. Tính khối lượng các chất trong A, C và số mol các chất trong dd D
Biết: Al2O3 + 6HCl --> 2AlCl3 + 3H2O
Hòa tan hoàn toàn 17,6 g sắt (II) sunfua vào dd HCl dư rồi đem toàn bộ khí sinh ra vào 92,3 g nước thu được dd X.
a) Tính nồng độ % dd X
b) Cần bao nhiêu gam dd NaOH 20% phản ứng hết 1/2 dd X. Biết tạo muối trung hòa
\(FeS+2HCl\rightarrow FeCl_2+H_2S\)\(\uparrow\)
0.2 0.2
\(H_2S+4H_2O\rightarrow H_2SO_4+4H_2\)
0.2 0.2 0.8
a. \(n_{FeS}=\dfrac{17.6}{88}=0.2mol\)
\(mdd_{H_2SO_4}=m_X=m_{H_2S}+m_{H_2O}-m_{H_2}=0.2\times34+92.3-0.8\times2=97.5g\)
\(C\%_{H_2SO_4}=\dfrac{0.2\times98\times100}{97.5}=20,1\%\)
b. \(\dfrac{1}{2}dd_X\Rightarrow n_X=0.1mol\)
\(2NaOH+H_2SO_4\rightarrow Na_2SO_4+2H_2O\)
0.2 0.1
\(mdd_{NaOH}=\dfrac{0.2\times40\times100}{20}=40g\)
Đúng 1
Bình luận (0)
Khử hoàn toàn m gam một oxit sắt phải dùng vừa đủ 0,672 lít khí H2 (đktc). Đem toàn bộ lượng sắt thu được hoà tan 300g dd HcL 7,3% thu được 0,448 lít H2(đktc) và dd A
a. Tìm oxit sắt
b. Tính C% của các chất trong dd A
PTHH: \(Fe_xO_y+yH_2\xrightarrow[]{t^o}xFe+yH_2O\) (1)
\(Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\) (2)
a) Ta có: \(\left\{{}\begin{matrix}n_O=n_{H_2O}=n_{H_2\left(1\right)}=\dfrac{0,672}{22,4}=0,03\left(mol\right)\\n_{Fe}=n_{H_2\left(2\right)}=\dfrac{0,448}{22,4}=0,02\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(n_{Fe}:n_O=x:y=0,02:0,03=2:3\)
\(\Rightarrow\) CTHH của oxit là Fe2O3
b) Theo PTHH: \(\left\{{}\begin{matrix}n_{FeCl_2}=n_{H_2}=0,02\left(mol\right)\\n_{HCl\left(dư\right)}=\dfrac{300\cdot7,3\%}{36,5}-2n_{H_2}=0,56\left(mol\right)\end{matrix}\right.\)
Mặt khác: \(m_{dd\left(sau.p/ứ\right)}=m_{Fe}+m_{ddHCl}-m_{H_2}=0,02\cdot56+300-0,02\cdot2=301,08\left(g\right)\)
\(\Rightarrow\left\{{}\begin{matrix}C\%_{FeCl_2}=\dfrac{0,02\cdot127}{301,08}\cdot100\%\approx0,84\%\\C\%_{HCl\left(dư\right)}=\dfrac{0,56\cdot36,5}{301,08}\cdot100\%\approx6,79\%\end{matrix}\right.\)
Đúng 5
Bình luận (7)
a)
n HCl = 300.7,3%/36,5 = 0,6(mol)
n H2 = 0,448/22,4 = 0,02(mol)
$Fe + 2HCl \to FeCl_2 + H_2$
n HCl > 2n H2 nên HCl dư
$n_{Fe} = n_{H_2} = 0,02(mol)$
$H_2 + O_{oxit} \to H_2O$
n O(oxit) = n H2 = 0,672/22,4 = 0,03(mol)
Ta có :
n Fe : n O =0,02 : 0,03 = 2 : 3
Vậy oxit là $Fe_2O_3$
b)
m dd = 0,02.56 + 300 -0,02.2 = 301,08(gam)
n HCl dư = 0,6 - 0,02.2 = 0,56(mol)
n FeCl2 = n Fe = 0,02(mol)
Vậy :
C% HCl = 0,56.36,5/301,08 .100% = 6,8%
C% FeCl2 = 0,02.127/301,08 .100% = 0,84%
Đúng 3
Bình luận (0)
Khử hoàn toàn 16 gam một oxit sắt bằng khí H2 chất rắn thu được hoà tan vào dd HCL dư thấy thoát ra 4,48 lít khí ở đktc. Xác định CTHH của oxit sắt đó
CTHH: FexOy
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: FexOy + yH2 --to--> xFe + yH2O
\(\dfrac{0,2}{x}\)<---------------0,2
Fe + 2HCl --> FeCl2 + H2
0,2<-------------------0,2
=> \(M_{Fe_xO_y}=56x+16y=\dfrac{16}{\dfrac{0,2}{x}}=80x\)
=> \(\dfrac{x}{y}=\dfrac{2}{3}\) => CTHH: Fe2O3
Đúng 1
Bình luận (1)
Đốt cháy hoàn toàn muối sunfua của 1 kim loiaj hóa trị II thu được khí A và rắn B cho A hấp thụ hoàn toàn vào 200ml dd NaOH 1,5M rồi đem cô cạn dd thu được 23g muối.
-Nếu đem B hòa tan bằng H2SO4 loãng rồi cô cạn dd thì được 50g MSO4.5H2O. Xác định kim loại hóa trị II
1. Hoà tan hoàn toàn hh kim loại gồm Mg, Cu, Fe trong dd HCl thu được dd X, chất rắn Y và khí X td hoàn toàn với dd NaOH, thu được kết tủa T. Nung hoàn toàn kết tủa T trong không khí thu được kết tủa rắn gồm?
2. Cho 13,44l hh khí A gồm Clo và Xoi td hết với 19,2g hh B gồm Mg và Al tạo ra 48,15g hh muối clorua và oxit của 2 kim loại. Khối lượng của Mg trong hh B là?
3. Cho 22g hh 2 muối NaX với X, Y là hai halogen ở hai chu kỳ liên tiếp vào dd AgNO3 dư thu được 47,5g kết tủa. X và Y là?
4. Cho...
Đọc tiếp
1. Hoà tan hoàn toàn hh kim loại gồm Mg, Cu, Fe trong dd HCl thu được dd X, chất rắn Y và khí X td hoàn toàn với dd NaOH, thu được kết tủa T. Nung hoàn toàn kết tủa T trong không khí thu được kết tủa rắn gồm?
2. Cho 13,44l hh khí A gồm Clo và Xoi td hết với 19,2g hh B gồm Mg và Al tạo ra 48,15g hh muối clorua và oxit của 2 kim loại. Khối lượng của Mg trong hh B là?
3. Cho 22g hh 2 muối NaX với X, Y là hai halogen ở hai chu kỳ liên tiếp vào dd AgNO3 dư thu được 47,5g kết tủa. X và Y là?
4. Cho 11,2l hh khí A gồm Clo và Oxi td hết với 16,98g hh B gồm Mg và Al tạo ra 42,34g hh muối clorua và oxit của 2 kim loại. Khối lượng của Mg, Al trong hh B lần lượt là?
5. Hòa tan 10g hh muối acbonat kim loại hóa trị 2 bằng dd Hcl dư ta thu được dd A và 2,24l khí bay ra. Cô cạn dd A thì thu được khối lượng muối khan là?
C1 :
- Hòa tan hh vào dd HCl :
Mg + 2HCl => MgCl2 + H2
Fe + 2HCl => FeCl2 + H2
X : MgCl2 , FeCl2 , HCl dư
Y : Cu
Z : H2
- Dung dịch X + NaOH :
MgCl2 + 2NaOH => Mg(OH)2 + 2NaCl
FeCl2 + 2NaOH => Fe(OH)2 + 2NaCl
Kết tủa T : Mg(OH)2 , Fe(OH)2
- Nung T :
Mg(OH)2 -to-> MgO + H2O
4Fe(OH)2 + O2 -to-> 2Fe2O3 + 4H2O
Chất rắn : MgO , Fe2O3
C2:
Đặt : nCl2 = x (mol) , nO2 = y (mol)
nA = x + y = 0.6 (mol) (1)
mCl2 + mO2 = 48.15 - 19.2 = 28.95 (g)
=> 71x + 32y = 28.95 (2)
(1),(2) :
x = 0.25 , y = 0.35
Đặt : nMg = a (mol) , nAl = b (mol)
Mg => Mg+2 + 2e
Al => Al+3 + 3e
Cl2 + 2e => 2Cl-1
O2 + 4e => 2O2-
BT e :
2a + 3b = 0.25*2 + 0.35*4 = 1.9
mB = 24a + 27b = 19.2
=> a = 0.35
b = 0.4
%Mg = 0.35*24/19.2 * 100% = 43.75%
Đúng 3
Bình luận (0)
Hòa tan hoàn toàn a gam sắt vào axit HCl thu được 3,36 lít khí. Hòa tan hết cũng a gam sắt vào axit H2SO4 đặc, nóng, dư thu được x lít khí. Còn khi hòa tan hết a gam sắt vào HNO3 loãng, dư thu được y lít khí NO. Tính x, y đo ở cùng điều kiện
Giả sử có u (mol) Fe
TN1:
PTHH: Fe + 2HCl --> FeCl2 + H2
u--------------------->u
=> \(n_{H_2}=u\left(mol\right)\)
TN2:
PTHH: 2Fe + 6H2SO4 --> Fe2(SO4)3 + 3SO2 + 6H2O
u------------------------------>1,5u
=> \(n_{SO_2}=1,5u\left(mol\right)\)
Có: \(\dfrac{V_{SO_2}}{V_{H_2}}=\dfrac{n_{SO_2}}{n_{H_2}}=\dfrac{1,5u}{u}=1,5\Rightarrow V_{SO_2}=1,5.3,36=5,04\left(l\right)\)
TN3:
PTHH: Fe + 4HNO3 --> Fe(NO3)3 + NO + 2H2O
u-------------------------->u
=> \(n_{NO}=u\left(mol\right)\)
Có: \(\dfrac{V_{NO}}{V_{H_2}}=\dfrac{n_{NO}}{n_{H_2}}=\dfrac{u}{u}=1\Rightarrow V_{NO}=3,36\left(l\right)\)
Đúng 4
Bình luận (0)
Hoà tan hoàn toàn 4,8 g Mg vào 200ml dd HCl thu đc dd A và khí B a, tính V khí B(đktc) b, tính Cm nồng độ chất có trong A c, cho dd NaOH 2M vừa đủ vào A. Tính V dd NaOH cần dùng
\(n_{Mg}=\dfrac{4,8}{24}=0,2\left(mol\right)\)
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,2-->0,4----->0,2------->0,2
a
\(V_{H_2}=0,2.22,4=4,48\left(l\right)\)
b
\(CM_{MgCl_2}=\dfrac{0,2}{0,2}=1M\)
c
\(MgCl_2+2NaOH\rightarrow Mg\left(OH\right)_2+2NaCl\)
0,2------>0,4
\(V_{dd.NaOH}=\dfrac{0,4}{2}=0,2\left(l\right)\)
Đúng 3
Bình luận (0)
Hoà tan 8.4 gam sắt vào dd H2SO4 loãng dư đến khi pứ xảy ra hoàn toàn thì thu được V1 lít khí A (đktc) và dd B
Tính v1
Xem chi tiết
PTHH: \(Fe+H_2SO_4\rightarrow FeSO_4+H_2\uparrow\)
Ta có: \(n_{Fe}=\dfrac{8,4}{56}=0,15\left(mol\:\right)=n_{H_2}\)
\(\Rightarrow V_{H_2}=0,15\cdot22,4=3,36\left(l\right)\)
Đúng 3
Bình luận (2)