Hòa tan 6 gam kim loại M vào dd hcm dư , sau khi phản ứng kết thúc thấy dd tăng 5,5 gam . Vậy M là kim loại nào

Những câu hỏi liên quan
Câu 1: Nhúng thanh kim loại M vào 1lít dung dịch CuSO4 x mol/lít, kết thúc phản ứng thấy thanh kim loại M tăng 20g. Nếu cũng nhúng thanh kim loại trên vào 1 lít dung dịch FeSO4 x mol/lít, kết thúc phản ứng thì thấy thanh M tăng 16g. Vậy M là kim loại nào?Câu2: Cho 2 thanh kim loại R( hóa trị II) có cùng khối lượng. Nhúng thanh thứ nhất vào dung dịch Cu(NO3)2 và thanh thứ 2 vào dd Pb(NO3)2. Sau một thời gian khi số mol 2 muối bằng nhau, lấy 2 thanh kim loại đó ra khỏi dd thấy khối lượng thanh thứ...
Đọc tiếp
Câu 1: Nhúng thanh kim loại M vào 1lít dung dịch CuSO4 x mol/lít, kết thúc phản ứng thấy thanh kim loại M tăng 20g. Nếu cũng nhúng thanh kim loại trên vào 1 lít dung dịch FeSO4 x mol/lít, kết thúc phản ứng thì thấy thanh M tăng 16g. Vậy M là kim loại nào?
Câu2: Cho 2 thanh kim loại R( hóa trị II) có cùng khối lượng. Nhúng thanh thứ nhất vào dung dịch Cu(NO3)2 và thanh thứ 2 vào dd Pb(NO3)2. Sau một thời gian khi số mol 2 muối bằng nhau, lấy 2 thanh kim loại đó ra khỏi dd thấy khối lượng thanh thứ nhất giảm 0,2% còn khối lượng thanh thứ 2 tăng 28,4%. Nguyên tố R là ngtố nào?
Câu 3: Ngâm một vật bằng Cu có khối lượng 5g tring 250g dd AgNO3 4%. Khi lấy vật ra thì lượng AgNO3 trong dd đã giảm 17%. Khối lượng của vật sau phản ứng là bao nhiêu?
Câu4: Nhúng một thanh Zn vào 2lít dd chứa AgNO3 và Cu(NO3)2 có số mol bằng nhau, cho đến khi 2 muối trong dd phản ứng hết thì thu được dd A. Lấy thanh Zn đem cân lại, thấy khối lượng tăng 14,9 gam so với ban đầu. Nồng độ mol của dung dịch A?
Câu5: Nhúng 1 thang graphit được phủ một lớp kim loại hóa trị 2 vaò dd CuSO4 dư. Sau phản ứng khối lượng của thanh graphit giảm đi 0,24g. Cũng thanh graphit này nếu được nhúng vào dd AgNO3 thì khi phản ứng xong thấy khối lượng thanh graphit tăng lên 0,52 gam. Kim loại hóa trị 2 là?
Câu6: Nhúng một thanh kim loại X hóa trị 2 vào dd CuSO4 dư. Sau phản ứng khối lượng thanh kim loại giảm 0,12g. Mặt khác cũng thanh kim loại X đó được nhúng vào dd AgNO3 dư thì kết thúc phản ứng khối lượng thanh tăng 0,26g. Ngtố X là?
Câu 7: Cho 2 dd FeCl2 và CuSO4 có cùng nồng độ mol. - Nhúng thanh kim loại M hóa trị 2 vào 1lít dd FeCl2 sau phản ứng khối lượng thanh kim loạităng16g. - Nhúng cùng thanh kim loại ấy vào 1 lít dd CuSO4 sau phản ứng khối lượng thanh kim loại tăng 20g. Giả thiết các phản ứng xảy ra hoàn toàn và thanh kim loại M chưa bị tan hết. Kim loại M là?
Nhờ các bạn giúp với ạ. Mình đang cần gấp
Câu 1:
2M+nCuSO4\(\rightarrow\)M2(SO4)n+nCu
2M+nFeSO4\(\rightarrow\)M2(SO4)n+nFe
- Gọi a là số mol của M
- Độ tăng khối lượng PTHH1:
64na/2-Ma=20 hay(32n-M).a=20
- Độ tăng khối lượng PTHH2:
56.na/2-Ma=16 hay (28n-M)a=16
Lập tỉ số ta được:\(\dfrac{32n-M}{28n-M}=\dfrac{20}{16}=1,25\)
32n-M=35n-1,25M hay 0,25M=3n hay M=12n
n=1\(\rightarrow\)M=12(loại)
n=2\(\rightarrow\)M=24(Mg)
n=3\(\rightarrow\)M=36(loại)
Đúng 1
Bình luận (0)
Câu 2:Gọi A là khối lượng thanh R ban đầu.
R+Cu(NO3)2\(\rightarrow\)R(NO3)2+Cu
R+Pb(NO3)2\(\rightarrow\)R(NO3)2+Pb
- Gọi số mol Cu(NO3)2 và Pb(NO3)2 là x mol
- Độ giảm thanh 1: \(\dfrac{\left(R-64\right)x}{A}.100=0,2\)
- Độ tăng thanh 2: \(\dfrac{\left(207-R\right)x}{A}.100=28,4\)
Lập tỉ số: \(\dfrac{207-R}{R-64}=\dfrac{28,4}{0,2}=142\)
207-R=142R-9088 hay 143R=9295 suy ra R=65(Zn)
Đúng 1
Bình luận (0)
Câu 3:
Cu+2AgNO3\(\rightarrow\)Cu(NO3)2+2Ag
\(m_{AgNO_3}=\dfrac{250.4}{100}=10g\)
\(m_{AgNO_3}\left(pu\right)=\dfrac{17.10}{100}=1.7g\)
\(n_{AgNO_3}\left(pu\right)=\dfrac{17.}{170}=0,1mol\)
Độ tăng khối lượng=108.0,1-64.0,1:2=7,6g
Khối lượng thanh Cu=5+7,6=12,6g
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
hòa tan 6g kim loại m vào hcl dư sau phản ứng kết thúc thấy dung dịch tăng 5,5g. m là kim loại nào
Tham khảo:
Vì sau p/ư khối lượng dung dịch tăng 0,55g và trong quá trình phản ứng có giải phóng khí H2 nên
m\(_{H_2}\)= 6-5,5= 0,5g
=> n\(_{H_2}\)= 0,5:2= 0.25 mol
PTHH: R + 2HCl --> RCl(2) + H(2)
0,25 mol <-- 0,25 mol
=>MR= 6:0,25=24(g/mol)
vậy kl cần tìm là magie (Mg)
Đúng 3
Bình luận (6)
Vì sau phản ứng khối lượng dung dịch tăng 5,5 g có giải phóng khi H2
\(m_{H_2}=6-5,5=0,5\left(g\right)\)
\(n_{H_2}=\dfrac{0,5}{2}=0,25\left(mol\right)\)
PTHH : \(m+2HCl->mCl\left(2\right)+H\left(2\right)\)
0,25 --------------------- 0,25
\(=>M_m=\dfrac{6}{0,25}=24\left(\dfrac{g}{mol}\right)\)
=> m là magie (mg)
Đúng 0
Bình luận (2)
Hòa tan 12,9 gam hỗn hợp 2 kim loại đều có hóa trị II vào dung dịch H2SO4 loãng dư , sau khi phản ứng kết thúc hoàn toàn , còn lại 6,4 gam kim loại không tan , lọc hết kim loại không tan ra thấy khối lượng tăng 6,3 g . Đem đốt cháy phần kim loại không tan trong không khí đến khối lượng không đổi thu được 8 gam một oxit duy nhất . Xác định 2 kim loại trên
Cho kim loại M có hóa trị (II). Hòa tan hết 8 gam oxit của M vào dung dịch axit clohiđric. Sau khi kết thúc phản ứng thấy có 0,4 mol HCl đã phản ứng. Kim loại M là ?
Em cần gấp ạ.
`MO + 2HCl -> MCl_2 + H_2O`
Theo PT: `n_(MO) = (n_(HCl))/2`
`<=> 8/(M_M +16) = (0,4)/2`
`<=> M_M = 24`
`=>M` là `Mg`.
Đúng 2
Bình luận (0)
\(MO+2HCl\rightarrow MCl_2+H_2O\)
Ta có : \(n_{MO}=\dfrac{1}{2}n_{HCl}=0,2\left(mol\right)\)
=> \(M_{MO}=\dfrac{8}{0,2}=40\)
=> M=24 (Mg)
Đúng 3
Bình luận (0)
hòa tan hết một gam hồn hợp gồm 2 kim loại A và B (chưa rõ hóa trị) vào dd HCI. Sau khi phản ứng kết thúc thu được m gam muối clorua và 8,96 lít H2 ( dktc )
a) Viết pthh
b) Tính a (biết a = 57,61 %m)
Bài 3. Cho 7,8 gam hỗn hợp hai kim loại Mg, Al tác dụng với dd H2SO4 loãng dư khi phản ứng kết thúc thấy khối lượng dd tăng thêm 7g.
a/ Tính khối lượng mỗi kim loại có trong hỗn hợp ban đầu.
b/ Tính % về khối lượng mỗi kim loại có trong hỗn hợp ban đầu.
c/ Tính khối lượng muối tạo thành.
\(a,Mg+H_2SO_4\rightarrow MgSO_4+H_2\\ 2Al+3H_2SO_4\rightarrow Al_2\left(SO_4\right)_3+3H_2\\ m_{tăng}=m_{hhMg,Al}-m_{H_2}\\ \Leftrightarrow7=7,8-m_{H_2}\\ \Leftrightarrow m_{H_2}=0,8\left(g\right)\\ \Rightarrow n_{H_2}=\dfrac{0,8}{2}=0,4\left(mol\right)\\ Đặt:a=n_{Al}\left(mol\right);n_{Mg}=b\left(mol\right)\left(a,b>0\right)\\ \Rightarrow\left\{{}\begin{matrix}24b+27a=7,8\\b+1,5a=0,4\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}a=0,2\\b=0,1\end{matrix}\right.\\m_{Mg}=24.0,1=2,4\left(g\right);m_{Al}=0,2.27=5,4\left(g\right)\\ \Rightarrow\%m_{Al}=\dfrac{0,2.27}{7,8}.100\approx69,231\%\\ \Rightarrow\%m_{Mg}\approx30,769\%\\ c,m_{muối}=m_{MgSO_4}+m_{Al_2\left(SO_4\right)_3}=120b+342.0,5a=120.0,1+342.0,5.0,2=46,2\left(g\right)\)
Đúng 2
Bình luận (2)
Cho 22,4 gam bột kim loại M vào dung dịch HCl dư, sau khi phản ứng kết thúc thu được 0,8 gam H2. Kim loại M là
A. Mg.
B. Ca
C. Fe
D. Zn
Đáp án C
Số mol H2 thu được là: n H 2 = 0 , 8 2 = 0 , 4 m o l
Gọi n là hóa trị của M
Phương trình hóa học:
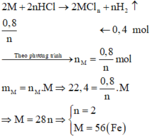
=> M là Fe
Đúng 0
Bình luận (0)
Hòa tan hoàn toàn m gam một kim loại kiềm R vào nước , sau phản ứng thu được 3,36 lít H2 và 200gam dd chứa một chất tan X có nồng độ là 6% . Xác định kim loại R
Xem chi tiết
R + H2O -> ROH + 1/2 H2
nH2= 0,15(mol)
=> nROH=0,3(mol)
mROH= 6%.200=12(g)
=> M(ROH)= 12/0,3=40(g/mol)
Mà: M(ROH)=M(R)+17
=>M(R)+17=40
=>M(R)=23(g/mol) => R là Natri (Na=23)
Đúng 2
Bình luận (0)
hòa tan hoàn toàn 9,6 gam kim loại a chưa rõ trị bằng dd hcl vừa đủ. khi phản ứng kết thúc thu được 8,96 lít khí hidro đktc. xác định tên kim loại a






















