Dùng hiđro (H2) để khử 7,2 gam sắt (II) oxit (CuO)
a) Viết phương trình hóa học của phản ứng xảy ra ?
b) Tính khối lượng đồng (Cu) thu được?
c) Tính thể tích khí hiđro đã dùng (ở đktc)?
Dùng hiđro (H2) để khử 7,2 gam sắt (II) oxit (FeO)
a) Viết phương trình hóa học của phản ứng xảy ra ?
b) Tính khối lượng đồng (Cu) thu được?
c) Tính thể tích khí hiđro đã dùng (ở đktc)?
hình như bn ghi sai r đó phải là:đồng oxit mới phải chứ![]()
a) PTHH: H2 + CuO --t0--> Cu + H2O
b) nCuO = \(\dfrac{m}{M}\) = \(\dfrac{7,2}{80}\) = 0,09 (mol)
nCu = nCuO = 0,09 (mol)
⇒ mCu = n x M = 0,09 x 64 = 5,76 (g)
c) nH2 = nCuO = 0,09 (mol)
⇒ VH2 = n x 22,4 = 0,09 x 22,4 = 2,016 (l)
Trong phòng thí nghiệm , người ta dùng hidro (H2) để khử 8 gam đồng (II) oxit (cuo) A. Viết phương trình hóa học của phản ứng xảy ra B. Tính khối lượng đồng (cu) thu được C. Tính thể tích hiđro đã dùng (ở đktc)
A. \(H_2+CuO\rightarrow Cu+H_2O\)
B. \(n_{CuO}=\dfrac{8}{80}=0,1\left(mol\right)\)
Theo PTHH: \(n_{Cu}=n_{CuO}=0,1\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,1.64=6,4\left(g\right)\)
C. Theo PTHH: \(n_{H_2}=n_{CuO}=0,1\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,1.22,4=2,24\left(l\right)\)
Trong phòng thí nghiệm người ta dùng khí hiđro để khử sắt(II) oxit và thu được 11,2 g Fe.
a) Viết phương trình hóa học của phản ứng đã xảy ra.
b) Tính khối lượng sắt (III) oxit đã phản ứng.
c) Tính thể tích khí hiđro đã tiêu thụ (đktc).
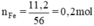
Phương trình hóa học của phản ứng:
Fe2O3 + 3H2 → 2Fe + 3H2O.
Khử 1 mol Fe2O3 cho 2 mol Fe.
x mol Fe2O3 → 0,2 mol.
x = 0,2 : 2 =0,1 mol.
m = 0,1 .160 =16g.
Khử 1 mol Fe2O3 cần 3 mol H2.
Vậy khử 0,1 mol Fe2O3 cần 0,3 mol H2.
V= 0,3 .22.4 = 6,72l.
Trong phòng thí nghiệm ,người ta dùng hiđro để khử sắt(III)oxit(Fe2O3) thu được 24 gam sắt. a. Viết phương trình hóa học của phản ứng xảy ra b.tính số gam sắt(III)oxit đã phản ứng c. tính thể tích khí hiđro dùng để khử(ở đktc)
a, \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
b, \(n_{Fe}=\dfrac{24}{56}=\dfrac{3}{7}\left(mol\right)\)
Theo PT: \(n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe}=\dfrac{3}{14}\left(mol\right)\Rightarrow m_{Fe_2O_3}=\dfrac{3}{14}.160=\dfrac{240}{7}\left(g\right)\)
c, Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Fe}=\dfrac{9}{14}\left(mol\right)\Rightarrow V_{H_2}=\dfrac{9}{14}.22,4=14,4\left(l\right)\)
\(n_{Fe}=\dfrac{m}{M}=\dfrac{24}{56}\approx0,43\left(mol\right)\\ a.PTHH:Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
2 3 2 3
0,43 0,645 0,45 0,645
\(b.m_{Fe_2O_3}=n.M=0,43.\left(56.2+16.3\right)=68,8\left(g\right)\\ c.V_{H_2}=n.24,79=0,645.24,79=15,98955\left(l\right).\)
a)\(PTHH:Fe_3O_4+4H_2\xrightarrow[]{}3Fe+4H_2O\)
b)\(m_{Fe}=\dfrac{24}{56}=0,4\left(m\right)\)
\(PTHH:Fe_3O_4+4H_2\xrightarrow[]{}3Fe+4H_2O\)
tỉ lệ :1 4 3 4
số mol :0,13 0,53 0,4 0,53
\(m_{Fe_3O_4}=0,13.232=30,16\left(g\right)\)
c)\(V_{H_2}=0,53.22,4=11,872\left(l\right)\)
:Trong phòng thí nghiệm người ta dùng khí hiđro để khử sắt(III) oxit và thu được 11,2 gam Fe. a) Viết phương trình hóa học của phản ứng đã xảy ra.
b) Tính khối lượng sắt(III) oxit đã phản ứng.
c) Tính thể tích khí hiđro đã tiêu thụ (ở đktc).
a, \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
b, \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Theo PT: \(n_{Fe_2O_3}=\dfrac{1}{2}n_{Fe}=0,1\left(mol\right)\Rightarrow m_{Fe_2O_3}=0,1.160=16\left(g\right)\)
c, Theo PT: \(n_{H_2}=\dfrac{3}{2}n_{Fe}=0,3\left(mol\right)\)
\(\Rightarrow V_{H_2}=0,3.22,4=6,72\left(l\right)\)
Trong phòng thí nghiệm, người ta dùng hiđro để khử sắt(III) oxit và thu được 11,2 gam sắt.
Viết phản ứng hóa học xảy ra.
Tính khối lượng sắt(III) oxit đã phản ứng.
Tính thể tích khí hiđro đã tiêu thụ (đktc).
Dùng V (lít) khí hiđro (ở đktc)khử 8 gam sắt (|||) oxit a) viết phương trình hóa học b) tính thể tích khí hiđro thu được (ở đktc) c) tính khối lượng axit Clohiđric (HCl) đã dùng
a, \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
b, \(n_{Fe_2O_3}=\dfrac{8}{160}=0,05\left(mol\right)\)
\(n_{H_2}=3n_{Fe_2O_3}=0,15\left(mol\right)\Rightarrow V_{H_2}=0,15.22,4=3,36\left(l\right)\)
c, Đề hỏi mHCl đã dùng khi nào bạn nhỉ?
Trong phòng thí nghiệm người ta đã dùng cacbon oxit CO để khử 0,2 mol Fe3O4 và dùng khí hiđro để khử 0,2 mol Fe2O3 ở nhiệt đô cao.
a) Viết phương trình hóa học của các phản ứng đã xảy ra.
b) Tính số lít khí ở đktc CO và H2 cần dùng cho mỗi phản ứng.
c) Tính số gam sắt thu được ở mỗi phản ứng hóa học.
a) Phương trình hóa học của các phản ứng:
4CO + Fe3O4 → 3Fe + 4 CO2 (1).
3H2 + Fe2O3 → 2Fe + 3H2O (2).
b)Theo phương trình phản ứng trên ta có:
Muốn khử 1 mol Fe3O4 cần 4 mol CO.
Muốn khử 0,2 mol Fe3O4 cần x mol CO.
x= 0,2.4 = 0,8 mol CO.
VCO = 0,8 .22,4 = 17,92 lít.
Muốn khử 1 mol Fe2O3 cần 3 mol H2.
Muốn khử 0,2 mol Fe2O3 cần y mol H2.
y = 0,2 .3 = 0,6 mol.
VH2= 0,6 .22,4 = 13,44l.
c) Ở phản ứng (1) khử 1 mol Fe3O4 được 3 mol Fe.
Vậy khử 0,2 mol Fe3O4 được 0,6 mol Fe.
mFe = 0,6 .56 = 33,6g Fe.
Ở phản ứng (2) khử 1 mol Fe2O3 được 2 mol Fe.
Vậy khử 0,2 mol Fe2O3 được 0,4 mol Fe.
mFe = 0,4 .56 = 22,4g Fe.
Người ta dùng hiđro để khử sắt từ oxit Fe3O4 ở nhiệt độ cao thu được 11,2 gam kim loại sắt.
a. Viết phương trình phản ứng xảy ra.
b. Tính khối lượng sắt từ oxit đã phản ứng.
c. Tính thể tích khí H2 ở đktc cần dùng cho phản ứng.
d. Tính khối lượng Zn, khối lượng axit HCl cần dùng để điều chế lượng khí H2 ở trên.
cíu em mn ơiiiii, ngày 14/3 em thi ruiiiii
a, \(Fe_3O_4+4H_2\underrightarrow{t^o}3Fe+4H_2O\)
b, \(n_{Fe}=\dfrac{11,2}{56}=0,2\left(mol\right)\)
Theo PT: \(n_{Fe_3O_4}=\dfrac{1}{3}n_{Fe}=\dfrac{1}{15}\left(mol\right)\Rightarrow m_{Fe_3O_4}=\dfrac{1}{15}.232=\dfrac{232}{15}\left(g\right)\)
c, \(n_{H_2}=\dfrac{4}{3}n_{Fe}=\dfrac{4}{15}\left(mol\right)\Rightarrow V_{H_2}=\dfrac{4}{15}.22,4=\dfrac{448}{75}\left(l\right)\)
d, \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
\(n_{Zn}=n_{H_2}=\dfrac{4}{15}\left(mol\right)\Rightarrow m_{Zn}=\dfrac{4}{15}.65=\dfrac{52}{3}\left(g\right)\)
\(n_{HCl}=2n_{H_2}=\dfrac{8}{15}\left(mol\right)\Rightarrow m_{HCl}=\dfrac{8}{15}.36,5=\dfrac{292}{15}\left(g\right)\)