khử 9,6 gam đồng (ll) oxit bằng khí hiđro. hãy:
a)tính số gam đồng kim loại thu được;
b)tính thể tích khí hiđro (đktc)cần dùng.
Bài 6: Khử 48 gam đồng (II) oxit bằng khí hidro. Hãy:
a) Tính số gam đồng kim loại thu được
Tính thể tích khí hiđro (đktc) cần dùng
nCuO = 48 : 80 = 0,6 (Mol)
pthh : CuO + H2 -t--> Cu + H2O
0,6---->06------>0,6
=> mCu= 0,6 . 64 = 38,4 (G)
=> VH2 = 0,6 .22,4 = 13,44 (L)
a, \(n_{CuO}=\dfrac{48}{80}=0,6\left(mol\right)\)
PTHH: CuO + H2 --to--> Cu + H2O
0,6 0,6 0,6
\(\rightarrow\left\{{}\begin{matrix}m_{Cu}=0,6.64=38,4\left(g\right)\\V_{H_2}=0,6.22,4=13,44\left(l\right)\end{matrix}\right.\)
PTHH : \(CuO+H_2\left(t^o\right)->Cu+H_2O\) (1)
a) \(n_{CuO}=\dfrac{m}{M}=\dfrac{48}{64+16}=0,6\left(mol\right)\)
Từ (1) -> \(n_{Cu}=n_{CuO}=n_{H_2}=0,6\left(mol\right)\)
-> \(m_{Cu}=n.M=0,6.64=38,4\left(g\right)\)
\(V_{H_2}=n.22,4=0,6.22,4=13,44\left(l\right)\)
Khử 48 gam đồng(II) oxit bằng khí hiđro. Hãy:
a) Tính số gam đồng kim loại thu được.
b) Tính thể tích khí hiđro (đktc) cần dùng.
nCuO = 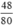 = 0,6 mol.
= 0,6 mol.
Phương trình hóa học của phản ứng khử CuO:
CuO + H2 → Cu + H2O.
nCu = 0,6mol.
mCu = 0,6 .64 = 38,4g.
Theo phương trình phản ứng trên:
nH2 = 0,6 mol
VH2 = 0,6 .22,4 = 13,44 lít.
II- BÀI TẬP TỰ LUẬN :
Bài 1: Viết phương trình hóa học cho các phản ứng giữa hidro và các oxit sau:a. Sắt (III) oxitb. Thủy ngân (II) oxitc. Chì (II) oxit
Bài 2: Khử 48 gam đồng(II) oxit bằng khí hiđro. Hãy:
a) Tính số gam đồng kim loại thu được.
b) Tính thể tích khí hiđro (đktc) cần dùng
Bài 3: Khử 21,7 gam thủy ngân(II) oxit bằng hiđro. Hãy:
a) Tính số gam thủy ngân thu được.
b) Tính số mol và thể tích khí hiđro (đktc) cần dùng
Bài 4: Tính thể tích oxi (đktc) thu được khi phân hủy 4,9 gam KClO3 trong phòng thí
nghiệm?
Bài 5: Tính số gam nước thu được khi cho 8,4 lít khí hiđro tác dụng với 2,8 lít oxi (các thể tích đo ở đktc).
Bài 6: Cho các kim loại kẽm, nhôm, sắt, lần lượt tác dụng với dung dịch H2SO4 loãng.
a, Viết phản ứng hóa học?
b, Cho cùng một khối lượng kim loại trên tác dụng hết với axit thì kim loại nào cho nhiều khí hiđro nhất?
c, Nêú thu được cùng một thể tích khí H2 thì khối lượng của kim loại nào đã phản ứng là nhỏ nhất?
Bài 7: Dẫn 2,24 lít khí H2 ở đktc vào một ống có chứa 12g CuO đã nung nóng tới nhiệt độ thích hợp. Kết thúc phản ứng trong ống còn a(g) chất rắn.
a. Viết phương trình phản ứng.
b. Tính khối lượng nước tạo thành sau phản ứng trên.
c. Tính a.
3.
nHgO = 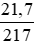
Phương trình hóa học của phản ứng khử HgO:
HgO + H2 → Hg + H2O
nHg = 0,1 mol.
mHg = 0,1 .201 = 20,1g.
nH2 = 0,1 mol.
VH2 = 0,1 .22,4 =2,24l.
1.
Phương trình phản ứng:
Fe3O4 + 4H2 → 4H2O + 3Fe
HgO + H2 → H2O + Hg
PbO + H2 → H2O + Pb
2.
a. Số mol đồng (II) oxit: n = m/M = 48/80 = 0,6 (mol)
Phương trình phản ứng:
CuO + H2 to→ H2O + Cu
1 mol 1 mol 1 mol
0,6 0,6 0,6
Khối lượng đồng kim loại thu được: m = n.M = 0,6.64 = 38,4 (g)
b. Thể tích khí hiđro cần dùng ở đktc là:
V = 22,4.n = 22,4.0,6 = 13,44 (lít).
Khử 48 gam đồng 2 oxit khí H2,hãy:
a) tính số gam đồng kim loại thu được
b)tính thể tích khí H2 (ở đktc) cần dùng
\(n_{CuO}=\dfrac{48}{80}=0,6\left(mol\right)\\
pthh:CuO+H_2\underrightarrow{t^o}Cu+H_2O\)
0,6 0,6 0,6 0,6
\(m_{Cu}=0,6.64=38,4g\\
V_{H_2}=0,6.22,4=13,44L\)
1/ khử 48 gam đồng (II) Oxit bằng khí hiđro.hãy
tính số gam đồng kim loại thu được
tính thể tích khí hiđro (đktc) cần dùng
2/ tính số gam nước thu được khi cho 8,4 lít khí hiđro tác dụng với 2,8 lít khí oxi (các thể tích khí đo ở đktc)
1/ \(CuO+H_2-^{t^o}\rightarrow Cu+H_2O\)
\(n_{Cu}=n_{CuO}=\dfrac{48}{80}=0,6\left(mol\right)\)
=> \(m_{Cu}=0,6.64=38,4\left(g\right)\)
\(n_{H_2}=n_{CuO}=0,6\left(mol\right)\)
=> \(V_{H_2}=0,6.22,4=13,44\left(l\right)\)
2. \(2H_2+O_2-^{t^o}\rightarrow2H_2O\)
\(n_{H_2}=0,375;n_{O_2}=0,125\)
Lập tỉ lệ \(\dfrac{0,375}{2}>\dfrac{0,125}{1}\)
=> Sau phản ứng H2 dư, tính theo số mol O2
\(n_{H_2O}=2n_{O_2}=0,25\left(mol\right)\)
=> \(m_{H_2O}=0,25.18=4,5\left(g\right)\)
Khử 48 gam đồng (II) oxit bằng khí hidro. Hãy: Tính số gam đồng kim loại thu được.
cao thủ làm tiếp đi ạ :D
Bài tập 4: Khử 16 gam đồng (II) oxit bằng khí hidro. Hãy:
a) Tính số gam đồng kim loại thu được
b) Tính thể tích khí hidro( đktc) cần dùng
Bài 5 : Cho các hợp chất sau : HCl, Na2O, NaOH, SO2, CaCO3, KCl ,Ca(HCO3)2. Hãy phân loại, gọi tên các hợp chất trên.
nCuO = 16 : 80 = 0,2 (MOL)
pthh : CuO + H2 -t--> H2O + Cu
0,2---> 0,2---------------> 0,2 (mol)
=> mCu = 0,2 . 64 = 12,8 (g)
=> VH2 = 0,2. 22,4 = 4,48 ( l)
bai 5
Axit : HCl : Axit Clohidric
Oxit Axit : SO2 : luu huynh dioxt
Oxit bazo : Na2O : natri oxit
Muoi : Ca(HCO3)2 : canxi bisulfit
KCl : Kali Clorua
bazo : NaOH : Natri hidroxit
9,6 gam đồng (2) = khí hiđro hãy
a)tính số gam đồng kim loại thu đc
b) tích thể tích khí hiđro (đktc)cần dùng
a, nCuO = 9,6/80 = 0,12 (mol)
PTHH: CuO + H2 -> (t°) Cu + H2O
Mol: 0,12 ---> 0,12 ---> 0,12
mCu = 0,12 . 64 = 7,68 (g)
b, VH2 = 0,12 . 22,4 = 2,688 (l)
Khử 0,8g đồng (II) oxit bằng khí hiđro. (Cho Cu = 64; H = 1; O = 16; Cl = 35,5).Hãy: a/Tính số gam đồng kim loại thu được? b/Tính thể tích khí hiđro (đktc) cần dùng? c/Để có lượng H2 đó phải lấy bao nhiêu gam Fe cho tác dụng vừa đủ với bao nhiêu gam dd axit HCl 20
`n_[CuO]=[0,8]/80=0,01(mol)`
`H_2 + CuO` $\xrightarrow{t^o}$ `Cu + H_2 O`
`0,01` `0,01` `0,01` `(mol)`
`a)m_[Cu]=0,01.64=0,64(g)`
`b)V_[H_2]=0,01.22,4=0,224(l)`
`c)`
`Fe + 2HCl -> FeCl_2 + H_2`
`0,01` `0,02` `0,01` `(mol)`
`@m_[Fe]=0,01.56=0,56(g)`
`@m_[dd HCl]=[0,02.36,5]/20 . 100=3,65(g)`