tính số gam nước thu được khi cho 8,4 lít khí hidro tác dụng với 2,8 lít khí oxi (các thể tích khí đo ở đktc)

Những câu hỏi liên quan
Tính số gam nước thu được khi cho 8,4 lít khí hiđro tác dụng với 2,8 lít oxi (các thể tích đo ở đktc).
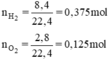
Phương trình hóa học của phản ứng tạo nước:
2H2 + O2 → 2H2O.
So sánh tỉ lệ 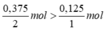 . Như vậy lượng H2 dư nên tính khối lượng nước sinh ra theo oxi.
. Như vậy lượng H2 dư nên tính khối lượng nước sinh ra theo oxi.
Theo phương trình trên ta có:
nH2O = 2. 0,125 = 0,25 mol.
mH2O = 0,25 .18 = 4,5g.
Đúng 0
Bình luận (0)
1/ khử 48 gam đồng (II) Oxit bằng khí hiđro.hãy
tính số gam đồng kim loại thu được
tính thể tích khí hiđro (đktc) cần dùng
2/ tính số gam nước thu được khi cho 8,4 lít khí hiđro tác dụng với 2,8 lít khí oxi (các thể tích khí đo ở đktc)
1/ \(CuO+H_2-^{t^o}\rightarrow Cu+H_2O\)
\(n_{Cu}=n_{CuO}=\dfrac{48}{80}=0,6\left(mol\right)\)
=> \(m_{Cu}=0,6.64=38,4\left(g\right)\)
\(n_{H_2}=n_{CuO}=0,6\left(mol\right)\)
=> \(V_{H_2}=0,6.22,4=13,44\left(l\right)\)
Đúng 3
Bình luận (0)
2. \(2H_2+O_2-^{t^o}\rightarrow2H_2O\)
\(n_{H_2}=0,375;n_{O_2}=0,125\)
Lập tỉ lệ \(\dfrac{0,375}{2}>\dfrac{0,125}{1}\)
=> Sau phản ứng H2 dư, tính theo số mol O2
\(n_{H_2O}=2n_{O_2}=0,25\left(mol\right)\)
=> \(m_{H_2O}=0,25.18=4,5\left(g\right)\)
Đúng 3
Bình luận (0)
Bài 6 :tính số gam nước thu được khi cho 8,4 lít hidro tác dụng với 2,8 lít khí õi (các thể tích khí đo ở đktc )
GIúp mk với ạ :)))
\(n_{H_2}=\dfrac{8,4}{22,4}=0,375\left(mol\right)\)
\(n_{O_2}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\)
PT: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Xét tỉ lệ: \(\dfrac{0,375}{2}>\dfrac{0,125}{2}\), ta được H2 dư.
Theo PT: \(n_{H_2O}=2n_{O_2}=0,25\left(mol\right)\Rightarrow m_{H_2O}=0,25.18=4,5\left(g\right)\)
Đúng 2
Bình luận (0)
Tính số gam nước thu được khi cho 8,96 lít khí hiđro tác dụng với 5,6 lít oxi (các thể tích đo ở đktc).
nH2 = V/22,4 = 8,96/22,4 = 0,4 (mol)
nO2 = V/22,4 = 5,6/22,4 = 0,25 (mol)
PTHH: 2H2 + O2 --to--> 2H2O
Ta có: 0,4/2 < 0,25/1
=> O2 dư
Theo PTHH: nH2O = nH2 = 0,4 (mol)
=> mH2O = n.M = 0,4 . 18 = 7,2(g)
Đúng 2
Bình luận (0)
Cho 4,48 lít khí hiđro tác dụng với khí oxi. Biết các thể tích khí đo ở đktc. Tính a/ số gam nước thu được b/ thể tích khí oxi cần dùng
Số mol của 4,48 lít H2:
\(n_{H_2}=\dfrac{V}{22,4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH:
\(2H_2+O_2\underrightarrow{t^o}2H_2O\)
tỉ lệ: 2 : 1 : 2
0,2-> 0,1 : 0,2( mol)
a/ số gam của 0,2 mol nước:
\(m_{H_2O}=n.M=0,2.=3,6\left(g\right)\)
b/ thể tích của 0,1 mol khí O2:
\(V_{O_2}=n.22,4=0,1.22,4=2,24\left(l\right)\)
Đúng 1
Bình luận (0)
Tính tổng số gam nước thu được khi cho 8,4 lít khí h2 tác dụng với 2,8 lít khí oxygen ( các khí đo ở đkc)
\(2H_2+O_2\rightarrow\left(t^o\right)2H_2O\\ Vì:\dfrac{8,4}{2}>\dfrac{2,8}{1}\Rightarrow O_2hết,H_2dư\\ n_{H_2O}=2n_{O_2}=2.\dfrac{2,8}{24}=\dfrac{7}{30}\left(mol\right)\\ m_{H_2O}=\dfrac{7}{30}.18=4,2\left(g\right)\)
Đúng 1
Bình luận (0)
Bài tập 1: Tính số gam nước thu được khi cho 2,24lít khí Hiđrô tác dụng với 2,8 lít khí ôxi. ( Các thể tích khí đo ở đktc)
PTHH: \(4H_2+O_2\underrightarrow{t^o}2H_2O\)
Ta có: \(\left\{{}\begin{matrix}n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\n_{O_2}=\dfrac{2,8}{22,4}=0,125\left(mol\right)\end{matrix}\right.\)
Xét tỉ lệ: \(\dfrac{0,1}{4}< \dfrac{0,125}{1}\) \(\Rightarrow\) Oxi còn dư, Hidro p/ứ hết
\(\Rightarrow n_{H_2O}=0,05\left(mol\right)\) \(\Rightarrow m_{H_2O}=0,05\cdot18=0,9\left(g\right)\)
Đúng 3
Bình luận (0)
Tính số gam nước thu được khi cho 8,4 lít khí H2 tác dụng với 2,8 lít khí O2 (các thể tích đo ở đktc).
PTHH: 2H2 + O2 -to-> 2H2O
Ta có: \(\dfrac{8,4}{2}>\dfrac{2,8}{1}\)
=> H2 dư, O2 hết nên tính theo \(V_{O_2}\)
Theo PTHH và đề bài, ta có:
\(m_{H_2O}=2.\dfrac{2,8}{22,4}.18=4,5\left(g\right)\)
Đúng 0
Bình luận (1)
PTHH 2H2 + O2 -t0-> 2H2O
2mol 1mol 2mol
2V(lit) V(lit)
Ta thấy thể tích H2 lớn hơn 2 lần thể tích Oxi, do đó H2 dư nên ta tính số gam nước theo số mol oxi
Theo PTHH ta có nH2=nH2O
nH2O= 2,8 . 2 :22,4 = 0,25 (mol)
Vậy mH2O= 0,25 . 18 =4,5 (gam)
Đúng 0
Bình luận (0)
Xem thêm câu trả lời
cho 2,8 gam khí Nitơ tác dụng với 10,08 lít khí Hiđro. tính % thể tích của các khí thu được sau khi phản ứng kết thúc
$n_{N_2} = \dfrac{2,8}{28} = 0,1(mol)$
$n_{H_2} = \dfrac{10,08}{22,4} = 0,45(mol)$
$N_2 + 3H_2 \buildrel{xt,t^o,p}\over\rightleftharpoons 2NH_3$
Theo PTHH :
$n_{N_2} : 1 < n_{H_2} : 3$ nên hidro dư
$n_{H_2\ pư} = 3n_{N_2} = 0,3(mol)$
$n_{NH_3} = 2n_{N_2} = 0,2(mol)$
Suy ra :
$V_{NH_3} = 0,2.22,4 = 4,48(lít)$
$V_{H_2} = 10,08 - 0,3.22,4 = 3,36(lít)$
$\%V_{NH_3} = \dfrac{4,48}{4,48+3,36}.100\% = 57,14\%$
$\%V_{H_2} = 100\% -57,14\% = 42,86\%$
Đúng 2
Bình luận (0)
\(n_{N_2}=\frac{2,8}{14}=0,2(mol)\\ n_{H_2}=\frac{10,08}{22,4}=0,45(mol)\\ N_2+3H_2 \to 2NH_3\\ 0,2 >\frac{0,45}{3}=0,15\\ \Rightarrow N_2 > H_2\\ n_{NH_3}=\frac{2}{3}.n{H_2}=0,3(mol)\\ V_{NH_3}=0,3.22,4=6,72(l)\\ n_{N_2}=0,15(mol)\\ V_{N_2}=(0,2-0,15).22,4=1,12(l)\\ \%V_{NH_3}=\frac{6,72}{6,72+1,12}=85,71\%\\ \%V_{N_2}=14,29\%\)
Đúng 1
Bình luận (0)





























