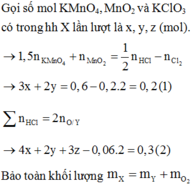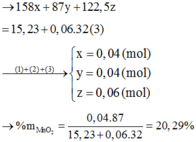Nung nóng 20 gam hỗn hợp KMnO4 và KClo3 sau một thời gian thu được V(lít) khí Oxi ở đktc và 18,88 gam chất rắn. Tính V

Những câu hỏi liên quan
Nung nóng 20 gam hỗn hợp gồm KMnO4 và KClO3, sau một thời gian thu được 18,88 gam chất rắn:
a) Hãy tính khối lượng hỗn hợp chất rắn thu được sau phản ứng.
b) Tính thể tích khí oxi sinh ra trong phản ứng.
a) Sau phản ứng : $m_{chất\ rắn} = 18,88(gam)$
b) Bảo toàn khối lượng :
$m_{O_2} = 20 - 18,8 = 1,12(gam)$
$n_{O_2} = 1,12 : 32 = 0,035(mol)$
$V_{O_2} = 0,035.22,4 = 0,784(lít)$
Đúng 1
Bình luận (0)
Nung nóng 31,205 gam hỗn hợp X gồm KMnO4, KClO3 và KClO2, sau một thời gian thu được khí oxi và 25,365 gam chất rắn Y gồm K2MnO4, MnO2, KMnO4, KCl. Để phản ứng hoàn toàn Y cần vừa đủ 2,0 lít dung dịch chứa HCl 0,4M thu được 4,844 lít khí Cl2 (đktc). Phần trăm KMnO4 bị nhiệt phân là A. 75,72%. B. 52,66%. C. 73,47%. D. 63,19%.
Đọc tiếp
Nung nóng 31,205 gam hỗn hợp X gồm KMnO4, KClO3 và KClO2, sau một thời gian thu được khí oxi và 25,365 gam chất rắn Y gồm K2MnO4, MnO2, KMnO4, KCl. Để phản ứng hoàn toàn Y cần vừa đủ 2,0 lít dung dịch chứa HCl 0,4M thu được 4,844 lít khí Cl2 (đktc). Phần trăm KMnO4 bị nhiệt phân là
A. 75,72%.
B. 52,66%.
C. 73,47%.
D. 63,19%.
một hỗn hợp x gồm KClO3 và KMnO4 được chia thành 2 phần bằng nhau. Phần 1 nung nóng một thời gian thu được 2,24 lít khí O2 ở đktc và chất rắn Y, trong Y có %O = 34,5%. Phần 2 đem nhiệt phân hoàn toàn thì thu được 29,1 gam chất rắn. Tính % khối lượng các chất trong X
Gọi số mol KClO3, KMnO4 trong mỗi phần là a, b (mol)
Phần 1:
\(n_{O_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
mY = 122,5a + 158b - 0,1.32 = 122,5a + 158b - 3,2 (g)
Bảo toàn O: \(n_{O\left(Y\right)}=3a+4b-0,2\left(mol\right)\)
\(\%O=\dfrac{16\left(3a+4b-0,2\right)}{122,5a+158b-3,2}.100\%=34,5\%\)
=> 5,7375a + 9,49b = 2,096 (1)
Phần 2:
PTHH: 2KClO3 --to--> 2KCl + 3O2
a----------->a
2KMnO4 --to--> K2MnO4 + MnO2 + O2
b------------>0,5b------>0,5b
=> 74,5a + 142b = 29,1 (2)
(1)(2) => a = 0,2 (mol); b = 0,1 (mol)
=> \(\left\{{}\begin{matrix}\%m_{KClO_3}=\dfrac{0,2.122,5}{0,2.122,5+0,1.158}.100\%=60,8\%\\\%m_{KMnO_4}=\dfrac{0,1.158}{0,2.122,5+0,1.158}.100\%=39,2\%\end{matrix}\right.\)
Đúng 1
Bình luận (0)
Nung 15,8 gam KMnO4 một thời gian thu được 14,84 gam hỗn hợp chất rắn. Cho 14,84 gam hỗn hợp chất rắn đó tác dụng với dd HCl đặc dư thu được V lít khí Cl2 (đktc). Tính V.
\(n_{KMnO_4}=\dfrac{15,8}{158}=0,1\left(mol\right)\)
PTHH: 2KMnO4 --to--> K2MnO4 + MnO2 + O2
a-------------->0,5a----->0,5a
=> 158(0,1-a) + 197.0,5a + 87.0,5a = 14,84
=> a = 0,06 (mol)
PTHH: 2KMnO4 + 16HCl --> 2KCl + 2MnCl2 + 5Cl2 + 8H2O
0,04----------------------------------->0,1
K2MnO4 + 8HCl --> 2KCl + MnCl2 + 2Cl2 + 4H2O
0,03--------------------------------->0,06
MnO2 + 4HCl --> MnCl2 + Cl2 + 2H2O
0,03--------------------->0,03
=> \(n_{Cl_2}=0,1+0,06+0,03=0,19\left(mol\right)\)
=> \(V_{Cl_2}=0,19.22,4=4,256\left(l\right)\)
Đúng 1
Bình luận (0)
Nung nóng hỗn hợp X gồm KMnO4, MnO2 và KClO3 sau một thời gian thu được 1,344 lít khí O2 (đktc) và 15,23 gam hỗn hợp rắn Y. Hòa tan hết 15,23 gam hỗn hợp rắn Y cần dùng dung dịch chứa 0,6 mol HCl, thu được 4,48 lít khí Z (đktc). Phần trăm khối lượng của MnO2 trong hỗn hợp X có giá trị gần nhất với giá trị nào sau đây? A. 30% B. 20% C. 25% D. 40%
Đọc tiếp
Nung nóng hỗn hợp X gồm KMnO4, MnO2 và KClO3 sau một thời gian thu được 1,344 lít khí O2 (đktc) và 15,23 gam hỗn hợp rắn Y. Hòa tan hết 15,23 gam hỗn hợp rắn Y cần dùng dung dịch chứa 0,6 mol HCl, thu được 4,48 lít khí Z (đktc). Phần trăm khối lượng của MnO2 trong hỗn hợp X có giá trị gần nhất với giá trị nào sau đây?
A. 30%
B. 20%
C. 25%
D. 40%
Có 48,2 gam hỗn hợp X gồm KMnO4 và KClO3 được trộn theo tỉ lệ số mol 3 : 4 tương ứng. Nung nóng hổn hợp X một thời gian thì thu được 40,2 gam hỗn hợp chất rắn Y (gồm 6 chất). Cho toàn bộ Y tác dụng với dung dịch HCl đặc (dư) đun nóng, thu được V lít khí Cl2 (đktc). Giá trị của V là?
Đặt : nKMnO4 = 3a(mol)
nKClO3 = 4a (mol)
mX = 3a * 158 + 4a * 122.5 = 48.2 (g)
=> a = 0.05
BTKL :
mO2 = 48.2 - 40.2 = 8 (g)
nO2 = 8/32 = 0.25 (mol)
BT e :
5nKMnO4 + 6nKClO3 = 4nO2 + 2nCl2
=> nCl2 = 5*0.15 + 6*0.2 - 4*0.25 = 0.95 (mol)
VCl2 = 21.28 (l)
Chúc em học tốt và có những trải nghiệm mới tại hoc24.vn !
Đúng 2
Bình luận (0)
Nung nóng 30,005g hỗn hợp X gồm KMnO4, KClO3 và MnO2, sau 1 thời gian thu được khí O2 và nung nóng 24,405g chất rắn Y gồm K2MnO4, KCl. Để tác dụng hết với hh Y cần vừa đủ dd chứa 0,8 mol HCl, thu đc 4,844 lít khí Cl2 ở đktc. Tính thành phần % khối lượng KMnO4 bị nhiệt phân
Nung nóng 30,005g hỗn hợp X gồm KMnO4, KClO3 và MnO2, sau 1 thời gian thu được khí O2 và nung nóng 24,405g chất rắn Y gồm K2MnO4, KCl. Để tác dụng hết với hh Y cần vừa đủ dd chứa 0,8 mol HCl, thu đc 4,844 lít khí Cl2 ở đktc. Tính thành phần % khối lượng KM
Sơ đồ quá trình phản ứng:
Theo bảo toàn khối lượng: mO2= 30,005 – 24,405 = 5,6 (g); ⇒ no2= 0,175 mol;
Bảo toàn e: 5x + 6y + 2z = 0,175×4 + 0,21625×2 = 1,1325;
Bảo toàn H: nH2O= 1/2nHCl = 0,4 mol;
Bảo toàn O: 4x + 3y + 2z = 0,175×2 + 0,4 = 0,75;
Theo bài ra ta có hệ pt:
Ta thấy: 0,0875 mol KClO3 bị nhiệt phân hoàn toàn sinh 0,13125 mol O2
⇒ còn 0,04375 mol O2 nữa là do 0,0875 mol KMnO4;
⇒ %(KMnO4 đã bị nhiệt phân) = ×100% = 72,92% nO4 bị nhiệt phân
Đúng 1
Bình luận (0)
Nung 43,3 gam hỗn hợp gồm KMnO4 và KClO3. Sau một thời gian thu được khí X và chất rắn Y. Nguyên tố Mn chiếm 24,103% khối lượng chất rắn Y. Tính khối lượng của KMnO4 và KClO3 trong hỗn hợp ban đầu. Biết hiệu suất các phản ứng đều đạt 90%.
Gọi n KMnO4 = a
n KClO3 = b ( mol )
--> 158a + 122,5 b = 43,3
PTHH :
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\uparrow\)
0,9b 1,35b
\(2KMnO_4\underrightarrow{t^o}K_2MnO_4+MnO_2+O_2\uparrow\)
0,9a 0,45a
\(\%Mn=\dfrac{55a}{43,3-32\left(0,45a+1,35b\right)}=24,103\%\)
\(\rightarrow a=0,15\)
\(b=0,16\)
\(m_{KMnO_4}=0,15.158=23,7\left(g\right)\)
\(m_{KClO_3}=0,16.122,5=19,6\left(g\right)\)
Đúng 3
Bình luận (0)
đun nóng 22,12 gam kmno4 thu được hỗn hợp chất rắn a và v lít khí o2 (ở đktc). cho lưỡng khí a thu được tác dụng với 10,24 gam cu ở nhiệt độ cao thu được hỗn hợp chất b a, viết cấc pthh xảy ra ? tính v? b, tính khối lượng chất rắn a và chất rắn b? biết các phản ứng xảy ra hoàn toàn 2. xác định khối lượn
2KMnO4-to>K2MnO4+MnO2+O2
0,14-------------0,07------0,07-------0,07 mol
n KMnO4=\(\dfrac{22,12}{158}\)=0,14 mol
=>a=mcr=0,07.197+0,07.87=23,82g
=>VO2=0,07.22,4=1,568l
b)
2Cu+O2-to>2CuO
0,07-----0,14
n Cu=\(\dfrac{10,24}{64}\)=0,16 mol
Cu dư :0,01 mol
m chất rắn =0,01.64+0,14.80=11,84g
Đúng 1
Bình luận (0)