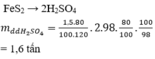trong công nghiệp người ta điều chế H2SO4 từ quặng pirit sắt có thành phần chính là FeS2 theo sơ đồ sau FeS2->SO2->SO3->H2SO4.tính khối lượng H2SO4 98% điều chế được từ 1 tấn quặng chứa 60% FeS2 .Biết hiệu của cả quá trình là 80%

Những câu hỏi liên quan
trong công nghiệp người ta điều chế H2SO4 từ quặng pirit sắt có thành phần chính là FeS2 theo sơ đồ sau
FeS2->SO2->SO3->H2SO4
a) hoàn thành sơ đồ trên bằng các phương trình hóa học (ghi rõ điều kiện)
b) tính khối lượng H2SO4 98% điều chế được từ 1 tấn quặng chứa 60% FeS2 .Biết hiệu của cả quá trình là 80%
Xem chi tiết
a)
\(4FeS_2 + 11O_2 \xrightarrow{t^o} 2Fe_2O_3 + 4SO_2\\ 2SO_2 + O_2 \xrightarrow{t^o,V_2O_5} 2SO_3\\ SO_3 + H_2O \to H_2SO_4\)
b)
\(m_{FeS_2} = 1000.60\% = 600(kg)\\ n_{FeS_2} = \dfrac{600}{120} = 5(kmol)\\ \Rightarrow n_{FeS_2\ pư} = 5.80\% = 4(kmol)\)
Bảo toàn nguyên tố với S : \(n_{H_2SO_4} = 2n_{FeS_2} = 4.2 = 8(kmol)\)
Suy ra :
\(m_{H_2SO_4} = 8.98 = 784(kg)\\ \Rightarrow m_{dd\ H_2SO_4} = \dfrac{784}{98\%} =800(kg)\)
Đúng 1
Bình luận (0)
9. Trong công nghiệp điều chế H2SO4 từ FeS2 theo sơ đồ sau: FeS2 SO2 SO3 H2SO4 a) Viết phương trình phản ứng và ghi rõ điều kiện. b) Tính lượng axit H2SO4 điều chế được từ 1 tấn quặng chứa 60% FeS2. Biết H% của quá trình là 80%.
a)
$4FeS_2 + 11O_2 \xrightarrow{t^o} 2Fe_2O_3 + 8SO_2$
$2SO_2 + O_2 \xrightarrow{t^o,xt} 2SO_3$
$SO_3 + H_2O \to H_2SO_4$
b)
$m_{FeS_2} = 1000.60\% = 600(kg)$
$n_{FeS_2} = \dfrac{600}{120} = 5(kmol)$
$n_{FeS_2\ pư} = 5.80\% = 4(kmol)$
$n_{H_2SO_4} = 2n_{FeS_2} = 8(kmol)$
$m_{H_2SO_4} = 8.98 = 784(kg)$
Đúng 1
Bình luận (0)
4FeS2+11O2to→2Fe2O3+8SO2
4FeS2+11O2→to2Fe2O3+8SO2
2SO2+O2to,xt−−→2SO3
2SO2+O2→to,xt2SO3
SO3+H2O→H2SO4
SO3+H2O→H2SO4
b)
mFeS2=1000.60%=600(kg)
mFeS2=1000.60%=600(kg)
nFeS2=600120=5(kmol)
nFeS2 pư=5.80%=4(kmol)
nFeS2 pư=5.80%=4(kmol)
nH2SO4=2nFeS2=8(kmol)
nH2SO4=2nFeS2=8(kmol)
mH2SO4=8.98=784(kg)
Đúng 0
Bình luận (0)
Trong công nghiệp, axit sunfuric được điều chế từ quặng pirit sắt. Khối lượng dung dịch
H
2
S
O
4
98% điều chế được từ 1,5 tấn quặng pirit sắt có chứa 80%
F
e
S
2
(hiệu suất toàn quá trình là 80%) là A. 0,80 tấn B. 1,60 tấn C. 1,25 tấn D. 2,00 tấn
Đọc tiếp
Trong công nghiệp, axit sunfuric được điều chế từ quặng pirit sắt. Khối lượng dung dịch H 2 S O 4 98% điều chế được từ 1,5 tấn quặng pirit sắt có chứa 80% F e S 2 (hiệu suất toàn quá trình là 80%) là
A. 0,80 tấn
B. 1,60 tấn
C. 1,25 tấn
D. 2,00 tấn
Trong công nghiệp , người ta điều chế axit sunfuric H2SO4 từ quặng pirit sắt theo sơ đồ sau : FeS2 ---- SO2 ---- SO3 ----- H2SO4
a) Viết các phương trình cho dãy P/Ư
b) Nếu dùng 1 tấn quặng có chứa 60% FeS2 thì điều chế đc bao nhiêu lg axit 98% .Biết H80%
c) Muốn điều chế 100g axit 98% vs H như trên thì khối lg quặng cần dùng là bao nhiêu .
, người ta điều chế
Đọc tiếp
Trong công nghiệp , người ta điều chế axit sunfuric H2SO4 từ quặng pirit sắt theo sơ đồ sau : FeS2 ----> SO2 ----> SO3 -----> H2SO4
a) Viết các phương trình cho dãy P/Ư
b) Nếu dùng 1 tấn quặng có chứa 60% FeS2 thì điều chế đc bao nhiêu lg axit 98% .Biết H=80%
c) Muốn điều chế 100g axit 98% vs H như trên thì khối lg quặng cần dùng là bao nhiêu .
, người ta điều chế
Trong công nghiệp người ta sản xuất axít sunfuric theo sơ đồ sau: FeS2
→
SO2
→
SO3
→
H2SO4 . Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axít sunfuric từ quặng trên là: A. 40% B. 60% C. 80% D. 62,5%
Đọc tiếp
Trong công nghiệp người ta sản xuất axít sunfuric theo sơ đồ sau: FeS2 → SO2 → SO3 → H2SO4 . Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axít sunfuric từ quặng trên là:
A. 40%
B. 60%
C. 80%
D. 62,5%
Trong công nghiệp người ta sản xuất axit sunfuric theo sơ đồ sau: FeS2 → SO2 → SO3 → H2SO4. Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axit sunfuric từ quặng trên là: A. 40%. B. 60%. C. 80%. D. 62,5%
Đọc tiếp
Trong công nghiệp người ta sản xuất axit sunfuric theo sơ đồ sau:
FeS2 → SO2 → SO3 → H2SO4.
Người ta sử dụng 15 tấn quặng pirit sắt (chứa 80% FeS2) để sản xuất ra 39,2 tấn dung dịch H2SO4 40%. Vậy hiệu suất chung cho cả quá trình sản xuất axit sunfuric từ quặng trên là:
A. 40%.
B. 60%.
C. 80%.
D. 62,5%
Đáp án C.
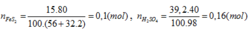
FeS2→ 2H2SO4
0,08 ← 0,16 (mol)
H% = 0,08.100/0,1= 80%
Đúng 0
Bình luận (0)
Trong công nghiệp, axit sunfuric được điều chế từ quang pirit sắt. Khối lượng H2SO4 điều chế được từ 1,5 tấn quặng pirit sắt có chứa 80% FeS2 ( hiệu suất toàn quá trình là 80%) là:
A. 1,568 tấn
B. 1,96 tấn
C. 1,25 tấn
D. 2,00 tấn
Đáp án A.
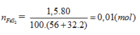
FeS2 → 2H2SO4 (Bảo toàn S)
0,01 → 0,02 (mol)
Do hiệu suất là 80%
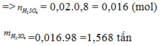
Đúng 0
Bình luận (0)
Từ một tấn quặng pirit sắt chứa 20% tạp chất, điều chế H2SO4 theo phương pháp tiếp xúc theo các giai đoạn sau:
FeS2 --90%--> SO2 --64%--> SO3 --80%--> H2SO4
Tính khối lượng dd H2SO4 72% điều chế được?
mFeS2 = 1.\(\dfrac{80}{100}\) = 0,8 tấn
nFeS2 = \(\dfrac{0,8}{120}\) = \(\dfrac{1}{150}\) mol/ tấn
2FeS2 + \(\dfrac{11}{2}\)O2 \(^{to}\rightarrow\) Fe2O3 + 4SO2 \(\uparrow\)
\(\dfrac{1}{150}\)-------------------------->\(\dfrac{1}{75}\)
- do H = 90% => nSO2(thực tế) = \(\dfrac{1}{75}.\dfrac{90}{100}\) = 0,012mol/tấn
2SO2 + O2 \(^{to}\rightarrow\) 2SO3
0,012------------>0,012
- do H = 64 % => nSO3(thực tế) = 0,012. \(\dfrac{64}{100}\) = 0,00768 mol/ tấn
SO3 + H2O -> H2SO4
0,00768------->0,00768
- do H = 80 % => nH2SO4 = 0,00768 . 80% = 0,006144 mol/tấn
=> mH2SO4 = 0,006144 . 98 = 0,602112 tấn = 602,112 kg
=>mH2SO4(72%) = 602,112 . 72% = 433,52064 kg
Đúng 1
Bình luận (1)
Từ 3 tấn quặng pirit sắt FeS2 (chứa 5% tạp chất) người ta điều chế được bao nhiêu tấn dung dịch H2SO4 98%. Biết hiệu suất của cả quá trình là 80%
ôi t làm nhầm....kq là
3,8 tấn ( cân bằng thêm 2 vào h2so4 là okok)
Đúng 0
Bình luận (2)
FeS2 ==> H2SO4
120g 98g
2,85( vì 5% tạp chất) 2,3275 (tấn)
vì H=80% ====> m H2SO4=1,3965( tấn). nhưng có C% H2SO4= 98%
VẬY mdd H2S04 là 1,425 tấn
Đúng 0
Bình luận (5)