Hòa tan 42g bột hỗn hộp sắt và hỗn hợp đồng bằng lượng dư dung dịch H2SO4 đằng sau phản ứng thu được 5,6l khí sinh ra ở đktc và chất rắn .
a) Viết phương trình hóa học
b) Tính phần trăm khối lượng
Cho 35 g hỗn hợp hai kim loại sắt và đồng tác dụng với dung dịch HCl dư. Sau khi phản ứng xong thu được chất rắn A và 8,96 lít khí (ở đktc).
a)Viết phương trình phản ứng hóa học xảy ra.
b)Tính thành phần trăm theo khối lượng của hỗn hợp ban đầu.
a, \(Fe+2HCl\rightarrow FeCl_2+H_2\)
b, \(n_{H_2}=\dfrac{8,96}{22,4}=0,4\left(mol\right)\)
Theo PT: \(n_{Fe}=n_{H_2}=0,4\left(mol\right)\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Fe}=\dfrac{0,4.56}{35}.100\%=64\%\\\%m_{Cu}=36\%\end{matrix}\right.\)
3. Hòa tan 24,8 gam hỗn hợp bột sắt và đồng trong dung dịch HNO3 loãng thu được 6,72 lít khí NO ( ở đktc).
a. Viết các phương trình phản ứng hóa học
b. Tính thành phần phần trăm về khối lượng của mỗi kim loại trong hỗn h
Gọi \(\left\{{}\begin{matrix}n_{Fe}=a\left(mol\right)\\n_{Cu}=b\left(mol\right)\end{matrix}\right.\)
\(Fe+4HNO_{3l}\rightarrow Fe\left(NO_3\right)_3+NO+2H_2O\)
\(3Cu+8HNO_{3l}\rightarrow3Cu\left(NO_3\right)_2+2NO+4H_2O\)
\(n_{NO}=\dfrac{6,72}{22,4}=0,3mol\)
\(\Rightarrow\left\{{}\begin{matrix}56a+64b=24,8\\BTe:3a+2b=3\cdot0,3\end{matrix}\right.\Rightarrow\left\{{}\begin{matrix}a=0,1\\b=0,3\end{matrix}\right.\)
\(\%m_{Fe}=\dfrac{0,1\cdot56}{24,8}\cdot100\%=22,58\%\)
\(\%m_{Cu}=100\%-22,58\%=77,42\%\)
Hòa tan 8,8g hỗn hợp gồm bột sắt và bột đồng bằng lượng dư dung dịch H2SO4 loãng thu đc 2,24 lit khí sinh ra (đktc) và chất rắn X
a) Tính % (m) các kim loại có trong hỗn hợp
b) hòa tan hoàn tan chất rắn X bằng H2SO4 đặc, thì thu đc bao nhiu lit khí bay ra (đktc)?
Cu không tác dụng với dung dịch H2SO4 loãng
\(n_{H2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,1 0,1
a) \(n_{Fe}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(m_{Fe}=0,1.56=5,6\left(g\right)\)
\(m_{Cu}=8,8-5,6=3,2\left(g\right)\)
0/0Fe = \(\dfrac{5,6.100}{8,8}=63,64\)0/0
0/0Cu = \(\dfrac{3,2.100}{8,8}=36,36\)0/0
b) Có : \(m_{Cu}=3,2\left(g\right)\)
\(n_{Cu}=\dfrac{3,2}{64}=0,05\left(mol\right)\)
Pt : \(Cu+2H_2SO_{4đặc,nóng}\rightarrow CuSO_4+SO_2+2H_2O|\)
1 2 1 1 2
\(n_{SO2}=\dfrac{0,05.1}{1}=0,05\left(mol\right)\)
\(V_{SO2\left(dktc\right)}=0,05.22,4=1,12\left(l\right)\)
Chúc bạn học tốt
Hòa tan 8,8g hỗn hợp gồm bột sắt và bột đồng bằng lượng dư dung dịch H2SO4 loãng thu đc 2,24 lit khí sinh ra (đktc) và chất rắn X
a) Tính % (m) các kim loại có trong hỗn hợp
b) hòa tan hoàn tan chất rắn X bằng H2SO4 đặc, thì thu đc bao nhiu lit khí bay ra (đktc)?
a, \(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH: Fe + H2SO4 → FeSO4 + H2
Mol: 0,1 0,1
\(\%m_{Fe}=\dfrac{0,1.56.100\%}{8,8}=63,64\%;\%m_{Cu}=100-63,64=36,36\%\)
Chất rắn X là Cu (Cu ko tác dụng với H2SO4 loãng)
b,\(n_{Cu}=\dfrac{8,8-5,6}{64}=0,05\left(mol\right)\)
PTHH: Cu + 2H2SO4 (đ) → CuSO4 + SO2 + 2H2O
Mol: 0,05 0,05
\(\Rightarrow V_{SO_2}=0,05.22,4=1,12\left(l\right)\)
Hòa tan hết 54,7 g hỗn hợp A gồm BaO và BaCO3, bằng dung dịch axit HCl 20% ,sau phản ứng thu được 4,48l khi ở đktc và dung dịch X a. Viết phương trình hóa học và tính phần trăm khối lượng mỗi chất trong A? b. Tính khối lượng dung dịch HCl cần dùng? ( Cho biết : Ba-137, O-16 , C-12 , H-1, Cl-35,5)
a. PTHH:
\(BaO+2HCl--->BaCl_2+H_2O\left(1\right)\)
\(BaCO_3+2HCl--->BaCl_2+CO_2\uparrow+H_2O\left(2\right)\)
Ta có: \(n_{CO_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo PT(2): \(n_{BaCO_3}=n_{CO_2}=0,2\left(mol\right)\)
\(\Rightarrow m_{BaCO_3}=0,2.197=39,4\left(g\right)\)
\(\Rightarrow\%_{m_{BaCO_3}}=\dfrac{39,4}{54,7}.100\%=72,03\%\)
\(\%_{m_{BaO}}=100\%-72,03\%=27,97\%\)
b. Ta có: \(m_{BaO}=54,7-39,4=15,3\left(g\right)\)
\(\Rightarrow n_{BaO}=\dfrac{15,3}{153}=0,1\left(mol\right)\)
\(\Rightarrow n_A=0,1+0,2=0,3\left(mol\right)\)
Theo PT(1,2): \(n_{HCl}=2.n_A=2.0,3=0,6\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,6.36,5=21,9\left(g\right)\)
Ta có: \(C_{\%_{HCl}}=\dfrac{21,9}{m_{dd_{HCl}}}.100\%=20\%\)
\(\Rightarrow m_{dd_{HCl}}=109,5\left(g\right)\)
\(n_{CO2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
a) Pt : \(BaO+2HCl\rightarrow BaCl_2+H_2O|\)
1 2 1 1
0,1 0,2
\(BaCO_3+2HCl\rightarrow BaCl_2+CO_2+H_2O|\)
1 2 1 1 1
0,2 0,4 0,2
\(n_{BaCO3}=\dfrac{0,2.1}{1}=0,2\left(mol\right)\)
\(m_{BaCO3}=0,2.197=39,4\left(g\right)\)
\(m_{BaO}=54,7-39,4=15,3\left(g\right)\)
0/0BaO = \(\dfrac{15,3.100}{54,7}=27,97\)0/0
0/0BaCO3 = \(\dfrac{39,4.100}{54,7}=72,03\)0/0
b) Có : \(m_{BaO}=15,3\left(g\right)\)
\(n_{BaO}=\dfrac{15,3}{153}=0,1\left(mol\right)\)
\(n_{HCl\left(tổng\right)}=0,2+0,4=0,6\left(mol\right)\)
\(m_{HCl}=0,6.36,5=21,9\left(g\right)\)
\(m_{ddHCl}=\dfrac{21,9.100}{20}=109,5\left(g\right)\)
Chúc bạn học tốt
nCO2= 4,48 / 22.4= 0,2 ( mol)
a, BaO + 2HCl -> BaCl2 + H2O (1)
BaCO3 + 2HCl-> BaCl2 + H2O + CO2 (2)
0,2 <- 0,2 (mol)
Theo pt (2) ta có nBaCO3= 0,2 => mBaCO3= 0,2 x 197= 39,4 (g)
=> mBaO= 54,7- 39,4= 15.3 (g)
->% BaCO3= ( 39,4 : 54,7)x 100%= 72%
->% BaO= 100%-72% = 28%
Tiến hành phản ứng nhiệt nhôm m gam hỗn hợp A gồm Al và một oxit sắt thu được hỗn hợp chất rắn B. Cho B tác dụng với dung dịch NaOH dư thu được dung dịch C, phần không tan D và 0,672 lít khí H2 (đktc). Cho từ từ dung dịch HCl vào dung dịch C đến khi thu được lượng kết tủa lớn nhất rồi lọc và nung kết tủa đến khối lượng không đổi được 5,1 gam chất rắn. Phần không tan D cho tác dụng hết với dung dịch H2SO4 đặc nóng. Sau phản ứng chỉ thu được dung dịch E chứa một muối sắt duy nhất và 2,688 lít khí SO2 duy nhất (đktc). (Biết các phản ứng xảy ra hoàn toàn; dung dịch E không hòa tan được bột Cu). Thành phần % khối lượng của oxit sắt trong hỗn hợp A là
A. 76,19%.
B. 70,33%.
C. 23,81%.
D. 29,67%.
Đáp án A
· Có n Al ( B ) = 2 3 . n H 2 = 2 3 . 0 , 672 22 , 4 = 0 , 02 mol
· Chất rắn thu được sau khi nung là Al2O3:
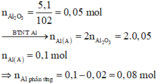
· Quy đổi A tương đương với hỗn hợp gồm 0,1 mol Al, a mol Fe, b mol O
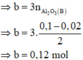
· Phần không tan D gồm Fe và oxit sắt + H2SO4 ® Dung dịch E + 0,12 mol SO2
Dung dịch E chứa một muối sắt duy nhất và không hòa tan được bột Cu
Þ Muối sắt là FeSO4.
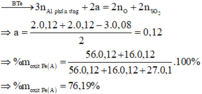
hòa tan hoàn toàn 13,45g hỗn hợp X gồm Al, Fe, Cu trong dung dịch H2SO4 0,5M loãng, dư thì thu được 5,6l khí bay ra ở ĐKTC và còn lại 8g phần rắn Y không tan.
A/ tính phần trăm khối lượng mỗi chất ban đầu
B/ tính thể tích dung dịch H2SO4 tham gia phản ứng
a) Y là Cu
$m_{Cu} = 8(gam)$
Gọi $n_{Al} = a(mol) ; n_{Fe} = b(mol)$
Ta có : $27a + 56b + 8 = 13,45(1)$
$2Al + 3H_2SO_4 \to Al_2(SO_4)_3 + 3H_2$
$Fe + H_2SO_4 \to FeSO_4 + H_2$
$n_{H_2} = 1,5a + b = \dfrac{5,6}{22,4} = 0,25(2)$
Từ (1)(2) suy ra a = 0,15 ; b = 0,025$
$\%m_{Cu} = \dfrac{8}{13,45}.100\% = 59,47\%$
$\%m_{Al} = \dfrac{0,15.27}{13,45}.100\% = 30,11\%$
$\%m_{Fe} = 10,42\%$
b)
$n_{H_2SO_4} = n_{H_2} = 0,25(mol)$
$V_{dd\ H_2SO_4} = \dfrac{0,25}{0,5} = 0,5(lít)$
Hòa tan 10gam hỗn hợp hai kim loại đồng và sắt vào dung dịch axit clohiđric , sau phản ứng thu được 3,36 lit khí (đktc) .
a) Viết phương trình của Hóa Học của phản ứng xảy ra .
b) Tính khối lượng của mỗi kim loại trong hỗn hợp ban đầu .
c) Cho hỗn hợp hai kim loại trên vào dung dịch axit sunfuric đặc nóng thì có những phản ứng nào xảy ra ? Viết phương trình Hóa Học của phản ứng ?
a) Fe +2HCl---> FeCl2 + H2
Cu ko pư nha
nh2= 3.36/22,4=0,15 mol
thế mol h2 vào phương trình ta được
nh2=nfe=0.15
có mol hết rồi thì bạn tìm mfe=0.15x56=8.4(gam)
mcu=mhh-mfe=10-8.4=1.6(gam)
Vì đồng không tác dụng với HCl loãng :
\(n_{H2}=\dfrac{3,36}{22,4}=0,15\left(mol\right)\)
a) Pt : \(Fe+2HCl\rightarrow FeCl_2+H_2|\)
1 2 1 1
0,15 0,15
b) \(n_{Fe}=\dfrac{0,15.1}{1}=0,15\left(mol\right)\)
\(m_{Fe}=0,15.56=8,4\left(g\right)\)
\(m_{Cu}=10-8,4=1,6\left(g\right)\)
c) Cả hai chất đều xảy ra phản ứng :
Pt : \(Cu+H_2SO_{4đặc}\underrightarrow{t^o}CuSO_4+SO_2+H_2O\)
\(2Fe+6H_2SO_{4đặc}\underrightarrow{t^o}Fe_2\left(SO_4\right)_3+3SO_2+6H_2O\)
Chúc bạn học tốt
b) thì chỉ có Cu tác dụng với H2SO4đặc nóng. fe ko phản ứng được
PTHH : Cuo + h2so4 ----> cuso4 + so2 + h2o
Cho 18g hỗn hợp hai kim loại sắt và đồng tác dụng với dd HCl dư. Sau khi phản ứng xong thu được chất rắn A và 4,48l khí (ở đktc)
a. Viết phương trình phản ứng hóa học xảy ra.
b. Tính thành phần phần trăm theo khối lượng của mỗi kim loại trong hỗn hợp ban đầu.
a) $Fe + 2HCl \to FeCl_2 + H_2$
b) Theo PTHH : $n_{Fe} = n_{H_2} = \dfrac{4,48}{22,4} = 0,2(mol)$
$\%m_{Fe} = \dfrac{0,2.56}{18}.100\% = 62,22\%$
$\%m_{Cu} = 100\% - 62,22\% = 37,78\%$