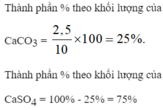Tính CaCo3 ? (Biết Ca = 40, C = 12, O = 16) giúp mik với mấy cậu ơi

Những câu hỏi liên quan
Khối lượng mol của CaCO3 là bao nhiêu? Biết Ca = 40, C = 12, O = 16
\(M_{CaCO_3}=40+12+48=100\left(g\text{/}mol\right)\)
Đúng 3
Bình luận (0)
Tính khối lượng phân tử của các chất sau:H2O,K2O,CaCO3,H2SO4,CO2(biết H=1,C=12,O=16,S=32,K=39,Ca=40
\(H_2O=1.2+16=18< amu>.\)
\(K_2O=39.2+16=94< amu>.\)
\(CaCO_3=40+12+16.3=100< amu>.\)
\(H_2SO_4=1.2+32+16.4=98< amu>.\)
\(CO_2=12+16.2=44< amu>.\)
Đúng 1
Bình luận (0)
Cho biết ý nghĩ công thức hóa học của CaCO3 . :(CA=40;C=12 O=16
- HC đc tạo bởi 3 nguyên tố Ca,C và O
- 1 phân tử CaCO3 có 1 nguyên tử Ca, 1 nguyên tử C và 3 nguyên tử O
- \(PTK_{CaCO_3}=40+12+16\cdot3=100\left(đvC\right)\)
Đúng 1
Bình luận (0)
Cho các CTHH sau: CaCO3; Al2(SO4)3 Hãy tính % khối lượng các nguyên tố có trong mỗi hợp chất (Biết Ca = 40;C= 12; O = 16; Al = 27; S = 32)
Cần gấp ạ
\(M_{CaCO_3}=40+12+16.3=100\left(\dfrac{g}{mol}\right)\\ \%m_{Ca}=\dfrac{40}{100}.100\%=40\%\\ \%m_C=\dfrac{12}{100}.100\%=12\%\\ \%m_O=100\%-\left(12\%+40\%\right)=48\%\\ M_{Al_2\left(SO_4\right)_3}=27.2+\left(32+16.4\right).3=342\left(\dfrac{g}{mol}\right)\\ \%m_{Al}=\dfrac{2.27}{342}.100\%=15,79\%\\ \%m_S=\dfrac{32.3}{342}.100\%=28\%\\ \%m_O=100\%-\left(28\%+15,79\%\right)=56,21\%\)
Đúng 2
Bình luận (0)
Cho 10g CaCO3 tác dụng với dung dịch HCL dư. a,Tính thể tích khí CO2 thu được ở đktc. b,Dẫn khí CO2 thu được vào lọ đựng 25g dung dịch NaOH 40%. Tính khối lượng muối cacbonnat thu được. (biết Ca=40, C=12, O=16, H=1, Na=23, Cl=35,5)
a) CaCO3+2HCl=>CaCl2+H2O+CO2
n CaCO3=10/100 = 0,1 mol
theo phương trình : n CO2 = n CaCO3 = 0,1 mol
=> V CO2 = 0,1*22,4 = 2,24 lít
b) CO2+2NaOH => Na2CO3+H2O
có thể xảy ra phản ứng :
Na2CO3+CO2+H2O=>2NaHCO3
m NaOH = 25*0,4 = 10 gam
=> n NaOH = 10/40 = 0,25 mol
mà nếu theo phương trình đầu tiên của câu b:
n CO2 = 1/2 n NaOH = 1/2*0,25 = 0,125 mol
mà thực tế n CO2 có 0,1 mol
=> n CO2 hết, n NaOH dư
=> chỉ tạo ra 1 muối là Na2CO3
n Na2CO3 = n CO2 = 0,1 mol
=> m Na2CO3 = 0,1*106=10,6 gam
Đúng 1
Bình luận (0)
Tính phân tử khối (khối lượng mol M) của: H2SO4, H3PO4, HCl, HNO3, CaO, SO2, P2O5, MgO, N2O, CaCO3, MgCl2, FeCl3. (Biết: H = 1, Ca = 40, N = 14, O = 16, S = 32, P = 31, Mg = 24, Fe = 56, Cl = 35,5, C = 12)
Lấy 10 g C a C O 3 v à C a S O 4 tác dụng với dung dịch HCl dư tạo thành 0,56 lít khí (đktc). Tính thành phần % theo khối lượng mỗi muối trong hỗn hợp ban đầu. (Ca=40, C=12, O=16, S=32)
BÀI 3: Có sơ đồ phản ứng sau: CaCO 3 +HCl CaCl 2 +CO 2 +H 2 O Tính khối axit clohidric (HCl) tham gia phản ứng vừa đủ với 10 gam canxi cacbonat(CaCo3)(cho Ca=40, C=12, O=16, H=1, Cl=35,5)
\(n C a C O 3 = 10 100 = 0 , 1 ( m o l ) P T H H : C a C O 3 + 2 H C l → C a C l 2 + C O 2 ↑ + H 2 O ⇒ n H C l = 2 n C a C O 3 = 0 , 2 ( m o l ) ⇒ m H C l = 0 , 2 ⋅ 36 , 5 = 7 , 3 ( g )\)
Đúng 1
Bình luận (0)
Ta có: \(n_{CaCO_3}=\dfrac{10}{100}=0,1\left(mol\right)\)
\(PTHH:CaCO_3+2HCl--->CaCl_2+CO_2+H_2O\)
Theo PT: \(n_{HCl}=2.n_{CaCO_3}=2.0,1=0,2\left(mol\right)\)
\(\Rightarrow m_{HCl}=0,2.36,5=7,3\left(g\right)\)
Đúng 0
Bình luận (0)
các bon nát mở ngoặc CaCO3 đóng ngoặc sau một thời gian khối lượng chất rắn giảm 3,8 gam Tính khối lượng của canxi cacbonat đã bị nhiệt phân biết: Fe=56;Zn=65;Mg=24;Cl=35;H=1;C=12;O=16;Ca=40
$CaCO_3 \xrightarrow{t^o} CaO + CO_2$
$m_{CO_2} = m_{giảm} = 3,8(gam)$
$\Rightarrow n_{CO_2} = \dfrac{3,8}{44} (mol)$
Theo PTHH : $n_{CaCO_3\ pư} = n_{CO_2}$
$\Rightarrow m_{CaCO_3\ pư} = \dfrac{3,8}{44}.100 = 8,64(gam)$
Đúng 2
Bình luận (0)