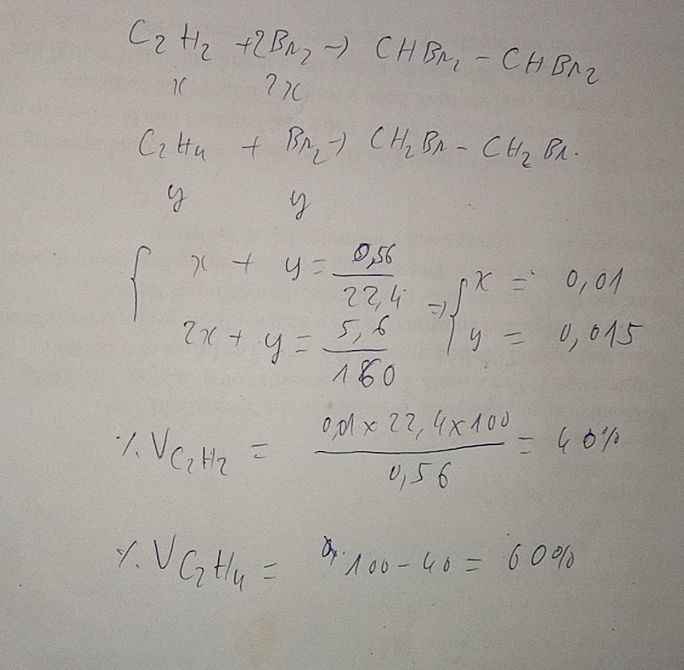Những câu hỏi liên quan
Dẫn 5,6 lít hh gồm etilen và etan vào bình đựng dd brom dư, thấy khối lượng bình đựng dd brom tăng lên 3g. Tính % theo thể tích và theo khối lượng mỗi chất trong hh.
Dẫn 5,6 lít hh gồm etilen và etan vào bình đựng dd brom dư, thấy khối lượng bình đựng dd brom tăng lên 3g. Tính % theo thể tích và theo khối lượng mỗi chất trong hh.
$C_2H_4 + Br_2 \to C_2H_4Br_2$
Ta có :
$m_{C_2H_4} = m_{dd\ tăng} = 3(gam)$
$\Rightarrow n_{C_2H_4} = \dfrac{3}{28}(mol)$
$\Rightarrow n_{C_2H_6} = 0,25 - \dfrac{3}{28} = \dfrac{1}{7}(mol)$
$\%V_{C_2H_4} = \dfrac{ \dfrac{3}{28} }{0,25}.100\% = 42,9\%4
$\%V_{C_2H_6} = 100\% - 42,9\% = 57,1\%$
$\%m_{C_2H_4} = \dfrac{3}{3 + \dfrac{1}{7}.30}.100\% = 41,2\%$
$\%m_{C_2H_6} = 100\% - 41,2\% = 58,8\%$
Đúng 1
Bình luận (0)
$C_2H_4 + Br_2 \to C_2H_4Br_2$
Ta có :
$m_{C_2H_4} = m_{dd\ tăng} = 3(gam)$
$\Rightarrow n_{C_2H_4} = \dfrac{3}{28}(mol)$
$\Rightarrow n_{C_2H_6} = 0,25 - \dfrac{3}{28} = \dfrac{1}{7}(mol)$
$\%V_{C_2H_4} = \dfrac{ \dfrac{3}{28} }{0,25}.100\% = 42,9\%$
$\%V_{C_2H_6} = 100\% - 42,9\% = 57,1\%$
$\%m_{C_2H_4} = \dfrac{3}{3 + \dfrac{1}{7}.30}.100\% = 41,2\%$
$\%m_{C_2H_6} = 100\% - 41,2\% = 58,8\%$
Đúng 0
Bình luận (0)
Dẫn từ từ 1200ml lit hh X( etilen và metan) đi qua bình đựng dd brom dư, thấy có 600ml một chất khí Y thoát ra khỏi bình đựng dd brom.
a. Tính thành phần % thể tích của etilen trong hhX.
b. Tính khối lượng brom tham gia phản ứng.
c. Dẫn Y vào 720 ml khí clo thì tạo thành bao nhiêu g hiđroclorua?
Các thể tích khí đo ở đkt.
a) \(V_{CH_4}=0,6\left(l\right)\)
=> \(\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{0,6}{1,2}.100\%=50\%\\\%V_{C_2H_4}=100\%-50\%=50\%\end{matrix}\right.\)
b) \(n_{C_2H_4}=\dfrac{1,2-0,6}{24}=0,025\left(mol\right)\)
PTHH: C2H4 + Br2 --> C2H4Br2
0,025-->0,025
=> \(m_{Br_2}=0,025.160=4\left(g\right)\)
c)
\(n_{CH_4}=\dfrac{0,6}{24}=0,025\left(mol\right)\)
=> nH = 0,025.4 = 0,1 (mol)
\(n_{Cl_2}=\dfrac{0,72}{24}=0,03\left(mol\right)\)
=> nCl(thế H) = 0,03 (mol)
Do nH > nCl(thế H)
=> H không bị thế hoàn toàn bởi Cl
=> nHCl = 0,03 (mol)
=> mHCl = 0,03.36,5 = 1,095 (g)
Đúng 3
Bình luận (0)
Cho 0,86 lít hỗn hợp khí gồm metan và etilen (đktc) lội qua dd brom dư lượng brom tham gia phản ứng là 5,6 gam
a. Viết PTHH?
b. Tính thành phần phần trăm về thể tích mỗi khí trong hỗn hợp ?
Xem chi tiết
a) \(C_2H_4 + Br_2 \to C_2H_4Br_2\)
b)
\(n_{C_2H_4} = n_{Br_2} = \dfrac{5,6}{160} = 0,035(mol)\\ \%V_{C_2H_4} = \dfrac{0,035.22,4}{0,86}.100\% = 91,16\%\\ \%V_{CH_4} = 100\% - 91,16\% = 8,84\%\)
Đúng 3
Bình luận (1)
Cho hh (A) gồm K2O và K2SO3 tác dụng hoàn toàn với 200g dd HCl 14,6% (vừa đủ), kết thúc phản ứng thu được thu được 6,72 l khí (đktc)
a. Tính thành phần % về khối lượng mỗi chất rắn trong hh đầu.
b. Tính C% của muối trong dd thu được.
PTHH: \(K_2O+2HCl\rightarrow2KCl+H_2O\)
\(K_2SO_3+2HCl\rightarrow2KCl+SO_2\uparrow+H_2O\)
a) Ta có: \(\left\{{}\begin{matrix}n_{HCl}=\dfrac{200\cdot14,6\%}{36,5}=0,8\left(mol\right)\\n_{SO_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\end{matrix}\right.\) \(\Rightarrow\left\{{}\begin{matrix}n_{K_2SO_3}=0,3\left(mol\right)\\n_{K_2O}=0,1\left(mol\right)\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{K_2O}=\dfrac{0,1\cdot94}{0,1\cdot94+0,3\cdot158}\cdot100\%\approx16,55\%\\\%m_{K_2SO_3}=83,45\%\end{matrix}\right.\)
b) Theo các PTHH: \(n_{KCl}=0,8\left(mol\right)\) \(\Rightarrow m_{KCl}=74,5\cdot0,8=59,6\left(g\right)\)
Mặt khác: \(\left\{{}\begin{matrix}m_{hh}=56,8\left(g\right)\\m_{SO_2}=0,3\cdot64=19,2\left(g\right)\end{matrix}\right.\)
\(\Rightarrow m_{dd}=m_{hh}+m_{ddHCl}-m_{SO_2}=237,6\left(g\right)\)
\(\Rightarrow C\%_{KCl}=\dfrac{59,6}{237,6}\cdot100\%\approx25,1\%\)
Đúng 2
Bình luận (2)
Cho 10g hh gồm CH4 , C2H4 tác dụng với 100ml dd Brom 2M Tính thành phần % theo khối lượng của các khí trong hh
$C_2H_4 + Br_2 \to C_2H_4Br_2$
Theo PTHH :
$n_{C_2H_4} = n_{Br_2} = 0,1.2 = 0,2(mol)$
$\%m_{C_2H_4} = \dfrac{0,2.28}{10}.100\% = 56\%$
$\%m_{CH_4} = 100\% - 56\% = 44\%$
Đúng 1
Bình luận (0)
Hòa tan 13,9 g hh Al và Fe vào dd HCl dư thu được V lít khí H2 (đktc) và dd A. Cô cạn dd A thu được 38 g hh muối khan
a. Tính thành phần % khối lượng hh ban đầu và giá trị V
b. Tính khối lượng dd HCl 25% đã lấy biết dùng dư 20% so với lượng phản ứng
Xem chi tiết
a)Gọi x,y lần lượt là số mol của Al, Fe trong hỗn hợp ban đầu (x,y>0)
Sau phản ứng hỗn hợp muối khan gồm: \(\left\{{}\begin{matrix}AlCl_3:x\left(mol\right)\\FeCl_2:y\left(mol\right)\end{matrix}\right.\)
Ta có hệ phương trình: \(\left\{{}\begin{matrix}27x+56y=13,9\\133,5x+127y=38\end{matrix}\right.\Leftrightarrow\left\{{}\begin{matrix}x\approx0,0896\\y\approx0,205\end{matrix}\right.\)
\(\Rightarrow\left\{{}\begin{matrix}\%m_{Al}=\dfrac{0,0896\cdot27\cdot100\%}{13,9}\approx17,4\%\\\%m_{Fe}=\dfrac{0,205\cdot56\cdot100\%}{13,9}\approx82,6\%\end{matrix}\right.\)
Theo Bảo toàn nguyên tố Cl, H ta có:\(n_{H_2}=\dfrac{n_{HCl}}{2}=\dfrac{3n_{AlCl_3}+2n_{FeCl_2}}{2}\\ =\dfrac{3\cdot0,0896+2\cdot0,205}{2}=0,3394mol\\ \Rightarrow V_{H_2}=0,3394\cdot22,4\approx7,6l\)
Đúng 2
Bình luận (0)
3/ Cho 5.6 lít (đktc) hỗn hợp C2H4 và C2H2 tác dụng hết với dd brom dư , thì thấy lượng brom đã phản ứng là 5,6g a/ Viết PTHH b/ tính thành phần % thể tích mỗi chất của hỗn hợp .4/ Đốt cháy hoàn toàn 11,2l hỗn hợp khí metan và etilen cần dùng dùng 25, 88l khí oxi (các khí ở đktc) a/ Viết các PTHH xãy ra .b/ Tính %các chất trong hỗn hợp ban đầu ,c/ Tính thể tích khí CO2 thu đc ở đktcgiải chi tiết giúp mk vớiiii ạ
Đọc tiếp
3/ Cho 5.6 lít (đktc) hỗn hợp C2H4 và C2H2 tác dụng hết với dd brom dư , thì thấy lượng brom đã phản ứng là 5,6g
a/ Viết PTHH
b/ tính thành phần % thể tích mỗi chất của hỗn hợp .
4/ Đốt cháy hoàn toàn 11,2l hỗn hợp khí metan và etilen cần dùng dùng 25, 88l khí oxi (các khí ở đktc)
a/ Viết các PTHH xãy ra .
b/ Tính %các chất trong hỗn hợp ban đầu ,
c/ Tính thể tích khí CO2 thu đc ở đktc
giải chi tiết giúp mk vớiiii ạ
Dẫn từ từ 5,6 lít hỗn hợp gồm metan và etilen đi qua bình đựng dd Brom dư, thấy có 1,12 lít một chất khí thoát ra khỏi bình.
a) Viết PTPƯ, cho biết tên chất khí thoát ra khỏi bình.
b) Tính % thể tích từng chất khí trong hỗn hợp.
c) Tính khối lượng dd Brom đã tham gia phản ứng. Biết các khí đều đo ở đktc.
a, PT: \(C_2H_4+Br_2\rightarrow C_2H_4Br_2\)
Khí thoát ra khỏi bình là CH4 (metan).
b, Ta có: \(\left\{{}\begin{matrix}\%V_{CH_4}=\dfrac{1,12}{5,6}.100\%=20\%\\\%V_{C_2H_4}=100-20=80\%\end{matrix}\right.\)
c, Ta có: \(V_{C_2H_4}=5,6.80\%=4,48\left(l\right)\)
\(\Rightarrow n_{C_2H_4}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
Theo PT: \(n_{Br_2}=n_{C_2H_4}=0,2\left(mol\right)\)
\(\Rightarrow m_{Br_2}=0,2.160=32\left(g\right)\)
Bạn tham khảo nhé!
Đúng 2
Bình luận (0)