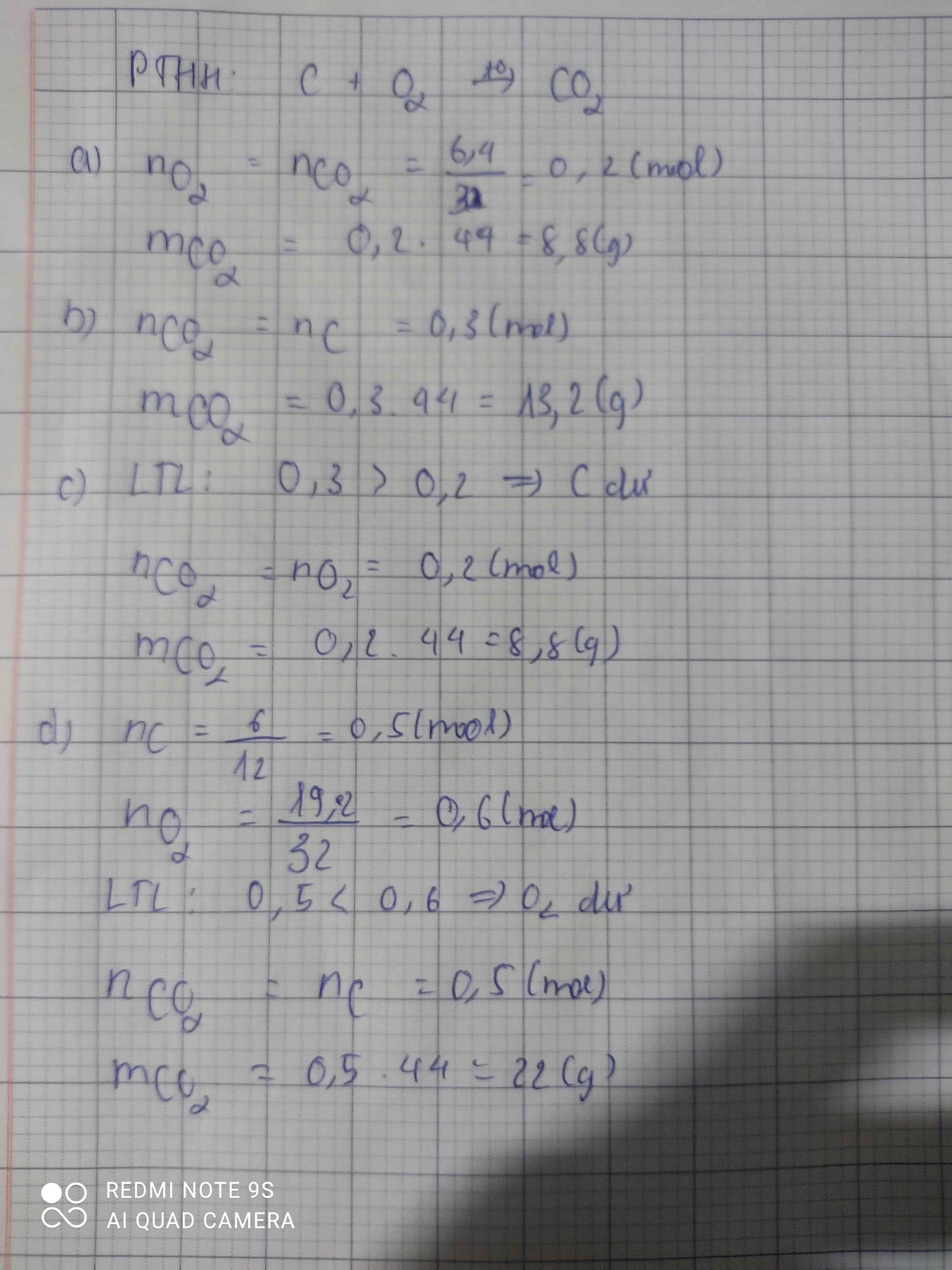Những câu hỏi liên quan
Tính khối lượng khí Cacbon sinh ra trong mỗi trường hợp sau: a) khi đốt 0,3 mol Cacbon trong bình chứa 4,48 lít khí oxi (đktc)
b) khi đốt 6gam Cacbon trong bình chứa 13,44 lít khí oxi (đktc)
Xem chi tiết
C + O2 -to-> CO2
a) nC= 0,3(mol)
nO2=0,2(mol)
Ta có: 0,3/1 > 0,2/1
=> C dư, O2 hết, tính theo nO2.
=> nCO2=nO2=0,2(mol)
=> mCO2= 0,2.44=8,8(l)
b) nC=0,5(mol); nO2=0,6(mol)
Ta có: 0,5/1 < 0,6/1
=> C hết, O2 dư, tính theo nC
=> nCO2=nC=0,5(mol)
=>mCO2=0,5.44=22(g)
Đúng 1
Bình luận (1)
Tính khối lượng khí cacbonic sinh ra trong mỗi trường hợp sau:
a) Khi đốt 0,3 mol cacbon trong bình chứa 4,48 lít khí oxi (đktc)
b) Khi đốt 6 (g) cacbon trong bình chứa 13,44 lít khí oxi
a)
C+O2-to>CO2
0,2---------0,2
nO2=0,2 mol
=>C dư
=>m CO2=0,2.44=8,8g
b) C+O2-to>CO2
0,5------------0,5 mol
n C=0,5 mol
n O2=0,6 mol
=>O2 dư
=>m CO2=0,5.44=22g
Đúng 3
Bình luận (0)
\(a,n_{O_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\\ PTHH:C+O_2\underrightarrow{t^o}CO_2\\ LTL:0,3>0,2\Rightarrow C.du\\ Theo.pt:n_{CO_2}=n_{O_2}=0,2\left(mol\right)\\ m_{CO_2}=0,2.44=8,8\left(g\right)\\ b,n_C=\dfrac{6}{12}=0,5\left(mol\right)\\ n_{O_2}=\dfrac{13,44}{22,4}=0,6\left(mol\right)\\ PTHH:C+O_2\underrightarrow{t^o}CO_2\\ LTL:0,5< 0,6\Rightarrow O_2.du\\ Theo.pt:n_{CO_2}=n_C=0,5\left(mol\right)\\ m_{CO_2}=0,5.44=22\left(g\right)\)
Đúng 4
Bình luận (0)
tính khối lượng khí cacbonicsinh ra trong các trường hợp sau :
a, khi đốt 0,3 mol cacbon trong bình chứa 4,48 lít khí oxi (đktc )
b, khi đốt 6 g cacbon trong bình chứa 13,44 lít khí oxi (đktc)
n O2=4,48:22,4=0,2 mol
pthh
C+O2--->CO2
ta có tỉ lệ 0,3/1>0,2/1
=> C dư O2 hết; ta tính theo O2
theo pthh cứ 0,2 mol O2 tgpu tạo 0,2 mol CO2
=> mCO2=8,8 g
câu b tương tự nhé
Đúng 0
Bình luận (0)
Tính khối lượng khí cacbonic sinh ra trong mỗi trường hợp sau:
a) Khi đốt 0,3 mol cacbon trong bình chứa 4,48 lít khí oxi (đktc)
b) Khi đốt 6 gam cacbon trong bình chứa 13,44 lít khí oxi (đktc)
a) Viết phương trình hoá học của phản ứng đốt cháy cacbon trong oxi. Dựa vào phương trình hoá học và số liệu đề bài cho xem chất nào dư, chất nào tác dụng hết, tính thê tích khí CO2 theo chất tác dụng hết.
mCO2=8,8(g)mCO2=8,8(g)
b) Làm như hướng dẫn giải ở phần a : mCO2=22(g)mCO2=22(g).
Đúng 0
Bình luận (0)
a) nC= 0,3(mol)
nO2= 4,48/22,4 = 0,2(mol)
PTHH: C + O2 -to-> CO2
_________0,2____0,2(mol)
Ta có : 0,2/1 < 0,3/1
=> C dư, O2 hết, tính theo nO2
=> mCO2= 0,2.44=8,8(g)
b) C + O2 -to-> CO2
0,5____________0,5(mol)
Ta có: nC= 6/12 = 0,5(mol)
nO2= 13,44/22,4= 0,6(mol)
Ta có: 0,5/1 < 0,6/1
=> C hết, O2 dư, tính theo nC
=> mCO2= 0,5.44=22(g)
Đúng 0
Bình luận (0)
Câu 1: Tính khối lượng của:
a) 0,15 mol sắt (III) sunfat
b) 0,05 mol magie clorua
c) 0,2 mol khí hidro
d) 4,48 lít khí nito (0 độ C, 1atm)
e) 6,72 lít khí oxi (đktc)
Câu 2: Tính thể tích (đktc) của:
a) 0,25 mol khí nito đioxit
b) 0,3 mol khí cacbon oxit
c) 3,55g khí clo
d) 1,32g khí đinito oxit
Câu 1:
a) \(m_{Fe_2\left(SO_4\right)_3}=0,15.400=60\left(g\right)\)
b) \(m_{MgCl_2}=0,05.95=4,75\left(g\right)\)
c) \(m_{H_2}=0,2.2=0,4\left(g\right)\)
d) \(n_{N_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\Rightarrow m_{N_2}=0,2.28=5,6\left(g\right)\)
e) \(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\Rightarrow m_{O_2}=0,3.32=9,6\left(g\right)\)
Đúng 1
Bình luận (0)
Câu 2:
a) \(V_{NO_2}=0,25.22,4=5,6\left(mol\right)\)
b) \(V_{CO_2}=0,3.22,4=6,72\left(mol\right)\)
c) \(n_{Cl_2}=\dfrac{3,55}{35,5}=0,1\left(mol\right)\Rightarrow V_{Cl_2}=0,1.22,4=2,24\left(l\right)\)
d) \(n_{N_2O}=\dfrac{1,32}{44}=0,03\left(mol\right)\Rightarrow V_{N_2O}=0,03.22,4=0,672\left(l\right)\)
Đúng 0
Bình luận (0)
Tính khối lượng khí cacbonic sinh ra trong mỗi trường hợp sau: Khi đốt 0,3 mol cacbon trong bình chứa 4,48lit khí oxi ( đktc)
Bài 2: Cacbon cháy trong bình đựng khí oxi tạo thành khí cacbonic. Viết PTHH và tính khối lượng khí cacbonic sinh ra trong mỗi trường hợp sau:a. Khi có 6,4g khí oxi tham gia phản ứngb. Khi có 0,3 mol cacbon tham gia phản ứngc. Khi đốt 0,3 mol cacbon trong bình đựng 0,2 mol khí oxid. Khi đốt 6gam cacbon trong bình đựng 19,2 gam khí oxiBài 4: Tính khối lượng oxi cần dùng để đốt cháy hết:a. 46,5 gam Photpho b. 30gam cacbonc. 67,5 gam nhôm ...
Đọc tiếp
Bài 2: Cacbon cháy trong bình đựng khí oxi tạo thành khí cacbonic. Viết PTHH và tính khối lượng khí cacbonic sinh ra trong mỗi trường hợp sau:
a. Khi có 6,4g khí oxi tham gia phản ứng
b. Khi có 0,3 mol cacbon tham gia phản ứng
c. Khi đốt 0,3 mol cacbon trong bình đựng 0,2 mol khí oxi
d. Khi đốt 6gam cacbon trong bình đựng 19,2 gam khí oxi
Bài 4: Tính khối lượng oxi cần dùng để đốt cháy hết:
a. 46,5 gam Photpho b. 30gam cacbon
c. 67,5 gam nhôm d. 33,6 lít hiđro
Bài 5: Người ta đốt cháy lưu huỳnh trong bình chứa 15 gam oxi. Sau phản ứng thu được 19,2 gam khí sunfurơ (SO2)
a. Tính số gam lưu huỳnh đã cháy
b. Tính số gam oxi còn dư sau phản ứng cháy
Bài 6: Một bình phản ứng chứa 33,6 lít khí oxi (đktc). với thể tích này có thể đốt cháy:
a. Bao nhiêu gam cacbon?
b. Bao nhiêu gam hiđro
c. Bao nhiêu gam lưu huỳnh
d. Bao nhiêu gam photpho
Bài 8: Đốt cháy 6,2 gam photpho trong bình chứa 6,72 lít khí oxi (đktc) tạo thành điphotpho pentaoxit.
a. Chất nào còn dư sau phản ứng, với khối lượng là bao nhiêu?
b. Tính khối lượng sản phẩm tạo thành.
Bạn nên đăng 1 baì / 1 lần đăng đêr nhận đc câu trả lời nhanh và chất lượng nhé :v
Đúng 0
Bình luận (0)
Bài 2: Cacbon cháy trong bình đựng khí oxi tạo thành khí cacbonic. Viết PTHH và tính khối lượng khí cacbonic sinh ra trong mỗi trường hợp sau:a. Khi có 6,4g khí oxi tham gia phản ứngb. Khi có 0,3 mol cacbon tham gia phản ứngc. Khi đốt 0,3 mol cacbon...
Xem chi tiết
Câu 1 :
\(2H_2 + O_2 \xrightarrow{t^o} 2H_2O\\ 2Mg + O_2 \xrightarrow{t^o} 2MgO\\ 2Cu + O_2 \xrightarrow{t^o} 2CuO\\ S + O_2 \xrightarrow{t^o} SO_2\\ 4Al + 3O_2 \xrightarrow{t^o} 2Al_2O_3\\ C + O_2 \xrightarrow{t^o} CO_2\\ 4P + 5O_2 \xrightarrow{t^o} 2P_2O_5\)
Đúng 3
Bình luận (0)
Bài 10 :
a) Cu2O : Đồng I oxit ; CuO : Đồng II oxit
b) Al2O3 : Nhôm oxit ; ZnO : Kẽm oxit ; MgO : Magie oxit
c) FeO : Sắt II oxit ; Fe2O3 : Sắt III oxit
d) N2O : Đinito oxit ; NO : Nito oxit ; N2O3: đinito trioxit ; NO2 : nito đioxit
N2O5 : đinito pentaoxit
Đúng 3
Bình luận (0)
Câu 9 :
a)
\(3Fe + 2O_2 \xrightarrow{t^o} Fe_3O_4\\ n_{Fe_3O_4} = \dfrac{2,32}{232} = 0,01(mol)\\ n_{Fe} = 3n_{Fe_3O_4} = 0,03(mol)\Rightarrow m_{Fe} = 0,03.56 =1,68(gam)\\ n_{O_2} = 2n_{Fe_3O_4} = 0,02(mol)\Rightarrow V_{O_2} =0,02.22,4 = 0,448(lít)\)
b)
\(n_{KMnO_4} = 2n_{O_2} = 0,02.2 = 0,04(mol)\\ \Rightarrow m_{KMnO_4} = 0,04.158 = 6,32(gam)\)
Đúng 3
Bình luận (0)
Xem thêm câu trả lời
Cacbon cháy trong bình đựng khí oxi tạo thành khí cacbonic. Viết PTHH và tính khối lượng khí cacbonic sinh ra trong mỗi trường hợp sau: a. Khi có 6,4g khí oxi tham gia phản ứng b. Khi có 0,3 mol cacbon tham gia phản ứng c. Khi đốt 0,3 mol cacbon trong bình đựng 0,2 mol khí oxi d. Khi đốt 6gam cacbon trong bình đựng 19,2 gam khí oxi