
Những câu hỏi liên quan
Tính khối lượng KMnO4 cần dùng để thu được thể tích khí ở đktc vừa đủ tác dụng với 12 gam Photpho. Nếu ko dùng KMnO4. Nếu ko dùng KMnO4 thì cần bao nhiêu gam KClO3 để thu được thể tích khí đủ dùng cho phản ứng trên?
\(n_P=\dfrac{12}{31}mol\)
\(4P+5O_2\underrightarrow{t^o}2P_2O_5\)
\(\dfrac{12}{21}\)\(\rightarrow\)\(\dfrac{5}{7}\)
Khối lượng \(KMnO_4\) cần dùng để thu lượng khí trên:
\(2KMnO_4\underrightarrow{t^o}K_2MnO_2+MnO_2+O_2\)
\(\dfrac{10}{7}\) \(\leftarrow\) \(\dfrac{5}{7}\)
\(\Rightarrow m_{KMnO_4}=\dfrac{10}{7}\cdot158=225,71g\)
Nếu không dùng \(KMnO_4\) mà dùng \(KClO_3\) để thu được khí đủ dùng trên:
\(2KClO_3\underrightarrow{t^o}2KCl+3O_2\)
\(\dfrac{10}{21}\) \(\leftarrow\) \(\dfrac{5}{7}\)
\(m_{KClO_3}=\dfrac{10}{21}\cdot122,5=58,33g\)
Đúng 2
Bình luận (3)
nP = 12/31 (mol)
PTHH: 4P + 5O2 -> (to) 2P2O5
Mol: 12/31 ---> 15/31
2KMnO4 -> (to) K2MnO4 + MnO2 + O2
nKMnO4 = 15/31 . 2 = 30/31 (mol)
mKMnO4 = 30/31 . 158 = 4740/31 (g)
PTHH: 2KClO3 -> (to, MnO2) 2KCl + 3O2
nKClO3 = 30/31 : 3 . 2 = 15/31 (mol)
mKClO3 = 15/31 . 122,5 = 3675/62 (g)
Đúng 0
Bình luận (0)
Khử 0,8g đồng (II) oxit bằng khí hiđro. (Cho Cu = 64; H = 1; O = 16; Cl = 35,5).Hãy: a/Tính số gam đồng kim loại thu được? b/Tính thể tích khí hiđro (đktc) cần dùng? c/Để có lượng H2 đó phải lấy bao nhiêu gam Fe cho tác dụng vừa đủ với bao nhiêu gam dd axit HCl 20
`n_[CuO]=[0,8]/80=0,01(mol)`
`H_2 + CuO` $\xrightarrow{t^o}$ `Cu + H_2 O`
`0,01` `0,01` `0,01` `(mol)`
`a)m_[Cu]=0,01.64=0,64(g)`
`b)V_[H_2]=0,01.22,4=0,224(l)`
`c)`
`Fe + 2HCl -> FeCl_2 + H_2`
`0,01` `0,02` `0,01` `(mol)`
`@m_[Fe]=0,01.56=0,56(g)`
`@m_[dd HCl]=[0,02.36,5]/20 . 100=3,65(g)`
Đúng 4
Bình luận (0)
Cho 2,44 gam hỗn hợp muối N
a
2
C
O
3
và
K
2
C
O
3
tác dụng vừa đủ với dung dịch
H
2
S
O
4
0,5M, sau phản ứng thu được 0,448 lít C
O
2
ở đktc. Thể tích dung dịch H2SO4 0,5 M cần dùng là: A. 100 ml...
Đọc tiếp
Cho 2,44 gam hỗn hợp muối N a 2 C O 3 và K 2 C O 3 tác dụng vừa đủ với dung dịch H 2 S O 4 0,5M, sau phản ứng thu được 0,448 lít C O 2 ở đktc. Thể tích dung dịch H2SO4 0,5 M cần dùng là:
A. 100 ml
B. 40ml
C. 30 ml
D. 25 ml
Chọn B
Đặt x,y lần lượt là số mol của N a 2 C O 3 và (x,y>0)
N a 2 C O 3 + H 2 S O 4 → N a 2 S O 4 + C O 2 + H2O (1)
x mol x mol x mol x mol
K 2 C O 3 + H 2 S O 4 → K 2 S O 4 + C O 2 + H 2 O (2)
y mol y mol y mol y mol
Từ phương trình ta dễ thấy muối cacbonat tác dụng với H 2 S O 4 thì
n H 2 S O 4 = n C O 2
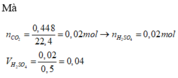
Đúng 0
Bình luận (0)
Cho 10,8 gam kim loại nhôm tác dụng hoàn toàn với dung dịch axit sunfuric loãng (H2SO4). Tính: a. Thể tích hiđro thu được ở đktc? b. Nếu dùng lượng khí Hiđro trên để khử vừa đủ một lượng oxit kim loại X hóa trị II thì thu được 38,4 gam kim loại. Tìm kim loại X.
\(a,n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\\ PTHH:2Al+3H_2SO_{4\left(loãng\right)}\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\\ Theo.pt:n_{H_2}=\dfrac{3}{2}n_{Al}=\dfrac{3}{2}.0,4=0,6\left(mol\right)\\ b,PTHH:RO+H_2\underrightarrow{t^o}R+H_2O\\ Mol:0,6\leftarrow0,6\rightarrow0,6\\ M_R=\dfrac{38,4}{0,6}=64\left(\dfrac{g}{mol}\right)\\ \Rightarrow R.là.Cu\)
Đúng 2
Bình luận (0)
2Al+3H2SO4->Al2(SO4)3+3H2
0,4---------------------------------0,6
n Al=0,4 mol
=>VH2=0,6.22,4=13,44l
b)
H2+XO-to>X+H2O
0,6------------0,6
=>0,6=\(\dfrac{38,4}{X}\)
=>X=64 đvC
=>X là Cu(đồng)
=>X=48
Đúng 1
Bình luận (0)
Cho 5,4 gam kim loại nhôm tác dụng hoàn toàn với dung dịch axit clohiđric (HCl). Tính: a. Thể tích hiđro thu được ở đktc? b. Nếu dùng lượng khí Hiđro trên để khử vừa đủ một lượng oxit kim loại X hóa trị II thì thu được 19,5 gam kim loại. Tìm kim loại X.
2Al+3H2SO4->Al2(SO4)3+3H2
0,2-----------------------------------0,3
n Al=0,2 mol
=>VH2=0,3.22,4=6,72l
b)
XO+H2-to>X+H2O
0,3-------------0,3
=>0,3=\(\dfrac{19,5}{X}\)
=>X là Zn( kẽm)
Đúng 3
Bình luận (0)
a.\(n_{Al}=\dfrac{5,4}{27}=0,2mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,2 0,3 ( mol )
\(V_{H_2}=0,3.22,4=6,72l\)
b.\(n_X=\dfrac{19,5}{M_X}\)
\(XO+H_2\rightarrow\left(t^o\right)X+H_2O\)
\(\dfrac{19,5}{M_X}\) \(\dfrac{19,5}{M_X}\) ( mol )
Ta có:
\(\dfrac{19,5}{M_X}=0,3\)
\(\Leftrightarrow M_X=65\)
=> X là kẽm (Zn)
Đúng 2
Bình luận (0)
\(a,n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\\ PTHH:2Al+6HCl\rightarrow AlCl_3+3H_2\uparrow\\ Theo.pt:n_{H_2}=\dfrac{3}{2}n_{Al}=\dfrac{3}{2}.0,2=0,3\left(mol\right)\\ V_{H_2}=0,3.22,4=6,72\left(l\right)\\ b,PTHH:RO+H_2\underrightarrow{t^o}R+H_2O\\ Mol:0,3\leftarrow0,3\rightarrow0,3\\ M_R=\dfrac{19,5}{0,3}=65\left(\dfrac{g}{mol}\right)\\ \Rightarrow R.là.Zn\)
Đúng 2
Bình luận (0)
Xem thêm câu trả lời
Câu 4: Cho 5,4 gam kim loại nhôm tác dụng hoàn toàn với dung dịch axit clohiđric (HCl).
Tính:
a. Thể tích hiđro thu được ở đktc?
b. Nếu dùng lượng khí Hiđro trên để khử vừa đủ một lượng oxit kim loại X hóa trị II thì thu
được 19,5 gam kim loại. Tìm kim loại X.
a.\(n_{Al}=\dfrac{5,4}{27}=0,2mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,2 0,3 ( mol )
\(V_{H_2}=0,3.22,4=6,72l\)
b.\(XO+H_2\rightarrow\left(t^o\right)X+H_2O\)
\(n_X=\dfrac{19,5}{M_X}\) mol
\(n_{H_2}=n_X=0,3mol\)
\(\Rightarrow\dfrac{19,5}{M_X}=0,3\)
\(M_X=65\) ( g/mol )
=> X là kẽm ( Zn )
Đúng 1
Bình luận (0)
a, nAl = \(\dfrac{5,4}{27}=0,2\left(mol\right)\)
PTHH: 2Al + 6HCl ---> 2AlCl3 + 3H2
0,2 0,6 0,2 0,3
VH2 = 0,3.22,4 = 6,72 (l)
b, PTHH: RO + H2 ---to---> R + H2O
0,3 0,3
=> MR = \(\dfrac{19,5}{0,3}=65\left(\dfrac{g}{mol}\right)\)
=> R là Zn
Đúng 0
Bình luận (0)
VD1:Khử 48 gam sắt (III) oxit bằng khí hiđro. Hãy tính(a) số gam sắt kim loại thu được? (b) thể tích khí hiđro (đktc) cần dùng?(c) thể tích khí oxi (đktc) cần dùng khi tác dụng với hiđro để tạo ra lượng nước gấp đôi lượng nước trong phản ứng trên.
Xem chi tiết
Ta có: \(n_{Fe_2O_3}=\dfrac{48}{160}=0,3\left(mol\right)\)
PT: \(Fe_2O_3+3H_2\underrightarrow{t^o}2Fe+3H_2O\)
_____0,3_____0,9___0,6____0,9 (mol)
a, \(m_{Fe}=0,6.56=33,6\left(g\right)\)
b, \(V_{H_2}=0,9.22,4=20,16\left(l\right)\)
c, PT: \(2H_2+O_2\underrightarrow{t^o}2H_2O\)
Theo PT: \(n_{O_2}=\dfrac{1}{2}n_{H_2O}=0,9\left(mol\right)\)
\(\Rightarrow V_{O_2}=0,9.22,4=20,16\left(l\right)\)
Đúng 3
Bình luận (1)
Câu 2:Tính khối lượng KMnO4 dùng để khi phân hủy thì thu được thể tích khí O2 là 6,72 lít (ở đktc)Câu 3:Cho kẽm tác dụng vừa đủ với HCl. Sau phản ứng thu được 4,48 lít khí hidro ở đktc và muối ZnCl2. tìm khối lượng của kẽm cần dùng cho phản ứng.Câu 4:Cho 22,4g sắt tác dùng vừa đủ với HCl thu được khí hidro và muối FeCl2. Toàn bộ lượng hidro sinh ra cho tác dụng vừa đủ với m (g) CuO. Tìm khối lượng CuO đã tham gia phản ứng (m)
Đọc tiếp
Câu 2:Tính khối lượng KMnO4 dùng để khi phân hủy thì thu được thể tích khí O2 là 6,72 lít (ở đktc)
Câu 3:Cho kẽm tác dụng vừa đủ với HCl. Sau phản ứng thu được 4,48 lít khí hidro ở đktc và muối ZnCl2. tìm khối lượng của kẽm cần dùng cho phản ứng.
Câu 4:Cho 22,4g sắt tác dùng vừa đủ với HCl thu được khí hidro và muối FeCl2. Toàn bộ lượng hidro sinh ra cho tác dụng vừa đủ với m (g) CuO. Tìm khối lượng CuO đã tham gia phản ứng (m)
Câu 2:
\(n_{O_2}=\dfrac{6,72}{22,4}=0,3\left(mol\right)\)
PTHH: \(2KMnO_4\xrightarrow[]{t^o}K_2MnO_4+MnO_2+O_2\)
0,6<------------------------------------0,3
\(\Rightarrow m_{KMnO_4}=0,6.158=94,8\left(g\right)\)
Câu 3:
\(n_{H_2}=\dfrac{4,48}{22,4}=0,2\left(mol\right)\)
PTHH: \(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,2<-----------------------0,2
=> mZn = 0,2.65 = 13 (g)
Câu 4:
\(n_{Fe}=\dfrac{22,4}{56}=0,4\left(mol\right)\)
PTHH: \(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,4------------------------->0,4
\(CuO+H_2\xrightarrow[]{t^o}Cu+H_2O\)
0,4<---0,4
\(\Rightarrow m_{CuO}=0,4.80=32\left(g\right)\)
Đúng 1
Bình luận (0)
Cho 4,8 gam kim loại magie tác dụng hoàn toàn với dung dịch axit HCl. Tính: a. Thể tích hiđro thu được ở đktc? c. Nếu dùng lượng khí Hiđro trên để khử vừa đủ một lượng oxit kim loại R hóa trị II thì thu được 12,8gam kim loại. Tìm kim loại R.
Mg+2HCl->MgCl2+H2
0,2-----------------------0,2
RO+H2-to>R+H2O
0,2-------------0,2
n Mg=\(\dfrac{4,8}{24}\)=0,2 mol
=>VH2=0,2.22,4=4,48l
->0,2=\(\dfrac{12,8}{R}\)
=>R=64 g\mol
=>R là Cu(đồng)
Đúng 2
Bình luận (0)



















