
Những câu hỏi liên quan
Đốt cháy hoàn toàn 7,2 gam kim loại M ( có hoá trị không đổi ) trong hỗn hợp khí Cl2 và O2 . Sau phản ứng thu được 23,0 g chất rắn và thể tích hỗn hợp khí đã phản ứng là 5,6 lít ( đktc ) . Xác định kim loại M.
\(n_{Cl_2}=a\left(mol\right),n_{O_2}=b\left(mol\right)\)
\(n_{hh}=a+b=0.25\left(mol\right)\left(1\right)\)
BTKL :
\(m_{khí}=23-7.2=15.8\left(g\right)\)
\(\Rightarrow71a+32b=15.8\left(2\right)\)
\(\left(1\right),\left(2\right):a=0.2,b=0.05\)
\(2M+nCl_2\underrightarrow{^{^{t^0}}}2MCl_n\)
\(4M+nO_2\underrightarrow{^{^{t^0}}}2M_2O_n\)
\(n_M=\dfrac{0.4}{n}+\dfrac{0.2}{n}=\dfrac{0.6}{n}\left(mol\right)\)
\(M_M=\dfrac{7.2}{\dfrac{0.6}{n}}=12n\)
\(n=2\Rightarrow M=24\)
\(M:Mg\)
Đúng 3
Bình luận (0)
Gọi $n_{Cl_2} = a ; n_{O_2} = b \Rightarrow a + b = 0,25(1)$
Bảo toàn khối lượng :
$7,2 + 71a + 32b = 23(2)$
Từ (1)(2) suy ra a = 0,2 ; b = 0,05
Gọi n là hóa trị M
$2M + nCl_2 \to 2MCl_n$
$4M + nO_2 \xrightarrow{t^o} 2M_2O_n$
Theo PTHH :
$n_M = \dfrac{2}{n}n_{Cl_2} + \dfrac{4}{n}n_{O_2} = \dfrac{0,6}{n}$
$\Rightarrow \dfrac{0,6}{n}.M = 7,2$
$\Rightarrow M = 12n$
Với n = 2 thì $M = 24(Magie)$
Đúng 3
Bình luận (1)
Đốt cháy hoàn toàn 7,2 gam kim loại M (có hoá trị II không đổi trong hợp chất) trong hỗn hợp khí C l 2 và O 2 . Sau phản ứng thu được 23,0 gam chất rắn và thể tích hỗn hợp khí đã phản ứng là 5,6 lít (ở đktc). Xác định kim loại M.
cho 4,365 g kim loại M hóa trị 1 vào 700 ml dd alcl3 0,75 M sau khi phản ứng hoàn toàn thu đc v lít khí h2 đktc và 26,91 g kết tủa . xác định kim loại m
M là kim loại hóa trị 1, cho M vào dung dịch AlCl3 thu được khí H2 và kết tủa
=> M là kim loại kiềm
\(M+H_2O\rightarrow MOH+\dfrac{1}{2}H_2\) (1)
\(3MOH+AlCl_3\rightarrow Al\left(OH\right)_3+3NaCl\) (2)
\(n_{Al\left(OH\right)_3}=\dfrac{26,91}{78}=0,345\left(mol\right)\)
\(n_{AlCl_3}=0,7.0,75=0,525\left(mol\right)\)
Vì \(n_{Al\left(OH\right)_3}< n_{AlCl_3}\) nên:
TH1: AlCl3 phản ứng hết và kết tủa tan 1 phần trong MOH
Al(OH)3 + MOH → MAlO2 + 2H2O (3)
Bảo toàn nguyên tố Al => \(n_{MAlO_2}=0,525-0,345=0,18\left(mol\right)\)
Theo (3) : \(n_{MAlO_2}=n_{MOH}=0,18\left(mol\right)\)
Theo (2) : \(n_{MOH}=3n_{AlCl_3}=0,525.3=1,575\left(mol\right)\)
=> \(\Sigma n_{MOH}=1,575+0,18=1,755\left(mol\right)\)
Theo (1) : \(n_M=n_{MOH}=1,755\left(mol\right)\)
=> \(M_M=\dfrac{4,365}{1,755}=2,49\left(loại\right)\)
TH2: AlCl3 còn dư, MOH phản ứng hết
Theo (2) => \(n_{MOH}=3n_{Al\left(OH\right)_3}=1,035\left(mol\right)\)
Theo (1) => \(n_M=n_{MOH}=1,035\left(mol\right)\)
=> \(M_M=\dfrac{4,365}{1,035}=4,2\left(loại\right)\)
Bạn xem lại đề giúp mình nhé
Đúng 1
Bình luận (0)
Cho 9,6 g một kim loại M chưa biết hóa trị tác dụng với lượng dư khí Oxi rồi cho toàn bộ chất rắn thu được sau phản ứng tan hoàn toàn .Trong dung dịch H2SO4 loãng thấy phải dùng hết 14,7 g Oxit
Xác định kim loại M.
hoà tan hoàn toàn 10,2g một oxit kim loại có hoá trị 3 vào 100g dung dụng h2so4 vừa đủ sau khi phản ứng xảy ra hoàn toàn thu được 34,2 g muối sunfat a)xác định tên kim loại b) tính nồng độ % của dung dịch h2so4 c) tính thể tích dung dịch NaOH 1,5 M cần dùng để kết tủa hoàn toàn dung dịch muối trên
\(Đặt.oxit:A_2O_3\\ A_2O_3+3H_2SO_4\rightarrow A_2\left(SO_4\right)_3+3H_2O\\ n_{Al_2O_3}=\dfrac{34,2-10,2}{96.3-16.3}=0,1\left(mol\right)\\ M_{A_2O_3}=\dfrac{10,2}{0,1}=102\left(\dfrac{g}{mol}\right)=2M_A+48\\ \Rightarrow M_A=27\left(\dfrac{g}{mol}\right)\\ a,\Rightarrow A.là.nhôm\left(Al=27\right)\\ b,n_{H_2SO_4}=3.0,1=0,3\left(mol\right)\\ C\%_{ddH_2SO_4}=\dfrac{0,3.98}{100}.100=29,4\%\\ c,n_{Al_2\left(SO_4\right)_3}=n_{Al_2O_3}=0,1\left(mol\right)\\ Al_2\left(SO_4\right)_3+6NaOH\rightarrow2Al\left(OH\right)_3+3Na_2SO_4\\ n_{NaOH}=6.0,1=0,6\left(mol\right)\\ V_{ddNaOH}=\dfrac{0,6}{1,5}=0,4\left(l\right)\)
Đúng 3
Bình luận (0)
Đốt cháy hoàn toàn 7,2 g kim loại M có hoá trị không đổi cần 5,6 lít hỗn hợp khí gồm Cl2 và O2 (đktc). Phản ứng hoàn toàn thu được 23 g hỗn hợp chất rắn. M là A. Cu. B. Be C. Mg D. Ca
Đọc tiếp
Đốt cháy hoàn toàn 7,2 g kim loại M có hoá trị không đổi cần 5,6 lít hỗn hợp khí gồm Cl2 và O2 (đktc). Phản ứng hoàn toàn thu được 23 g hỗn hợp chất rắn. M là
A. Cu.
B. Be
C. Mg
D. Ca
Giải thích: Đáp án C
Bảo toàn khối lượng m↑ = 23-7,2 =15,8 g
→ hỗn hợp khí có Cl2 : 0,2 mol và O2 :0,05 mol
Đặt hóa trị của M là x
Bảo toàn e có 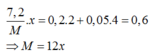
→x=2 và M =24 (Mg)
Đúng 0
Bình luận (0)
Có hh Q gồm kim loại M(có hóa trị II trong hợp chất)oxit và muối clorua của M.Cho20,2g hỗn hợp Q vào dd HCL dư thu đc dd Q1 và 5,6 lít khí H2 (đktc).Lấy toàn bộ dd Q1 cho tác dụng với dd NaOH dư thu đc kết tủa O2.Nung kết tủa O2 đến khối lượng ko đổi thu đc 22g chất rắn.Nếu cũng lấy 20,2g hỗn hợp Q cho vào 300ml dd CuCL2 1M,sau khi phản ứng xong,lọc bỏ chất rắn,làm khô dd thu đc 34,3g muối khan.Giả thiết các phản ứng xảy ra hoàn toàn.Biết rằng kim loại M,oxit của nó ko tan và ko tác dụng với nướ...
Đọc tiếp
Có hh Q gồm kim loại M(có hóa trị II trong hợp chất)oxit và muối clorua của M.Cho20,2g hỗn hợp Q vào dd HCL dư thu đc dd Q1 và 5,6 lít khí H2 (đktc).Lấy toàn bộ dd Q1 cho tác dụng với dd NaOH dư thu đc kết tủa O2.Nung kết tủa O2 đến khối lượng ko đổi thu đc 22g chất rắn.Nếu cũng lấy 20,2g hỗn hợp Q cho vào 300ml dd CuCL2 1M,sau khi phản ứng xong,lọc bỏ chất rắn,làm khô dd thu đc 34,3g muối khan.Giả thiết các phản ứng xảy ra hoàn toàn.Biết rằng kim loại M,oxit của nó ko tan và ko tác dụng với nước ở điều kiện thường ,muối clorua của M tan hoàn toàn trong nước,kim loại M hoạt động hóa học hơn Cu.
a)Viết các pthh và xác định kim loại M
b)Tính thành phần phần trăm về khối lượng các chất trong hỗn hợp Q
Có hh Q gồm kim loại M(có hóa trị II trong hợp chất)oxit và muối clorua của M.Cho20,2g hỗn hợp Q vào dd HCL dư thu đc dd Q1 và 5,6 lít khí H2 (đktc).Lấy toàn bộ dd Q1 cho tác dụng với dd NaOH dư thu đc kết tủa O2.Nung kết tủa O2 đến khối lượng ko đổi thu đc 22g chất rắn.Nếu cũng lấy 20,2g hỗn hợp Q cho vào 300ml dd CuCL2 1M,sau khi phản ứng xong,lọc bỏ chất rắn,làm khô dd thu đc 34,3g muối khan.Giả thiết các phản ứng xảy ra hoàn toàn.Biết rằng kim loại M,oxit của nó ko tan và ko tác dụng với nướ...
Đọc tiếp
Có hh Q gồm kim loại M(có hóa trị II trong hợp chất)oxit và muối clorua của M.Cho20,2g hỗn hợp Q vào dd HCL dư thu đc dd Q1 và 5,6 lít khí H2 (đktc).Lấy toàn bộ dd Q1 cho tác dụng với dd NaOH dư thu đc kết tủa O2.Nung kết tủa O2 đến khối lượng ko đổi thu đc 22g chất rắn.Nếu cũng lấy 20,2g hỗn hợp Q cho vào 300ml dd CuCL2 1M,sau khi phản ứng xong,lọc bỏ chất rắn,làm khô dd thu đc 34,3g muối khan.Giả thiết các phản ứng xảy ra hoàn toàn.Biết rằng kim loại M,oxit của nó ko tan và ko tác dụng với nước ở điều kiện thường ,muối clorua của M tan hoàn toàn trong nước,kim loại M hoạt động hóa học hơn Cu.
a)Viết các pthh và xác định kim loại M
b)Tính thành phần phần trăm về khối lượng các chất trong hỗn hợp Q
đun nóng m gam kim loại M có hóa trị không đổi trong không khí đến khi phản ứng xảy ra hoàn toàn thì thu được oxit có khối lượng 1,25m gam .Để hòa tan hết lượng oxit trên cần 200 g dung dịch H2SO4 19,6% thu được dung dịch X .Xác định kim loại M .Tính nồng độ phần trăm C% của chất tan có trong dung dịch X
Gọi n là hóa trị của M
Phản ứng xảy ra:
4M+nO2→2M2On
Giả sử số mol M là 1 mol.
→nM2On=1/2nM=0,5 mol
→mM=m=1M(M)=M(M)gam
mM2On=0,5.(2MM+16MO)=0,5(2MM+16n)=MM+8n=1,25m
→MM+8n=1,25MM→MM=32n→n=2→MM=64→M:Cu(Đồng)
Hòa tan oxit
CuO+H2SO4→CuSO4+H2O
Ta có:
mH2SO4=200.19,6%=39,2 gam
→nH2SO4=39,298=0,4 mol = nCuO=nCuSO4
→mCuO=0,4.(64+16)=32 gam;mCuSO4=0,4.(64+96)=64 gam
Áp dụng định luật bảo toàn khối lượng:
mddX=mCuO+mddH2SO4=200+32=232 gam
→C%CuSO4=64232=27,5862%
chúc bạn học tốt
Đúng 0
Bình luận (0)
Gọi n là hóa trị của M Phản ứng xảy ra: 4M+nO2→2M2On
Giả sử số mol M là 1 mol.
→nM2On=1/2nM=0,5 mol →mM=m=1M(M)=M(M)gam
mM2On=0,5.(2MM+16MO)=0,5(2MM+16n)=MM+8n=1,25m →MM+8n=1,25MM→MM=32n→n=2→MM=64→M:Cu(Đồng)
Đúng 0
Bình luận (0)




















