Axit sunfuric đặc, dư tác dụng với 10 gam hỗn hợp CuO và Cu thì thu được 2,24 lít khí SO2(đktc). Khối lượng ( gam) của CuO và Cu trong hỗn hợp lần lượt là: ( Cu= 64 ,O=16

Những câu hỏi liên quan
Câu 17:. Axit sunfuric đặc, dư tác dụng với 10 gam hỗn hợp CuO và Cu thì thu được 2,24
lít khí (đktc). Khối lượng ( gam) của CuO và Cu trong hỗn hợp lần lượt là:
Cau 17 :
\(n_{SO2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
Pt : \(Cu+2H_2SO_{4dac,du}\rightarrow CuSO_4+SO_2+2H_2O|\)
1 2 1 1 2
0,1 0,1
\(CuO+H_2SO_4\rightarrow CuSO_4+H_2O|\)
1 1 1 1
\(n_{Cu}=\dfrac{0,1.1}{1}=0,1\left(mol\right)\)
\(m_{Cu}=0,1.64=6,4\left(g\right)\)
\(m_{CuO}=10-6,4=3,6\left(g\right)\)
Chuc ban hoc tot
Đúng 0
Bình luận (0)
Hòa tan hết 50 gam hỗn hợp X gồm Cu và CuO trong H2SO4 đặc, nóng, dư thu được 11,2 lít khí SO2 (sản phẩm khử duy nhất ở đktc). Phần trăm khối lượng của CuO trong hỗn hợp X là A. 64%. B. 36%. C. 32%. D. 68%.
Đọc tiếp
Hòa tan hết 50 gam hỗn hợp X gồm Cu và CuO trong H2SO4 đặc, nóng, dư thu được 11,2 lít khí SO2 (sản phẩm khử duy nhất ở đktc). Phần trăm khối lượng của CuO trong hỗn hợp X là
A. 64%.
B. 36%.
C. 32%.
D. 68%.
Đáp án B
Số mol SO2 thu được là: n SO 2 = 11 , 2 22 , 4 = 0 , 5 mol
Sơ đồ phản ứng:
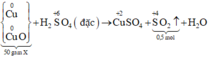
Các quá trình nhường , nhận electron:
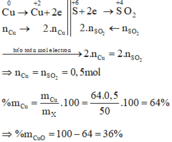
Đúng 0
Bình luận (0)
Cho 2,4 gam hỗn hợp X gồm Fe và Cu tác dụng với dung dịch axit sunfuric loãng , dư thu được V ml khí hidro ( đktc ) . Nếu cho m gam hỗn hợp X đó tác dụng với dung dịch axit sunfuric đặc nóng dư thì thu được 1,12 lít khí sunfurơ ( đktc ) . a . Tính V. b . Tính thành phần phần trăm về khối lượng các chất trong hỗn hợp X. c . Dẫn toàn bộ lượng khí sunfurơ thu được vào 50ml dung dịch NaOH 1,2M . Tính nồng độ mol / l của chất tan trong dung dịch sau phản ứng . Coi thể tích dung dịch không đổi .
Đọc tiếp
Cho 2,4 gam hỗn hợp X gồm Fe và Cu tác dụng với dung dịch axit sunfuric loãng , dư thu được V ml khí hidro ( đktc ) . Nếu cho m gam hỗn hợp X đó tác dụng với dung dịch axit sunfuric đặc nóng dư thì thu được 1,12 lít khí sunfurơ ( đktc ) . a . Tính V. b . Tính thành phần phần trăm về khối lượng các chất trong hỗn hợp X. c . Dẫn toàn bộ lượng khí sunfurơ thu được vào 50ml dung dịch NaOH 1,2M . Tính nồng độ mol / l của chất tan trong dung dịch sau phản ứng . Coi thể tích dung dịch không đổi .
Cho 10 gam hỗn hợp Fe và Cu tác dụng với dung dịch H2 SO4 loãng để điều chế H2 ta thu được 2,24 lít khí H2 ( đktc) . khối lượng của Fe và Cu lần lượt là
Cho hỗn hợp qua dung dịch \(H_2SO_4\) loãng chỉ có Fe tác dụng.
\(\Rightarrow n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\)
\(Fe+H_2SO_4\rightarrow FeSO_4+H_2\)
0,1 0,1
\(m_{Fe}=0,1\cdot56=5,6g\)
\(\Rightarrow m_{Cu}=10-5,6=4,4g\)
Đúng 1
Bình luận (0)
Cho 4 gam hỗn hợp X gồm Fe và Cu tác dụng với dung dịch H2SO4 loãng dư thì thu được 1,12 lít khí (đktc). Thành phần phần trăm theo khối lượng của Fe và Cu trong hỗn hợp X lần lượt là A. 40% và 60%. B. 30% và 70%. C. 70% và 30%. D. 60% và 40%.
Đọc tiếp
Cho 4 gam hỗn hợp X gồm Fe và Cu tác dụng với dung dịch H2SO4 loãng dư thì thu được 1,12 lít khí (đktc). Thành phần phần trăm theo khối lượng của Fe và Cu trong hỗn hợp X lần lượt là
A. 40% và 60%.
B. 30% và 70%.
C. 70% và 30%.
D. 60% và 40%.
Đáp án C
Trong X, chỉ có Fe tác dụng với dung dịch H2SO4 loãng:

Đúng 0
Bình luận (0)
Cho 3,35 gam hỗn hợp gồm Mg, Al, Cu tác dụng hoàn toàn với dung dịch H2SO4 đặc nóng, dư được 2,8 lít khí SO2 (đktc). Khi đốt 3,35 gam hỗn hợp trên trong khí Clo dư thì khối lượng muối clorua thu được là
nSO2 = \(\dfrac{2,8}{22,4}\)=0,125 mol
S+6 + 2e → S+4
0,25<-----0,125
=> Số mol e do 3,35 gam hỗn hợp kim loại nhường là 0,25 mol.
Xét phản ứng với Clo
Kim loại + Cl2 → Muối clorua
Có 3,35 gam kim loại phản ứng nên số mol e kim loại nhường cũng là 0,25 mol
Cl20 + 2e → 2Cl-1
0,25 --> 0,25
=> nCl-1 trong muối clorua = 0,25 mol
<=> mCl-1 = 0,25.35,5 = 8,875 gam.
mMuối = mKim loại + mCl-1 = 3,35 + 8,875 = 12,225 gam.
Đúng 2
Bình luận (0)
Cho 20 gam hỗn hợp gồm Cu và Fe tác dụng với dung dịch HCl dư sinh ra 2,24 lít khí (đktc).% khối lượng của Cu trong hỗn hợp là
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\)
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,1 ( mol )
\(m_{Fe}=0,1.56=5,6g\)
\(\%m_{Cu}=\dfrac{20-5,6}{20}.100=72\%\)
Đúng 2
Bình luận (0)
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\\ PTHH:Fe+2HCl\rightarrow FeCl_2+H_2\uparrow\\ Theo.pt:n_{Fe}=n_{H_2}=0,1\left(mol\right)\\ m_{Fe}=0,1.56=5,6\left(g\right)\\ \%m_{Fe}=\dfrac{5,6}{20}=28\%\\ \%m_{Cu}=100\%-28\%=72\%\)
Đúng 1
Bình luận (0)
Cho 18,2 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (ở đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là A. 42,86% và 26,37%. B. 48,21% và 9,23%. C. 42,86% va 48,21%. D. 48,21% và 42,56%.
Đọc tiếp
Cho 18,2 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (ở đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là
A. 42,86% và 26,37%.
B. 48,21% và 9,23%.
C. 42,86% va 48,21%.
D. 48,21% và 42,56%.
Xét thí nghiệm 2: chú ý tính thụ động hóa của kim loại:
H2SO4 đặc, nguội không phản ứng với Al, Cr, Fe!
⇒ trong X chỉ có Cu phran ứng. Bảo toàn electron: n Cu = n SO 2 = 0 , 075 mol.
Đặt n Cr = x mol; n Fe = y mol → m X 52x + 56y + 0,075 × 64 = 18,2 gam.
x + y = 0,25 mol. Giải hệ có: x = 0,15 mol; y = 0,1 mol.
mCr trong X = 42,86% và %mCu trong X = 26,37%
Đáp án A
Đúng 0
Bình luận (0)
Cho 18,2 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (ở đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là A. 42,86% và 26,37%. B. 48,21% và 9,23%. C. 42,86% va 48,21%. D. 48,21% và 42,56%.
Đọc tiếp
Cho 18,2 gam hỗn hợp X gồm các kim loại Cr, Fe, Cu tác dụng với lượng dư dung dịch H2SO4 loãng, nóng (trong điều kiện không có không khí), thu được dung dịch Y, chất rắn Z và 5,6 lít khí H2 (ở đktc). Nếu cho 18,2 gam hỗn hợp X tác dụng với lượng dư dung dịch H2SO4 đặc, nguội thì thu được 1,68 lít khí SO2 (ở đktc). Thành phần % về khối lượng của crom và đồng trong hỗn hợp X là
A. 42,86% và 26,37%.
B. 48,21% và 9,23%.
C. 42,86% va 48,21%.
D. 48,21% và 42,56%.
Chọn đáp án A
Xét thí nghiệm 2: chú ý tính thụ động hóa của kim loại:
H2SO4 đặc, nguội không phản ứng với Al, Cr, Fe!
⇒ trong X chỉ có Cu phran ứng. Bảo toàn electron: n C u = n S O 2 = 0 , 075 m o l
Đặt nCr = x mol; nFe = y mol ⇒ m X = 52x + 56y + 0,075 × 64 = 18,2 gam.
nH2 = x + y = 0,25 mol. Giải hệ có: x = 0,15 mol; y = 0,1 mol.
⇒ % mCr trong X = 42,86% và %mCu trong X = 26,37%
Đúng 0
Bình luận (0)
















