Có những chất sau: 32g F e 2 O 3 ; 0,125g mol PbO; 28g CuO.
Hãy cho biết: Thành phần phần trăm (Theo khối lượng) mỗi nguyên tố có trong mỗi hợp chất trên.
Có những chất sau: 32g F e 2 O 3 ; 0,125g mol PbO; 28g CuO.
Hãy cho biết: Khối lượng của mỗi kim loại co trong những lượng chất đã cho.

Cứ 1 mol F e 2 O 3 có 2 mol Fe
Vậy 0,2 mol F e 2 O 3 có x? mol Fe
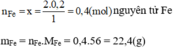
- Trong 0,125 mol phân tử PbO có 0,125 mol nguyên tử Pb.
Khối lượng của Pb = mPb=nPb.MPb=0,125.207=25,875(g)
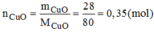
Trong 0,35 mol phân tử CuO có 0,35 mol nguyên tử Cu.
Khối lượng của nguyên tử Cu: M C u = n C u . M C u =0,35.6=22,4(g)
Cho các chất sau: a.CaCO 3 ; b. Fe 3 O 4 ; c. KMnO 4 ; d. H 2 O ; e. KClO 3 ; f. Không khí.
Những chất được dùng để điều chế khí oxi trong phòng thí nghiệm là:
A) a, b, c, d. B) b, c, d. C) c, e. D) c, d, e, f.
dùng 3,6 l hydro(đktc) để khử 32g fe2o3
a,sau phản ứng có mặt những chất nào?
b, tính khối lượng các chất có mặt sau phản ứng
nH2 = \(\dfrac{3,6}{22,4}\) = 0,16 mol
nFe2O3 = \(\dfrac{32}{160}\) = 0,2 mol
3H2 + Fe2O3 -> 2Fe + 3H2O
0,16(hết);0,2(dư) ->0,106 ->0,16
mH2O = 0,106 . 18 = 1,908 g
mFe = 0,16.56 = 8,96 g
a)3H2 + Fe2O3 -> 2Fe + 3H2O
b)nH2 = 3,6/22,4 \(\simeq\)0,16 (mol)
nFe2O3 = 32/160 = 0,2 (mol)
ta có: 0,16/3 < 0,2/1 => H2 hết, Fe2O3 dư
theo Pt ta có: nFe = 2/3.nH2=2/3.0,16\(\simeq\)0,1( mol)
n H2O=nH2=0,16 (mol)
=> m Fe=0,1.56=5,6(g)
mH2O=0,16.18=2,88(g)
Dùng 3,36l H2 (Đktc) để khử 32g Fe2O3
A. Sau phản ứng có mặt những chất nào
B. Tính khối lượng các chất có mặt sau phản ứng
Cho 14,4g Mg tác dụng với 32g Br. Sau khi phản ứng kết thúc rắn thu được gồm những chất nào? Có khối lượng bao nhiêu gam?
\(2Mg+Br_2\rightarrow2MgBr\)
\(n_{Mg}=\frac{14,2}{24}=0,6\left(mol\right)\)
\(n_{Br}=\frac{32}{80}=0,4\left(mol\right)\)
Vì \(\frac{0,6}{2}< 0,4\)
Nên Br dư, các chất tính theo Mg
\(\Rightarrow n_{MgBr}=n_{Mg}=0,6\left(mol\right)\)
\(\Rightarrow m_{MgBr}=0,6.104=62,4\left(g\right)\)
Có những chất sau:
32g Fe2O3;28 g CuO;45g Fe(OH)2;0,125 mol PbO.Hãy cho biết:
A)Khối lượng của mỗi kim loại có trong những lượng chất đã cho.
B)Tính thành phần %(theo khối lượng) của mỗi nguyên tố có trong mỗi hợp chất trên.\
p/s:help me!mk sẽ tick cho!
nFe2O3= 32/160=0.2mol
nCuO=28/80=0.35mol
mPbO=223*0.125=27.875g
số ptu Fe2O3=6*10^23*0.2=1.2*10^23(ptu)
=> số ntu Fe = .2*10^23 * 2= 2.4*10^23(ntu);
mFe = 0.2* 56* 2 = 22.4g
%Fe=(22.4/32)*100%=70%
sô ptu PbO = 6*10^23 * 0.125 = 7.5*10^22(ptu)
=>số ntu Pb=7.5*10^22(ntu)
mPb=0.125*207=25.875g
%Pb=(25.875/27.875)*100%=92.83%
số ptu CuO=6*10^23*0.35=2.1*10^23(ptu)
=>số ntu Cu = 2.1*10^23(ntu)
mCu= 0.35*64=22.4g
%Cu=(22.4/28)*100%=80%
\\tham khảo//
1) 32g Fe2O3
\(n_{Fe_2O_3}=\dfrac{32}{160}=0,2\left(mol\right)\)
Ta có: \(n_{Fe}=2n_{Fe_2O_3}=2\times0,2=0,4\left(mol\right)\)
\(\Rightarrow m_{Fe}=0,4\times56=22,4\left(g\right)\)
\(\%m_{Fe}=\dfrac{22,4}{32}\times100\%=70\%\)
Ta có: \(n_O=3n_{Fe_2O_3}=3\times0,2=0,6\left(mol\right)\)
\(\Rightarrow m_O=0,6\times16=9,6\left(g\right)\)
\(\%m_O=\dfrac{9,6}{32}\times100\%=30\%\)
2) 28g CuO
\(n_{CuO}=\dfrac{28}{80}=0,35\left(mol\right)\)
Ta có:\(n_{Cu}=n_O=n_{CuO}=0,35\left(mol\right)\)
\(\Rightarrow m_{Cu}=0,35\times64=22,4\left(g\right)\)
\(\%m_{Cu}=\dfrac{22,4}{28}\times100\%=80\%\)
\(m_O=0,35\times16=5,6\left(g\right)\)
\(\%m_O=\dfrac{5,6}{28}\times100\%=20\%\)
3) 45g Fe(OH)2
\(n_{Fe\left(OH\right)_2}=\dfrac{45}{90}=0,5\left(mol\right)\)
Ta có: \(n_{Fe}=n_{Fe\left(OH\right)_2}=0,5\left(mol\right)\)
\(\Rightarrow m_{Fe}=0,5\times56=28\left(g\right)\)
\(\%m_{Fe}=\dfrac{28}{45}\times100\%=62,22\%\)
Ta có: \(n_O=n_H=2n_{Fe\left(OH\right)_2}=2\times0,5=1\left(mol\right)\)
\(\Rightarrow m_O=1\times16=16\left(g\right)\)
\(\%m_O=\dfrac{16}{45}\times100\%=35,56\%\)
\(m_H=1\times1=1\left(g\right)\)
\(\%m_H=\dfrac{1}{45}\times100\%=2,22\%\)
4) 0,125 mol PbO
\(m_{PbO}=0,125\times223=27,875\left(g\right)\)
Ta có: \(n_{Pb}=n_O=n_{PbO}=0,125\left(mol\right)\)
\(\Rightarrow m_{Pb}=0,125\times207=25,875\left(g\right)\)
\(\%m_{Pb}=\dfrac{25,875}{27,875}\times100\%=92,83\%\)
\(m_O=0,125\times16=2\left(g\right)\)
\(\%m_O=\dfrac{2}{27,875}\times100\%=7,17\%\)
1)trong các hợp chất sau, hợp chất nào thuộc loại oxit?
a. K2O b.Mg(OH)2 c. SO3 d. CuSO4 e. H2S f. Fe2O3
2)trong những chất sau, những chất nào là oxit axit, những chất nào là oxit bazơ?
NO, BaO, P2O5, Na2O, CuO, Al2O3, SO2, CO, Mn2O7
3) đọc tên các oxit sau: BaO, P2O5, K2O, CuO
4)lập CTHH của 1 loại đồng oxit. biết khối lượng mol của nó là 80(g) và có chứa 80% Cu, 20% O về khối lượng.
1) Hợp chất a, c, f
2) Oxit axit: P2O5, SO2, Mn2O7
Oxit bazơ: BaO, Na2O, CuO, Al2O3
3)
BaO: Bari oxit
P2O5: điphotpho pentaoxit
K2O: Kali oxit
CuO: Đồng (II) oxit
4) Khối lượng đồng trong oxit là \(80.80\%=64\left(g\right)\)
=> \(n_{Cu}=\frac{64}{64}=1\left(mol\right)\)
Khối lượng oxi trong oxit là \(80-64=16\left(g\right)\)
=> \(n_O=\frac{16}{16}=1\left(mol\right)\)
=> CTHH: CuO
Cho các hợp chất sau:
( a ) H O C H 2 - C H 2 O H . ( b ) H O C H 2 - C H 2 - C H 2 O H . ( c ) H O C H 2 - C H ( O H ) - C H 2 O H . ( d ) C H 3 - C H ( O H ) - C H 2 O H . ( e ) C H 3 - C H 2 O H . ( f ) C H 3 - O - C H 2 C H 3 .
Trong các hợp chất trên, những chất đều tác dụng được với Na, C u ( O H ) 2 là
A. (a), (b), (c).
B. (c), (d), (f)
C. (a), (c), (d)
D. (c), (d), (e)
C
Các hợp chất tác dụng được với Na và C u ( O H ) 2 là các ancol có các nhóm – OH cạnh nhau
Tính khối lượng của mỗi nguyên tố có trong thành phần các chất của:
a)32g Fe2O3
b)1,25 mol PbO
c)1,68 lít khí CO2(đktc)
a/ nFe2O3 = 32 / 160 = 0,2 mol
=> nFe = 2nFe2O3 = 0,4 mol
=> mFe = 0,4 x 56 = 22,4 gam
=> nO = 3nFe2O3 = 0,6 mol
=> mO = 0,6 x 16 = 9,6 gam
b, c/ Bạn tự làm nhé! Nó tương tự phần a nhé!!!