Lưu huỳnh cháy trong không khí sinh ra khí sunfurơ, theo phản ứng sau:
S + O 2 − t o → S O 2
Hãy cho biết:
Những chất tham gia và tạo thành trong phản ứng trên, chất nào là đơn chất, chất nào là hợp chất? Vì sao?
Lưu huỳnh cháy trong không khí sinh ra khí sunfurơ, theo phản ứng sau:
S + O 2 − t o → S O 2
Hãy cho biết:
Khí sunfurơ nặng hay nhẹ hơn không khí. Hãy giải thích.
Lưu huỳnh cháy trong không khí sinh ra khí sunfurơ, theo phản ứng sau:
S + O 2 − t o → S O 2
Hãy cho biết:
Thể tích khí oxi ở đktc cần dùng để đốt cháy hoàn toàn 2,5 mol nguyên tử lưu huỳnh.
Lưu huỳnh (S) cháy trong không khí sinh ra chất khí mùi hắc, gây ho đó là lưu huỳnh đioxit (khí sunfurơ) có công thức hóa học là SO2.
a) Viết phương trình hóa học của lưu huỳnh cháy trong không khí.
b) Biết khối lượng lưu huỳnh tham gia phản ứng là 1,6g. Hãy tìm.
-Thể tích khí sunfurơ sinh ra ở đktc.
-Thể tích không khí cần dùng ở đktc. Biết oxi chiếm 1/5 thể tích không khí.
a) Phương trình hóa học S + O2 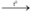 SO2
SO2
b) nS = 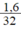 = 0,05 mol.
= 0,05 mol.
Theo phương trình trên, ta có:
nSO2 = nS = nO2 = 0,05 mol.
⇒ VSO2 = 0,05 .22,4 = 1,12 l.
⇒ VO2 = 22,4.0,05 = 1,12 l
Vì khí oxi chiếm 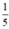 thể tích của không khí nên thể tích không khí cần là
thể tích của không khí nên thể tích không khí cần là
⇒ Vkk = 5VO2 = 5.1,12 = 5,6 l
Lưu huỳnh cháy theo sơ đồ phản ứng sau: Lưu huỳnh + khí oxi → khí sunfurơ. Nếu đã có 32g lưu huỳnh cháy và thu được 64g khí sunfurơ thì khối lượng oxi đã tham gia phản ứng là
A.
32g
B.
48g
C.
40g
D.
44g
Theo ĐLBTKL, ta có:
mS + mO2 = mSO2
\(\Rightarrow m_{O_2}=64-32=32g\)
=> A
Câu 14: (1.5đ). Cho 3,2 gam lưu huỳnh cháy trong khí oxi sau phản ứng thu được khí sunfurơ (SO2 ) a. Lập phương trình phản ứng? b. Tính khối lượng oxi tham gia phản ứng và thể tích SO2 sinh ra ở (đktc). Cho biết : S =32 ; O2 =16
a) $S + O_2 \xrightarrow{t^o} SO_2$
b)
Theo PTHH :
$n_{O_2} = n_{SO_2} = n_S = \dfrac{3,2}{32} = 0,1(mol)$
$m_{O_2} = 0,1.32 = 3,2(gam)$
$V_{SO_2} = 0,1.22,4 = 2,24(lít)$
Ta có: n S = 3,2 / 32 = 0,1 ( mol )
PTHH: S + O2 \(\rightarrow\) SO2
0,1--0,1-----0,1
Theo pthh
n O2 = 0,1 ( mol ) => m O2 = 3,2 ( g )
n SO2 = 0,1 ( mol ) => V SO2 = 2,24 ( lít )
: Lưu huỳnh (S) cháy trong không khí sinh ra khí sunfurơ (SO2). Hãy cho biết:
a) Những chất tham gia và tạo thành trong phản ứng trên, chất nào là đơn chất, chất nào là hợp chất ? Vì sao ?
b) Thể tích khí oxi (đktc) cần dùng để đốt cháy hoàn toàn 4,8 g lưu huỳnh
a) Khí sunfurơ nặng hay nhẹ hơn không khí bằng bao nhiêu lần?
Câu 14: Cho 13gam Zn tác dụng với dung dịch H2SO4 thu được ZnSO4 và khí hidro Tính:
a. Thể tích khí H2 thu được ở đktc.
b. Khối lượng H2SO4 phản ứng.
c. Khối lượng ZnSO4 tạo thành.
Câu 15: Cho một hợp chất sắt oxit có tỉ lệ khối lượng giữa sắt và oxi là:
mFe : mO = 7 : 3
a. Hãy xác định công thức phân tử của hợp chất oxit nói trên.
b. Tính số mol của 32g oxit nói trên.
ai chỉ mik vứ
Câu 13:
a) PTHH: \(S+O_2\underrightarrow{t^o}SO_2\)
Chất tham gia: \(S;O_2\)
Chất sp: \(SO_2\)
Đơn chất: \(S;O_2\)
Hợp chất: \(SO_2\)
Vì đơn chất là những chất được tạo từ 1 nguyên tố. Còn hợp chất là chất được tạo từ 2 nguyên tố trở lên.
b) \(n_S=\dfrac{4,8}{32}=0,15\left(mol\right)\)
Từ PTHH ở trên ta có:
1 mol S thì đốt cháy hết 1 mol khí oxi
=> 0,15 mol S thì đốt cháy hết 0,15 mol khí oxi
=> Thể tích của 0,15 khí oxi là:
\(V_{O_2}=0,15.22,4=3,36\left(l\right)\)
Câu 13:
c) \(d_{\dfrac{S}{kk}}=\dfrac{32}{29}>1\)
Lưu huỳnh (S) cháy trong không khí sinh ra khí sunfurơ (SO2). Hãy cho biết:
a) Những chất tham gia và tạo thành trong phản ứng trên, chất nào là đơn chất, chất nào là hợp chất ? Vì sao ?
b) Thể tích khí oxi (đktc) cần dùng để đốt cháy hoàn toàn 4,8 g lưu huỳnh
a) Khí sunfurơ nặng hay nhẹ hơn không khí bằng bao nhiêu lần?
a) S + O2 -> SO2
Chất tham gia phản ứng là S và O2
Chất tạo thành phản ứng là SO2
b) \(n_S=\dfrac{4,8}{32}=0,15\left(mol\right)\)
Thể tích khí oxi (đktc) cần dùng để đốt cháy hoàn toàn 4,8 g lưu huỳnh
\(V_{O_2}=0,15.22,4=3,36\left(l\right)\)
c) dSO2/kk= \(\dfrac{M_{SO_2}}{M_{kk}}=\dfrac{32+16.2}{29}=\dfrac{64}{29}=2.2>1\)
=> Khí sunfurơ nặng hơn không khí 2,2 lần
Tính số mol khí sunfurơ sinh ra trong mỗi trường hợp sau:
a. Có 1,5 mol khí oxi tham gia phản ứng với lưu huỳnh
b. Đốt cháy hoàn toàn 38,4 gam lưu huỳnh trong khí oxi.
cứu![]()
a, S + O2 \(\underrightarrow{t^o}\) SO2
=> \(n_{SO_2}=1,5mol\)
b, \(n_S=\dfrac{37,4}{32}=1,168mol\)
\(n_{SO_2}=1,168mol\)
a) PTHH : S + O2 -> SO2
\(n_{SO_2}=\dfrac{1,5}{1}=1,5\left(mol\right)\)
b) \(n_S=\dfrac{38,4}{32}=1,2\left(mol\right)\)
\(n_{SO_2}=1,2\left(mol\right)\)