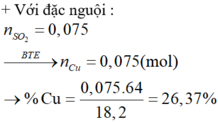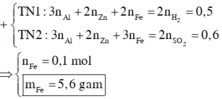Cho a gam hỗn hợp gồm Fe và FeO tác dụng với dung dịch H2SO4 loãng dư thu được 2,24 lít khí H2 (đktc). Mặc khác, nếu cho cùng lượng hỗn hợp trên tác dụng với dung dịch H2SO4 đặc nóng dư thì thu được 5,6 lít khí SO2 (đktc). Giá trị của a là?
Mọi người giải giúp em theo phương pháp bảo toàn e với ạ !. Em cần gấp . Xin cảm ơn !