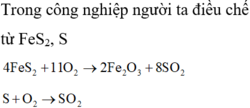Có bao nhiêu mol FeS2 tác dụng hết với oxi để thu được 64g khí SO2 theo phương trình hóa
học sau: 4FeS2 + 11O2 → 2Fe2O3 + 8SO2

Những câu hỏi liên quan
Cho PTHH :
4
FeS
2
+
11
O
2
→
2
Fe
2
O
3
+
8
SO
2
Cần đốt cháy bao nhiêu mol...
Đọc tiếp
Cho PTHH :
4 FeS 2 + 11 O 2 → 2 Fe 2 O 3 + 8 SO 2
Cần đốt cháy bao nhiêu mol FeS 2 để thu được 64 gam SO 2 theo PTHH trên ?
A. 0,4 mol. B. 0,5 mol.
C. 0,8 mol. D. 1,2 mol.
Có các phản ứng sinh ra khí SO2
(
1
)
4
F
e
S
2
+
11
O
2
→
2
F
e
2
O
3
+
8
S
O
2
(
2
)
S
+
O
2
→
S
O
2
(
3
)
C
u
+...
Đọc tiếp
Có các phản ứng sinh ra khí SO2
( 1 ) 4 F e S 2 + 11 O 2 → 2 F e 2 O 3 + 8 S O 2
( 2 ) S + O 2 → S O 2 ( 3 ) C u + 2 H 2 S O 4 → N a 2 S O 4 + S O 2 + H 2 O
( 4 ) N a 2 S O 3 + H 2 S O 4 → N a 2 S O 4 + S O 2 + H 2 O
Các phản ứng được dùng để điều chế khí SO2 trong công nghiệp là
A. (1) và (2).
B. (2) và (3).
C. (2) và (4).
D. (1), (2) và (3).
a) Xác định biến thiên enthalpy của phản ứng sau ở điều kiện chuẩn:
4FeS2 (s) + 11O2 (g) → 2Fe2O3 (s) + 8SO2 (g)
Biết nhiệt tạo thành ΔrH0298 của các chất FeS2(s), Fe2O3(s) và SO2(g) lần lượt là -177,9 kJ/mol,
-825,5 kJ/mol và -296,8 kJ/mol.
\(\Delta_rH^o_{298}=2\left(-825,5\right)+8\left(-296,8\right)-4\left(-177,9\right)\\ \Delta_rH^o_{298}=-3313,8\left(kJ\right)\)
Đúng 2
Bình luận (0)
4FeS2+11O2------> 2Fe2O3+8SO2
a,Nếu lấy 100kg FeS2 thì sau phản ứng thu được bao nhiêu kg SO2?
b,Tính Vkk(đktc) cần cho phản ứng
c,Số kg chất rắn thu được
\(n_{FeS_2}=\dfrac{10^5}{120}\left(mol\right)\)
\(4FeS_2+11O_2\underrightarrow{t^0}2Fe_2O_3+8SO_2\)
\(n_{SO_2}=2n_{FeS_2}=2\cdot\dfrac{10^5}{120}=\dfrac{10^5}{60}\left(mol\right)\)
\(m_{SO_2}=\dfrac{10^5}{60}\cdot64=1.06\cdot10^5\left(g\right)=106\left(kg\right)\)
\(V_{kk}=5V_{O_2}=5\cdot\dfrac{11}{4}\cdot\dfrac{10^5}{120}\cdot22.4=256666\left(l\right)\)
\(m_{Fe_2O_3}=\dfrac{10^5}{240}\cdot160=0.6\cdot10^5\left(g\right)=90\left(kg\right)\)
Đúng 1
Bình luận (0)
a) Ta có: \(n_{FeS_2}=\dfrac{100}{120}=\dfrac{5}{6}\left(kmol\right)\)
\(\Rightarrow n_{SO_2}=\dfrac{5}{3}\left(kmol\right)\) \(\Rightarrow m_{SO_2}=\dfrac{5}{3}\cdot64\approx106,67\left(kg\right)\)
b) Theo PTHH: \(n_{O_2}=\dfrac{11}{4}n_{FeS_2}=\dfrac{55}{24}\left(kmol\right)=\dfrac{6875}{3}\left(mol\right)\)
\(\Rightarrow V_{O_2}=\dfrac{6875}{3}\cdot22,4=\dfrac{154000}{3}\left(l\right)\)
Mà Oxi chiếm khoảng 20% thể tích không khí
\(\Rightarrow V_{kk}=\dfrac{\dfrac{154000}{3}}{20\%}\approx256666,7\left(l\right)\)
c) Theo PTHH: \(n_{Fe_2O_3}=\dfrac{1}{2}n_{FeS_2}=\dfrac{5}{12}\left(kmol\right)\)
\(\Rightarrow m_{Fe_2O_3}=\dfrac{5}{12}\cdot160=66,67\left(kg\right)\)
Đúng 1
Bình luận (0)
a) nFeS2=\(\dfrac{100}{120}=\dfrac{5}{6}\left(mol\right)\)
+nSO2=2nFeS2=\(\dfrac{5}{3}\)(mol)
+mSO2=\(\dfrac{5}{3}\).64 ≈ 106,6(Kg)
b)+nO2=2,75nFeS2=\(\dfrac{55}{24}\left(mol\right)\)
VO2=\(\dfrac{55}{24}.22,4\approx51,3\left(lit\right)\)
c) nFe2O3=\(\dfrac{1}{2}\)nFeS2=\(\dfrac{5}{12}\)(mol)
+mFeSO3=\(\dfrac{5}{12}.178=74,1\left(Kg\right)\)
Đúng 0
Bình luận (2)
Xem thêm câu trả lời
Câu 5: Đốt cháy quặng pirit trong khí Oxi theo sơ đồ sau: 4FeS2 + 11O2 → 4Fe + 8SO2. Nếu đốt 7,2 gam FeS2 trong 6,72 lít khí O2 (đktc) thì khối lượng sắt thu được là:
A. 9,24 gam B. 6,109 gam C. 6,2 gam D. 3,36 gam
Câu 6: Khối lượng nước cần dùng để pha chế 350g dung dịch FeCl2 12,7%
A. 305,55 gamB. 251,9 gamC. 38,1 gamD. 261,9 gam
Câu 8: Trong 225gam nước cất có hoà tan 25g KCl. C% của dung dịch là:
A. 10%...
Đọc tiếp
Câu 5: Đốt cháy quặng pirit trong khí Oxi theo sơ đồ sau: 4FeS2 + 11O2 → 4Fe + 8SO2. Nếu đốt 7,2 gam FeS2 trong 6,72 lít khí O2 (đktc) thì khối lượng sắt thu được là: A. 9,24 gam B. 6,109 gam C. 6,2 gam D. 3,36 gam Câu 6: Khối lượng nước cần dùng để pha chế 350g dung dịch FeCl2 12,7% A. 305,55 gamB. 251,9 gamC. 38,1 gamD. 261,9 gam Câu 8: Trong 225gam nước cất có hoà tan 25g KCl. C% của dung dịch là: A. 10% B. 11% C. 12% D. 13% Câu 9: Đốt cháy hết a (gam) CH4 trong khí O2 thu được 4,48 lít khí CO2 (đktc) . Giá trị của a là: A. 4,6 (gam) B. 3,2 (gam) C. 0,8 (gam) D. 1,6 (gam) Mong có thể kèm cách giải để mình hiểu bài hơn ạ :( mình cảm ơn
Nung quặng pyrit không khí có phản ứng hóa học:
4FeS2+11O2->2Fe2O3+SO2
Nếu nung hoàn toàn 12g FeS2(hiệu suất phản ứng 100%) tính
a/K/lg Fe2O3 thu được sau phản ứng
b/Thể tích khí SO2 sinh ra ở đktc
c/Vkk ở đktc cần để phản ứng xảy ra hoàn toàn biết oxi chiếm 1/5kk
\(n_{FeS_2}=\dfrac{12}{120}=0,1\left(mol\right)\)
PT: 4FeS2 + 11O2 → 2Fe2O3 + SO2
mol 0,1 → 0,275 0,05 0,025
a) \(m_{Fe_2O_3}=0,05.160=8\left(g\right)\)
b) \(V_{SO_2\left(đktc\right)}=0,025.22,4=0,56\left(l\right)\)
d) Vkhông khí (đktc) = (0,275.22,4).5 = 30,8 (g)
Đúng 0
Bình luận (0)
Cho dãy các chất sau : Mg , Al2O3 , Ag , Fe , C , Br2 , S ,CuO , FeS2 , C2H6O , So2 , CaO , O2 a ) Chất nào tác dụng với khí oxi b ) chất nào tác dụng với khí hidro . Viết phương trình hóa học nếu có
a)
2Mg+O2-to>2MgO
3Fe+2O2-to>Fe3O4
C+O2-to>CO2
S+O2-to>SO2
2FeS2+\(\dfrac{11}{2}\)O2-to>Fe2O3+4SO2
C2H6O+3O2-to>2CO2+3H2O
b)
S+H2-to>H2S
CuO+H2-to>Cu+H2O
2H2+O2-to>2H2O
H2+Br2->2HBr
2C+H2-to>C2H2
Đúng 2
Bình luận (0)
b) 2C + H2 -> (3000°C) C2H2
Br2 + H2 -> 2HBr
CuO + H2 -> (t°) Cu + H2O
O2 + 2H2 -> (t°) 2H2O
S + H2 -> H2S
a) 2Mg + O2 -> (t°) 2MgO
3Fe + 2O2 -> (t°) Fe3O4
C + O2 -> (t°) CO2
S + O2 -> (t°) SO2
4FeS2 + 11O2 -> (t°) 2Fe2O3 + 8SO2
C2H6O + 3O2 -> (t°) 2CO2 + 3H2O
2SO2 + O2 -> (t°, V2O5) 2SO3
Đúng 0
Bình luận (0)
a) Cacbon oxit CO tác dụng với khí oxi tạo ra cacbon đioxit. Hãy viết phương trình hóa học. b) Nếu muốn đốt cháy 20 mol CO thì phải dùng bao nhiêu mol O2 để sau phản ứng người ta chỉ thu được một chất khí duy nhất? c) Hãy điền vào những ô trống số mol các chất phản ứng và sản phẩm có ở những thời điểm khác nhau. Biết hỗn hợp CO và O2 ban đầu được lấy đúng tỉ lệ về số mol các chất theo phương trình hóa học.
Đọc tiếp
a) Cacbon oxit CO tác dụng với khí oxi tạo ra cacbon đioxit. Hãy viết phương trình hóa học.
b) Nếu muốn đốt cháy 20 mol CO thì phải dùng bao nhiêu mol O2 để sau phản ứng người ta chỉ thu được một chất khí duy nhất?
c) Hãy điền vào những ô trống số mol các chất phản ứng và sản phẩm có ở những thời điểm khác nhau. Biết hỗn hợp CO và O2 ban đầu được lấy đúng tỉ lệ về số mol các chất theo phương trình hóa học.
a) Phương trình phản ứng:
2CO + O2 → 2CO2
b) Theo phương trình 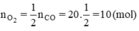
c) Hoàn chỉnh bảng
Thời điểm t1 nCO còn 15mol ⇒ nCO đã phản ứng = 20 - 15= 5mol
Theo pt nCO2 = nCO(pư) = 5 mol
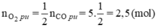 ⇒ nO2 còn lại = 10 - 2,5 = 7,5 mol
⇒ nO2 còn lại = 10 - 2,5 = 7,5 mol
Tương tự tính thời điểm t2 và thời điểm t3 ta được số liệu sau:
| Số mol | |||
| Các thời điểm | Các chất phản ứng | Sản phẩm | |
| CO | O2 | CO2 | |
| Thời điểm ban đầu t0 | 20 | 10 | 0 |
| Thời điểm t1 | 15 | 7,5 | 5 |
| Thời điểm t2 | 3 | 1,5 | 17 |
| Thời điểm kết thúc t3 | 0 | 0 | 20 |
Đúng 1
Bình luận (0)
Cho 1 lượng kẽm tác dụng với Axit clohiđric (HCl) thu được 2,24 lít khí hiđro theo sơ đồ phản ứng sau a) lập phương trình hóa học b) tính khối lượng Axit clohiđric c) khí Hiđro nặng hơn hay nhẹ hơn khí Oxi bao nhiêu lần
\(Zn+2HCl\rightarrow H_2\)
b)
Số mol của khí hidro là :
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\)
số mol của axit clohidric là :
0,1 . 2 = 0,2 mol
vậy khối lượng cua Axit clohidric là :
\(m_{HCl}=n_{HCl}.M_{HCl}=0,2.36,5=7,3g\)
Vậy....
Đúng 1
Bình luận (0)