Nếu cho một lượng kim loại Al,Zn,Fe và dung dịch HCl, dung dịch H2SO4 loãng. Để điều chế Khí Hiđro từ các kim loại trên nếu cùng một lượng kim loại thì dùng kim loại nào để thu được nhiều khí hiđro nhất, viết các PT để minh họa? DA Al thu được nhiều nhất

Những câu hỏi liên quan
Cho 10,8 gam kim loại nhôm tác dụng hoàn toàn với dung dịch axit sunfuric loãng (H2SO4). Tính: a. Thể tích hiđro thu được ở đktc? b. Nếu dùng lượng khí Hiđro trên để khử vừa đủ một lượng oxit kim loại X hóa trị II thì thu được 38,4 gam kim loại. Tìm kim loại X.
\(a,n_{Al}=\dfrac{10,8}{27}=0,4\left(mol\right)\\ PTHH:2Al+3H_2SO_{4\left(loãng\right)}\rightarrow Al_2\left(SO_4\right)_3+3H_2\uparrow\\ Theo.pt:n_{H_2}=\dfrac{3}{2}n_{Al}=\dfrac{3}{2}.0,4=0,6\left(mol\right)\\ b,PTHH:RO+H_2\underrightarrow{t^o}R+H_2O\\ Mol:0,6\leftarrow0,6\rightarrow0,6\\ M_R=\dfrac{38,4}{0,6}=64\left(\dfrac{g}{mol}\right)\\ \Rightarrow R.là.Cu\)
Đúng 2
Bình luận (0)
2Al+3H2SO4->Al2(SO4)3+3H2
0,4---------------------------------0,6
n Al=0,4 mol
=>VH2=0,6.22,4=13,44l
b)
H2+XO-to>X+H2O
0,6------------0,6
=>0,6=\(\dfrac{38,4}{X}\)
=>X=64 đvC
=>X là Cu(đồng)
=>X=48
Đúng 1
Bình luận (0)
Trong PTN có các kim loại Mg và Zn, dung dịch axit clohiđric (HCl)a) Viết các PTPƯ có thể điều chế khí Hiđrob) Nếu cho cùng khối lượng các kim loại trên td vs axit dư thì kim loại nào cho nhiều khí Hiđro hơnGiups mik vs mik đag cần gấp mik c.ơn trước
Đọc tiếp
Trong PTN có các kim loại Mg và Zn, dung dịch axit clohiđric (HCl)
a) Viết các PTPƯ có thể điều chế khí Hiđro
b) Nếu cho cùng khối lượng các kim loại trên td vs axit dư thì kim loại nào cho nhiều khí Hiđro hơn
Giups mik vs mik đag cần gấp![]()
![]() mik c.ơn trước
mik c.ơn trước
a, PT: \(Mg+2HCl\rightarrow MgCl_2+H_2\)
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
b, Coi mMg = mZn = 1 (g)
Ta có: \(n_{H_2\left(Mg\right)}=n_{Mg}=\dfrac{1}{24}\left(mol\right)\)
\(n_{H_2\left(Zn\right)}=n_{Zn}=\dfrac{1}{65}\left(mol\right)\)
\(\Rightarrow\dfrac{1}{24}>\dfrac{1}{65}\)
Vậy: Mg cho nhiều khí H2 hơn.
Đúng 2
Bình luận (1)
Câu 19: Trong phòng thí nghiệm có các kim loại Zn và Fe, các dung dịch axit H2SO4 loãng và HCl. Muốn điều chế được 2,24 lít khí H2 (đktc) phải dùng kim loại nào, axit nào để chỉ cần một khối lượng nhỏ nhất?A. Fe và H2SO4 B. Fe và HCl C. Zn và H2SO4 D. Zn và HClCâu 20: Khử 5,6g sắt(III) oxit bằng khí hiđro .Thể tích khí hiđro(đktc) cần dùng là:A. 5,04 lít B. 6,72 lit C. 2,24 lít D. 3,36 lítCâu 21: Số gam sắt cần tác dụng hết với axit clohiđr...
Đọc tiếp
Câu 19: Trong phòng thí nghiệm có các kim loại Zn và Fe, các dung dịch axit H2SO4 loãng và HCl. Muốn điều chế được 2,24 lít khí H2 (đktc) phải dùng kim loại nào, axit nào để chỉ cần một khối lượng nhỏ nhất?
A. Fe và H2SO4 B. Fe và HCl C. Zn và H2SO4 D. Zn và HCl
Câu 20: Khử 5,6g sắt(III) oxit bằng khí hiđro .Thể tích khí hiđro(đktc) cần dùng là:
A. 5,04 lít B. 6,72 lit C. 2,24 lít D. 3,36 lít
Câu 21: Số gam sắt cần tác dụng hết với axit clohiđric để cho 4,48 lít khí hiđro (đktc) là:
A. 11,2g B.28g C. 5,6g D. 3,7g
Cho các kim loại kẽm, nhôm, sắt lần lượt tác dụng với dung dịch axit sunfuric loãng. a) Viết các phương trình phản ứng. b) Cho cùng một khối lượng các kim loại trên tác dụng hết với axit sunfuric? Kim loại nào cho nhiều khi hiđro nhất? c) Nếu thu được cùng một thể tích khí hiđro thì khối lượng kim loại nào nhỏ nhất?
Đọc tiếp
Cho các kim loại kẽm, nhôm, sắt lần lượt tác dụng với dung dịch axit sunfuric loãng.
a) Viết các phương trình phản ứng.
b) Cho cùng một khối lượng các kim loại trên tác dụng hết với axit sunfuric? Kim loại nào cho nhiều khi hiđro nhất?
c) Nếu thu được cùng một thể tích khí hiđro thì khối lượng kim loại nào nhỏ nhất?
a) Phương trình phản ứng:
Zn + H2SO4 → ZnSO4 + H2
Fe + H2SO4loãng → FeSO4 + H2
2Al+ 3H2SO4 → Al2(SO4)3 + 3H2
b) Giả sử cho cùng một khối lượng là a g kim loại kẽm sắt và nhôm
Zn + H2SO4 → ZnSO4 + H2 (1)
Fe + H2SO4loãng → FeSO4 + H2 (2)
2Al+ 3H2SO4 → Al2(SO4)3 + 3H2 (3)
Ta có 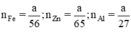
Theo pt nH2 (1) = nZn = 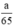 mol
mol
nH2 (2) = nFe = 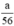 mol
mol
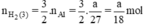
Như vậy ta nhận thấy 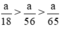 ⇒ nH2 (3) > nH2 (2) > nH2 (1)
⇒ nH2 (3) > nH2 (2) > nH2 (1)
Như vậy cho cùng một lượng kim loại tác dụng với axit H2SO4 loãng dư thì nhôm cho nhiều khí hidro hơn, sau đó đến sắt và ít nhất là kẽm
c) Nếu thu được cùng một lượng khí hidro thì khối lượng kim loại ít nhất là nhôm, sau đó đến sắt, cuối cùng là kẽm.
Đúng 1
Bình luận (0)
Trong phòng thí nghiệm có các kim loại Mg , Zn và Fe, các dung dịch axit H2SO4 loãng và HCl. Muốn điều chế được 2,24 lít khí H2 (đktc) phải dùng kim loại nào, axit nào để chỉ cần một khối lượng nhỏ nhất ?
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1\left(mol\right)\)
PTHH:
Mg + 2HCl ---> MgCl2 + H2
Zn + 2HCl ---> ZnCl2 + H2
Fe + 2HCl ---> FeCl2 + H2
Mg + H2SO4 ---> MgSO4 + H2
Zn + H2SO4 ---> ZnSO4 + H2
Fe + H2SO4 ---> FeSO4 + H2
Theo các pthh trên: \(\left\{{}\begin{matrix}n_{HCl}=2n_{H_2}=2.0,1=0,2\left(mol\right)\\n_{H_2SO_4}=n_{H_2}=0,1\left(mol\right)\\n_{Fe}=n_{Zn}=n_{Mg}=n_{H_2}=0,1\left(mol\right)\end{matrix}\right.\)
\(\rightarrow\left\{{}\begin{matrix}\left\{{}\begin{matrix}m_{HCl}=0,2.36,5=7,3\left(g\right)\\m_{H_2SO_4}=98.0,1=9,8\left(g\right)\end{matrix}\right.\\\left\{{}\begin{matrix}m_{Fe}=0,1.56=5,6\left(g\right)\\m_{Zn}=0,1.65=6,5\left(g\right)\\m_{Mg}=0,1.24=2,4\left(g\right)\end{matrix}\right.\end{matrix}\right.\rightarrow\left\{{}\begin{matrix}m_{HCl}< m_{H_2SO_4}\\m_{Mg}< m_{Fe}< m_{Zn}\end{matrix}\right.\)
Vậy chọn HCl và Mg thì đièu chế vs lượng nhỏ nhất
Đúng 4
Bình luận (0)
\(n_{H_2}=\dfrac{2,24}{22,4}=0,1mol\)
Nếu dùng HCl:
\(n_{HCl}=2n_{H_2}=0,2mol\Rightarrow m_{HCl}=0,2\cdot36,5=7,3g\)
Nếu dùng \(H_2SO_4\) :
\(n_{H_2SO_4}=n_{H_2}=0,1mol\Rightarrow m_{H_2SO_4}=0,1\cdot98=9,8g\)
\(\Rightarrow\)Dùng \(HCl\) để cần một khối lượng nhỏ nhất.
Nếu dùng Mg:
\(Mg+2HCl\rightarrow MgCl_2+H_2\)
0,1 0,1
\(m_{Mg}=0,1\cdot24=2,4g\)
Nếu dùng Zn:
\(Zn+2HCl\rightarrow ZnCl_2+H_2\)
0,1 0,1
\(m_{Zn}=0,1\cdot65=6,5g\)
Nếu dùng Fe:
\(Fe+2HCl\rightarrow FeCl_2+H_2\)
0,1 0,1
\(m_{Fe}=0,1\cdot56=5,6g\)
\(\Rightarrow\)Dùng Mg để có khối lượng nhỏ nhất.
Vậy dùng kim loại Mg và axit HCl.
Đúng 2
Bình luận (0)
Cho 4,8 gam kim loại magie tác dụng hoàn toàn với dung dịch axit HCl. Tính: a. Thể tích hiđro thu được ở đktc? c. Nếu dùng lượng khí Hiđro trên để khử vừa đủ một lượng oxit kim loại R hóa trị II thì thu được 12,8gam kim loại. Tìm kim loại R.
Mg+2HCl->MgCl2+H2
0,2-----------------------0,2
RO+H2-to>R+H2O
0,2-------------0,2
n Mg=\(\dfrac{4,8}{24}\)=0,2 mol
=>VH2=0,2.22,4=4,48l
->0,2=\(\dfrac{12,8}{R}\)
=>R=64 g\mol
=>R là Cu(đồng)
Đúng 2
Bình luận (0)
Cho kim loại : Zn,Alo,Fe,Mg lần lượt tác dụng với dung dịch H2SO4 loãng. Nếu cho cùng một khối lượng kim loại trên tác dụng hết với axit ,thì kim loại nào cho nhiều khí h2 nhất
Cho 5,4 gam kim loại nhôm tác dụng hoàn toàn với dung dịch axit clohiđric (HCl). Tính: a. Thể tích hiđro thu được ở đktc? b. Nếu dùng lượng khí Hiđro trên để khử vừa đủ một lượng oxit kim loại X hóa trị II thì thu được 19,5 gam kim loại. Tìm kim loại X.
2Al+3H2SO4->Al2(SO4)3+3H2
0,2-----------------------------------0,3
n Al=0,2 mol
=>VH2=0,3.22,4=6,72l
b)
XO+H2-to>X+H2O
0,3-------------0,3
=>0,3=\(\dfrac{19,5}{X}\)
=>X là Zn( kẽm)
Đúng 3
Bình luận (0)
a.\(n_{Al}=\dfrac{5,4}{27}=0,2mol\)
\(2Al+6HCl\rightarrow2AlCl_3+3H_2\)
0,2 0,3 ( mol )
\(V_{H_2}=0,3.22,4=6,72l\)
b.\(n_X=\dfrac{19,5}{M_X}\)
\(XO+H_2\rightarrow\left(t^o\right)X+H_2O\)
\(\dfrac{19,5}{M_X}\) \(\dfrac{19,5}{M_X}\) ( mol )
Ta có:
\(\dfrac{19,5}{M_X}=0,3\)
\(\Leftrightarrow M_X=65\)
=> X là kẽm (Zn)
Đúng 2
Bình luận (0)
\(a,n_{Al}=\dfrac{5,4}{27}=0,2\left(mol\right)\\ PTHH:2Al+6HCl\rightarrow AlCl_3+3H_2\uparrow\\ Theo.pt:n_{H_2}=\dfrac{3}{2}n_{Al}=\dfrac{3}{2}.0,2=0,3\left(mol\right)\\ V_{H_2}=0,3.22,4=6,72\left(l\right)\\ b,PTHH:RO+H_2\underrightarrow{t^o}R+H_2O\\ Mol:0,3\leftarrow0,3\rightarrow0,3\\ M_R=\dfrac{19,5}{0,3}=65\left(\dfrac{g}{mol}\right)\\ \Rightarrow R.là.Zn\)
Đúng 2
Bình luận (0)
Xem thêm câu trả lời
Trong phòng thí nghiệm có các kim loại Mg , Zn và Fe, các dung dịch axit H2SO4 loãng và HCl. Muốn điều chế được 1,12 lít khí H2 (đktc) phải dùng kim loại nào, axit nào để chỉ cần một khối lượng nhỏ nhất ?
a. Fe và HCl
b. Fe và H2SO4
c. Mg và HCl
d. Zn và H2SO4
\(n_{H_2}=\dfrac{1,12}{22,4}=0,05\left(mol\right)\)
- Nếu dùng HCl: nHCl = 2.nH2 = 0,1 (mol)
=> mHCl = 0,1.36,5 = 3,65 (g)
- Nếu dùng H2SO4: nH2SO4 = nH2 = 0,05 (mol)
=> mH2SO4 = 0,05.98 = 4,9 (g)
=> Dùng HCl để cần khối lượng nhỏ nhất
=> 1 trong 2 đáp án A, C đúng
- Nếu dùng Fe
PTHH: Fe + 2HCl --> FeCl2 + H2
0,05<-0,1
=> mFe = 0,05.56 = 2,8 (g)
- Nếu dùng Mg
PTHH: Mg + 2HCl --> MgCl2 + H2
0,05<--0,1
=> mMg = 0,05.24 = 1,2 (g)
=> Dùng Mg để có khối lượng nhỏ nhất
=> Chọn C
Đúng 3
Bình luận (0)

















